はじめに
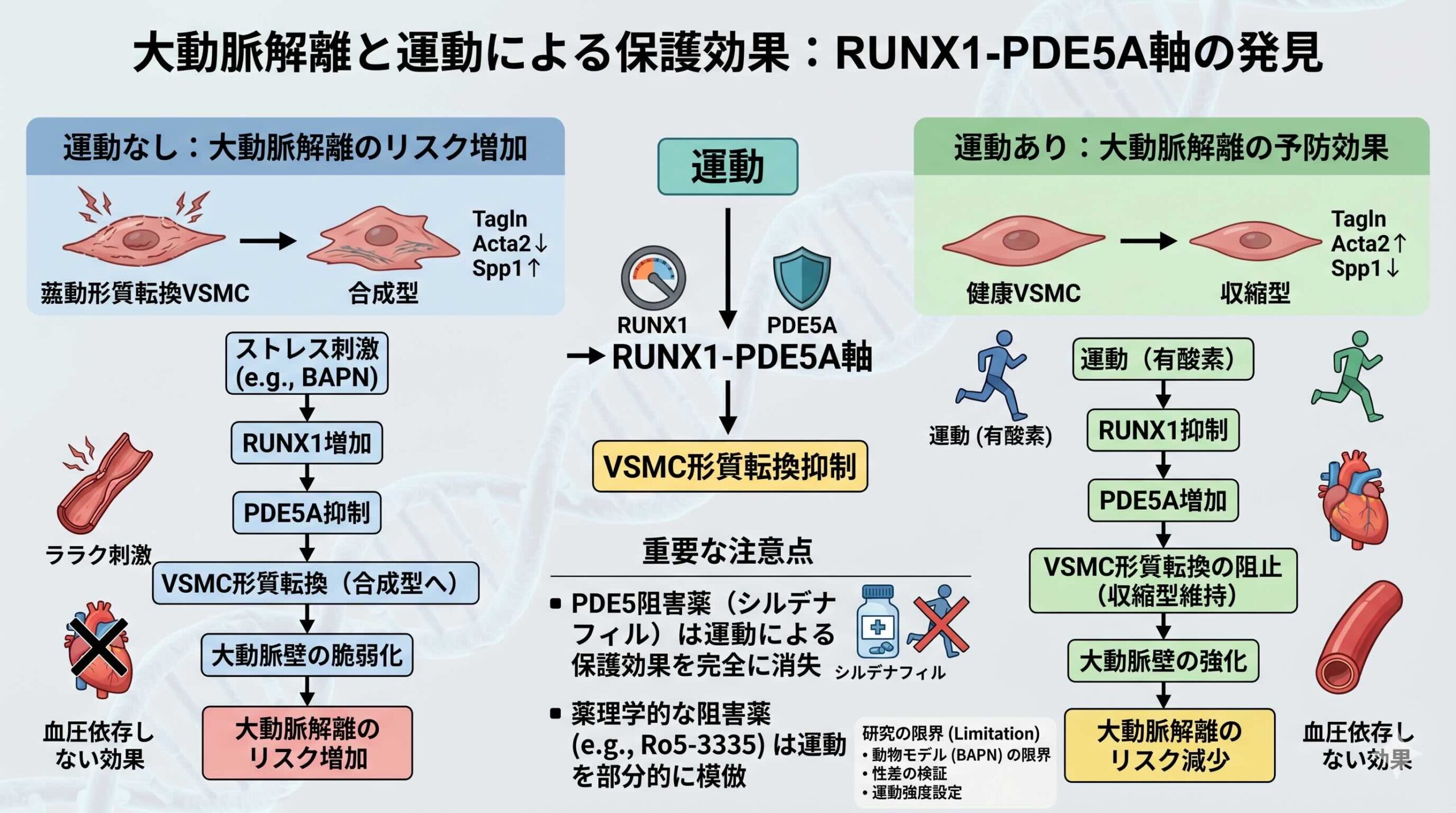
大動脈解離(Aortic dissection ;AD)は、前触れもなく生命を脅かす、循環器領域における最も劇的かつ壊滅的な救急疾患の一つです。大動脈中膜が裂け、偽腔が形成されるこの病態は、発症後一時間ごとに生存率が低下していくという残酷なタイムリミットを突きつけます。これまで、運動が心血管健康に寄与することは広く知られていましたが、大動脈解離という極めて構造的な破壊を伴う疾患に対して、運動がどのような分子言語で対話しているのかは、長い間ブラックボックスの中にありました。2026年に発表されたZhangらによる革新的な研究は、血管平滑筋細胞(Vascular smooth muscle cell;VSMC)の運命を左右する分子スイッチを特定し、運動が単なる健康習慣ではなく、大動脈の構造的レジリエンスを強化する強力な分子介入であることを証明しました。
研究プロトコールの概要
P(対象):3から4週齢の雄性C57BL/6Jマウス(BAPN誘発大動脈解離モデル)および大動脈解離患者から提供された大動脈組織
I(介入):12週間の強制トレッドミルによる有酸素運動(週5回、漸増負荷)
C(比較):自由活動のみを行う非運動(セデンタリー)群
O(結果):生存率、大動脈解離の発生率、大動脈破裂率、最大大動脈径、血管平滑筋細胞の形質転換マーカー発現量
研究デザイン:マウスを用いた介入研究およびヒト病理組織の横断的解析
忍び寄る大動脈の危機と血管平滑筋の裏切り
大動脈の柔軟性と強度を支えているのは、中膜に存在する血管平滑筋細胞です。健康な血管では、これらの細胞は「収縮型(contractile phenotype/contractile state)」という安定した状態にあり、血管の弾性を維持しています。しかし、病的なストレス下では、平滑筋細胞は「合成型(synthetic phenotype/synthetic state)」へとその姿を変えてしまいます。これは細胞の形質転換と呼ばれ、収縮能力を失う代わりに、周囲の細胞外マトリックスを分解し、炎症を引き起こすタンパク質を分泌し始めます。この細胞の裏切りこそが、大動脈の壁を脆くし、解離を引き起こす真犯人の一つです。
大動脈解離患者から採取された組織の解析では、この形質転換が明確に確認されました。収縮型マーカーであるMYH11やCNN1、alpha-SMAの発現が著しく低下している一方で、合成型の象徴であるオステオポンチン(osteopontin;OPN)が増加していたのです。研究チームは、この細胞の運命決定プロセスに、運動がどのように介入できるのかを探索し始めました。
運動がもたらす劇的な生存率の向上と解離抑制の衝撃
マウスモデルを用いた実験結果は、驚くべきものでした。β-aminopropionitrile;BAPN※という試薬を用いて大動脈を脆弱化させたマウスのうち、運動を行わなかった群では、84日目までに44匹中23匹が死亡するという極めて低い生存率を示しました。これに対し、トレッドミル運動を継続した群では、37匹中死亡したのはわずか8匹に留まりました。統計学的な生存率の差は一目瞭然であり、運動が大動脈解離の死神を遠ざけることが示されました。
さらに具体的な数値を見ると、運動の予防効果がより際立ちます。非運動群では31/44(約70.5%)のマウスが解離を発症し、23/44(約52.3%)が破裂に至りました。しかし、運動群では解離の発生率は13/37(約35.1%)へと半減し、破裂率も8/37(約21.6%)へと劇的に低下しました。重要なのは、この保護効果が血圧の変動に依存しないという点です。収縮期血圧は両群で有意な差が認められず、運動は血圧を下げるという間接的な効果ではなく、血管壁そのものを内側から作り変える細胞自律的なメカニズムによって効果を発揮していることが明らかになりました。
※ 大動脈が強い血圧に耐えられるのは、血管の壁にコラーゲンやエラスチン(弾性線維)といった頑丈な繊維が、ジャングルジムのように複雑に絡み合って補強しているからです。この繊維同士を結びつける(架橋する)役割を果たすのが、リシルオキシダーゼ(LOX)という酵素です。このマウスには、飲料水を通じてベータアミノプロピオニトリル(BAPN)という化合物が投与されています。BAPNはこのLOX酵素の働きを完全にブロックしてしまいます。
失われた守護者PDE5A:大動脈解離における分子の崩壊
研究チームはRNAシーケンシングを用い、運動によって発現が変化する数千の遺伝子の中から、真の鍵となる分子を追い求めました。そこで浮上したのがphosphodiesterase 5A;PDE5A(ホスホジエステラーゼ5A)です。PDE5Aは、血管弛緩や平滑筋の恒常性維持に重要な役割を果たすcGMPという二次メッセンジャーを分解する酵素です。意外なことに、大動脈解離の病変部では、このPDE5Aが極端に枯渇していることが分かりました。
ヒトの病変組織においても、PDE5AのmRNAおよびタンパク質レベルは、正常な遠位組織と比較して顕著に低下していました。一方で、運動を行ったマウスの大動脈では、PDE5Aの発現が力強く回復していたのです。
この発見の重要性を検証するため、研究チームは平滑筋細胞特異的にPDE5Aを過剰発現させる遺伝子治療(AAV-Pde5a)をマウスに施しました。その結果、運動をさせずとも、PDE5Aが増えるだけで生存率は劇的に改善し(死亡率 2/25 vs 11/25)、大動脈の破裂はほぼ完璧に抑えられました。つまり、PDE5Aこそが血管の強度を保つための守護者であったのです。
影の抑制者RUNX1:運動が解除する負の連鎖
では、なぜ大動脈解離ではPDE5Aが減り、運動によって増えるのでしょうか。この謎を解くため、研究チームはPDE5Aのプロモーター領域に結合する転写因子を探索しました。そこで見つかった黒幕がRunt-related transcription factor 1;RUNX1です。RUNX1は通常、造血幹細胞の分化などに関わる因子ですが、血管平滑筋細胞においてはPDE5Aの産生をストップさせる「抑制的なブレーキ」として機能していました。
大動脈解離の状態では、血管壁でRUNX1が増加し、PDE5Aのスイッチをオフにしてしまいます。しかし、運動はこのRUNX1の発現を強力に抑制することが判明しました。特に、マウスにおけるRunx1bというアイソフォームが運動によって抑制されることで、PDE5Aへのブレーキが解除され、血管は再び収縮型のアイデンティティを取り戻すのです。クロマチン免疫沈降(ChIP)実験により、RUNX1がPDE5Aのプロモーターに直接結合していることが証明され、運動、RUNX1、PDE5A、そして平滑筋の形質の間に、一直線の論理的な因果関係が確立されました。
形質転換という細胞の変身を封じ込める
運動、あるいはRUNX1の阻害剤(Ro5-3335)を用いることで、平滑筋細胞の内部では何が起きているのでしょうか。細胞生物学的な視点で見ると、RUNX1の抑制によって復活したPDE5Aは、cGMP-PKG経路を安定化させ、細胞が「合成型」という破壊的なモードに突入するのを防ぎます。
実験では、血小板由来成長因子(PDGF-BB)によって合成型への変身を促された平滑筋細胞に対し、RUNX1を阻害すると、細胞の増殖が抑えられ、炎症性サイトカイン(IL-6やMMP9)など)の放出も劇的に減少しました。運動は、血管壁が炎症とマトリックス分解の悪循環に陥るのを、転写レベルで未然に防いでいるのです。これにより、大動脈中膜の弾性線維の断裂が最小限に抑えられ、血管壁の構造的な整合性が保たれることになります。
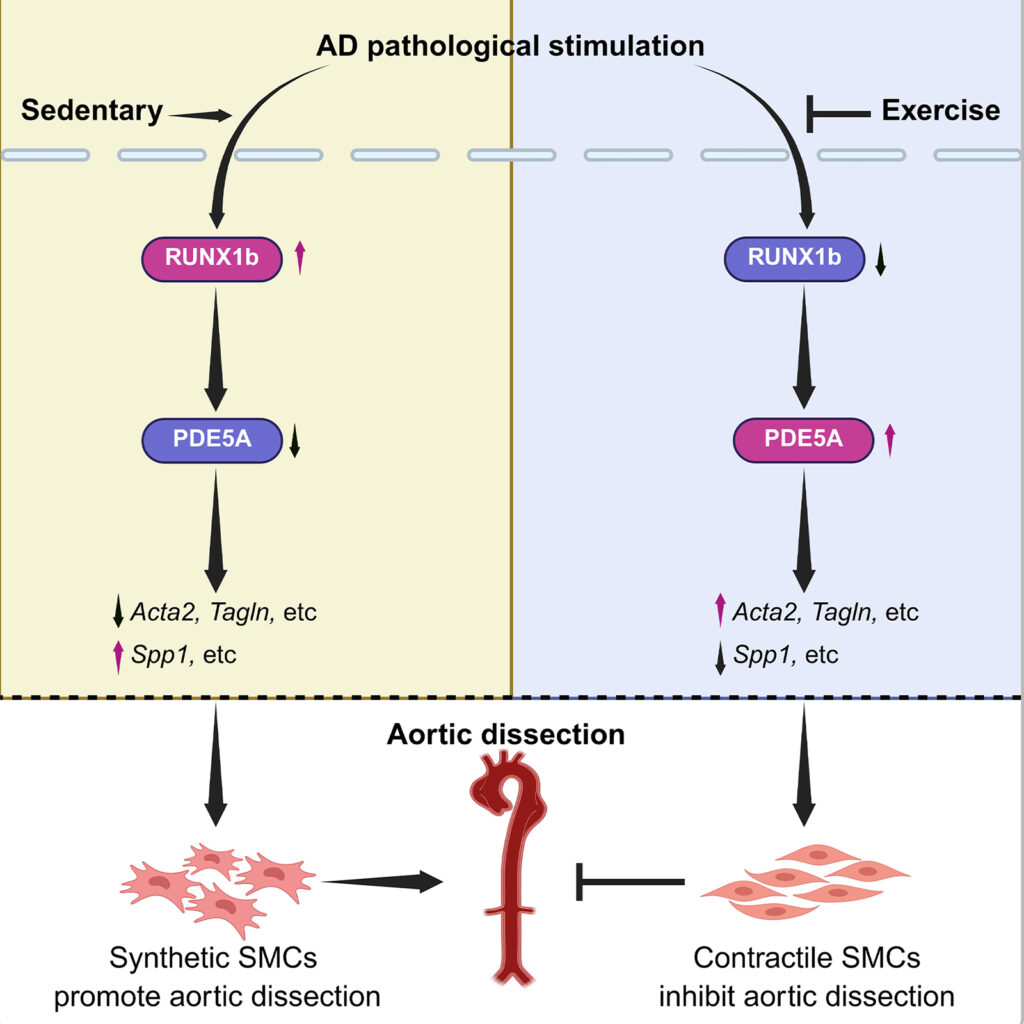
(図)有酸素運動は、転写因子RUNX1(ラント関連転写因子1)を阻害することで大動脈壁の完全性を促進し、血管平滑筋細胞における酵素PDE5A(ホスホジエステラーゼ5A)の発現を増加させます。RUNX1-PDE5A経路は、血管平滑筋細胞の収縮性表現型を維持するために不可欠です。
既存研究に対するこの研究の新規性
本研究の最大の新規性は、運動による大動脈解離抑制のメカニズムを、RUNX1-PDE5Aという具体的なシグナル軸として同定した点にあります。これまでの研究では、運動がMMPの発現を抑えるといった現象論的な報告に留まっていましたが、本研究は「なぜMMPが抑えられるのか」という問いに対し、平滑筋細胞の形質転換という根本的なプロセスに遡って回答を提示しました。
また、PDE5Aという、勃起不全薬などの標的として既に薬理学的に馴染みの深い分子が、大動脈解離の予防という全く新しい文脈で登場したことも驚きを持って迎えられました。さらに、運動の効果を薬理学的なRUNX1阻害や遺伝子治療によって再現できることを示した点は、将来的な臨床応用の可能性を大きく広げるものです。
本研究の限界(Limitation)
本研究にはいくつかの限界も存在します。まず、使用されたBAPNモデルは、細胞外マトリックスの架橋を阻害することで血管を弱体化させるものであり、ヒトにおける高血圧を背景とした解離の全プロセスを完全に模倣しているわけではありません。次に、本研究は主に雄のマウスを用いて行われており、性差によるホルモンの影響が大動脈解離の発生や運動の効果にどのように関与するかについては、今後の検証が必要です。
また、運動の強度設定についても議論の余地があります。実験で行われた強制的な有酸素運動は、人間における「中強度」の運動に相当すると想定されていますが、既に大動脈瘤や解離のリスクを抱えている患者がどの程度の強度で運動を行うべきかという臨床的なガイドラインを策定するためには、さらなるヒトを対象とした研究が不可欠です。
実践への橋渡し:明日から始める「動脈のレジリエンス」強化
この論文が私たちに示唆する最大のメッセージは、運動は大動脈を物理的に強くする「最も安価で効果的な薬」であるということです。明日から活かせる知見を以下にまとめます。
第一に、有酸素運動の定期的実施の推奨です。週に数回、少し息が上がる程度の中強度の有酸素運動(早歩きやジョギングなど)は、RUNX1を抑え、大動脈の平滑筋を「収縮型」に維持する強力な転写プログラムを起動させます。これは高血圧になる前の段階から、血管壁の「内なる力」を高める予防策となります。
第二に、運動習慣の重要性を裏付ける分子基盤の理解です。単に「心臓に良いから」ではなく、「大動脈平滑筋の形質転換を防ぎ、PDE5Aという守護者を維持するため」という明確なメカニズムを理解することで、運動に対するモチベーションを科学的に補強できます。
第三に、薬理学的介入への期待です。運動が困難な高齢者や身体的制約のある方にとって、RUNX1-PDE5A軸をターゲットとした新規薬剤の開発は、将来的に大きな希望となります。今はまだ研究段階ですが、この軸の存在を知ることは、血管老化を防ぐためのライフスタイルの指針となるでしょう。
私たちは今、運動という古くからの知恵が、大動脈解離という現代医学の難敵を打ち破るための、洗練された分子生物学的介入であることを知りました。明日からの一歩が、あなたの大動脈の細胞一つ一つの運命を変え、未来の破裂を未然に防ぐための強力なブレーキとなるのです。
参考文献
Zhang Y, Wu C, Du D, et al. Exercise Attenuates Aortic Dissection Via PDE5A-Mediated Inhibition of Vascular Smooth Muscle Cell Phenotypic Switch. Arterioscler Thromb Vasc Biol. 2026;46:e324293. DOI: 10.1161/ATVBAHA.125.324293.
おまけ:RUNX1bの暴走
血管にかかる様々なストレスがある状況下で、運動による「抑制ブレーキ」が効かないためにRUNX1bが暴走してしまうという構図です 。
RUNX1bを増加させる主な要因
この研究および背景知識から、RUNX1b(またはRUNX1全体)を増加、あるいは活性化させる要因として以下のものが挙げられています。
・ 病的な刺激と成長因子(PDGF-BB)
細胞レベルでは、血小板由来成長因子-BB(PDGF-BB)の刺激がRUNX1のレベルを有意に上昇させます 。 また、実験的な大動脈解離モデルで使用されるBAPNの投与によって、マウスの大動脈内でRUNX1bが顕著に増加することが確認されています 。
・ 炎症と酸化ストレス
慢性的な低強度の炎症や酸化ストレスは、RUNX1の強力な誘導因子(Inducer)として知られています 。 血管壁の炎症トーンが高まると、RUNX1を介した転写プログラムが起動し、平滑筋細胞の形質転換が促進されます 。
・ 代謝ストレス
インスリン抵抗性の悪化や、血中の脂質プロファイルの悪化などの代謝異常も、血管平滑筋細胞におけるRUNX1の病的な活性化に寄与すると考えられています 。 運動はこれらの代謝状態を改善することで、間接的にRUNX1を抑制しています 。
・ メカニカルストレス(血流の物理的刺激)
血管壁にかかる流体せん断応力(Shear stress)や、拍動による周期的な伸展(Cyclic stretch)などの力学的刺激は、メカノセンシティブな経路を通じてRUNX1を含む転写因子の発現を調節しています 。 異常な血流負荷や血管壁への過度なストレッチは、RUNX1bを介した病的なリモデリングを引き起こす要因となります 。
おまけのまとめ
「高脂肪食などの不摂生(代謝ストレス)」「慢性炎症(酸化ストレス)」「喫煙などの血管への直接的ダメージ(成長因子の放出)」といった介入は、すべてRUNX1bを増加させる方向に働きます。
運動は、骨格筋から放出されるマイオカイン(イリシンなど)や全身的な代謝改善を通じて、これらの悪影響を中和し、RUNX1bという「血管のブレーキ役」を抑え込んでくれているのです 。