はじめに
大動脈弁狭窄症(Aortic Valve Stenosis, AVS)は、加齢に伴い進行する疾患であり、特に繊維性石灰化大動脈弁狭窄症(Fibrocalcific Aortic Valve Stenosis, FCAVS)は、現在有効な薬物療法が存在せず、外科的治療に依存せざるを得ない状況が続いています。しかし、最近の研究では、可溶性グアニル酸シクラーゼ(sGC)のシグナル伝達がこの疾患の進行に深く関与している可能性が示され、新たな治療ターゲットとして注目されています。本稿では、Zhangらの研究をもとに、sGCの再活性化という革新的な治療戦略について解説します。
FCAVSの病態と現在の治療法の限界
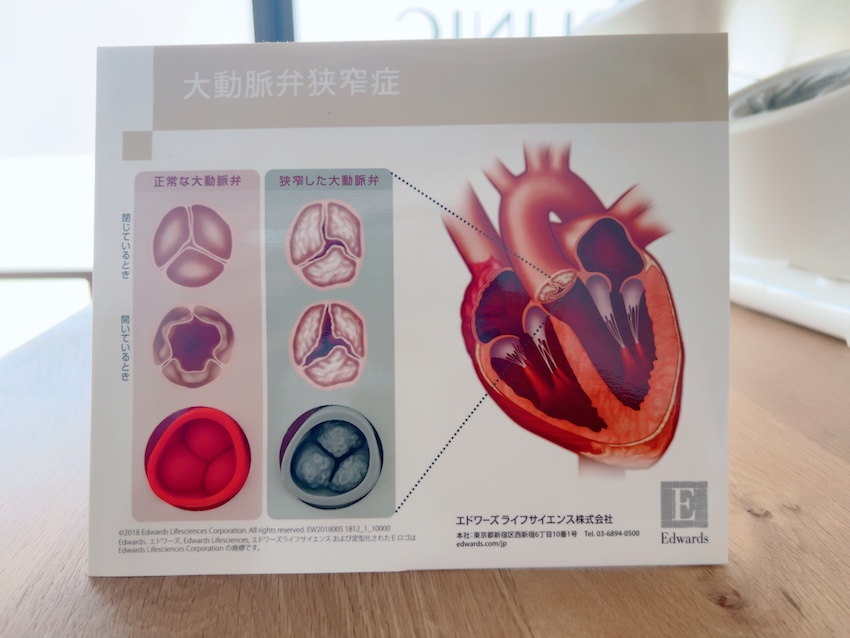
FCAVSは、弁尖の石灰化と線維化が進行することで弁の可動性が低下し、心臓のポンプ機能に過剰な負荷をかける疾患です。病態の進行により、左室肥大や収縮能の低下、最終的には心不全へと至ります。
これまでの研究では、FCAVSの進行に関与する因子として、脂質異常症や慢性炎症、機械的ストレス、酸化ストレスの増加が指摘されてきました。一部の研究では、スタチンやビスフォスフォネートが石灰化の進行を抑制する可能性が示唆されましたが、ランダム化試験では明確な有効性が証明されず、現在も薬物療法の確立には至っていません。
sGCシグナル伝達の役割
可溶性グアニル酸シクラーゼ(sGC)は、一酸化窒素(NO)によって活性化され、環状グアノシン一リン酸(cGMP)の産生を介して血管拡張や抗炎症作用を発揮する重要な酵素です。NO-sGC-cGMP経路は血管や心臓の機能調節に重要な役割を果たしています。また、骨代謝にも関与していることが近年明らかになってきました。しかし、FCAVS患者の弁組織では、sGCの機能が大幅に低下しており、NOシグナル伝達の破綻が病態の進行に寄与している可能性が示唆されています。具体的には、内皮型一酸化窒素合成酵素(eNOS)の発現が減少し、cGMPの産生が抑制されていました。また、cGMPの分解を促進するホスホジエステラーゼ5A(PDE5A)の発現が増加していることも確認されました。
Zhangらの研究では、FCAVS患者の弁組織において、sGCの主要なサブユニット(GUCY1A2, GUCY1A3, GUCY1B2, GUCY1B3)の発現は増加しているものの、機能的には低下していることが明らかになりました。これは、酸化ストレスによってsGCが酸化型となり、通常のNOによる活性化が困難になっているためと考えられます。
sGCと骨代謝の関係:石灰化制御の新たな視点
骨形成とsGC経路の役割
骨形成は、骨形成因子(BMP: Bone Morphogenetic Protein)のシグナル伝達を介して制御され、特にBMP2は骨芽細胞(osteoblast)の分化と石灰化を促進する重要な因子です。
この過程には、Runx2(Runt-related transcription factor 2)やOsterix(SP7)などの転写因子が関与し、骨基質タンパク質の発現やミネラル沈着を促します。
一方、可溶性グアニル酸シクラーゼ(sGC)-cGMP-プロテインキナーゼG(PKG)経路は、心血管系や平滑筋の調節だけでなく、骨代謝にも関与していることが近年明らかになってきました。
sGCは、骨形成と石灰化のバランスを制御する可能性があり、特に以下のメカニズムを介して骨代謝に影響を与えると考えられます。
sGC-cGMP経路が骨形成に及ぼす影響
sGCは一酸化窒素(NO)と結合し、cGMPの産生を促進することでPKGを活性化します。この経路は以下の2つの側面で骨形成および石灰化に影響を与えます。
(1)BMP2シグナルの抑制
- BMP2 → SMAD1/5/8 → Runx2 / Osterix → 骨形成促進
- BMP2はSMADシグナルを介してRunx2やOsterixを活性化し、骨芽細胞の成熟と石灰化を促します。
- sGCが活性化されると、BMP2シグナルの抑制が起こり、Runx2やOsterixの発現が低下することが示唆されています。
- 実際に、アタシグアット(sGC活性化薬)はBMP2シグナルを抑制し、弁石灰化を抑制する効果があると報告されています。
(2)抗炎症・抗酸化作用
- 酸化ストレスや炎症性サイトカイン(IL-6, TNF-α)が骨リモデリングを促進
- 酸化ストレスは骨リモデリングの促進因子となり、特に大動脈弁狭窄症(AS)では、局所的な炎症が骨形成プロセスを促進することが知られています。
- sGCの活性化により、抗酸化酵素(SOD, catalase)の発現が増加し、炎症性サイトカインの発現が抑制されることが示されています。
- 結果として、炎症性の骨リモデリングが抑制され、異常な石灰化が減少する可能性があります。
大動脈弁石灰化とsGCの関係
なぜsGCが大動脈弁石灰化に関連するのか?
ASの進行過程では、骨と類似した組織変化(異所性石灰化)が起こることが知られています。
通常の骨組織では、sGC活性化が骨形成を促進する場合もあるのに対し、異所性石灰化の抑制にはsGCが重要な役割を果たす可能性があります。
- 大動脈弁石灰化では、BMP2シグナルが異常に活性化
- BMP2の異常活性化により、Runx2やOsterixが過剰発現し、弁組織の線維芽細胞が骨芽細胞様に分化してしまう。
- sGC経路が抑制されると、BMP2の異常活性化が進行し、石灰化が加速する。
- sGC活性化薬(例:アタシグアット)によるBMP2シグナルの抑制
- sGCの活性化によりcGMPの産生が増加し、PKGが活性化される。
- PKGはRunx2/Osterix経路を抑制し、大動脈弁の石灰化を抑制する可能性がある。
このことから、sGCの活性化が異所性石灰化を抑制する新しい治療ターゲットとなる可能性が高まっています。
sGCと骨代謝の今後の研究課題
現在、sGCと骨代謝に関する研究は発展途上であり、以下の課題が残されています。
- 骨粗鬆症との関連性
- sGC活性化薬が、骨形成を抑制することで、正常な骨代謝にも影響を与える可能性がある。
- 長期的なsGC活性化が骨密度に与える影響を検討する必要がある。
- 異所性石灰化と骨組織の違い
- 骨組織と大動脈弁石灰化では、細胞環境やシグナル伝達が異なるため、sGCの作用が異なる可能性がある。
- AS患者におけるsGC活性の変化を詳細に調査し、標的治療を確立する必要がある。
- sGC刺激薬とsGC活性化薬の違い
- sGC刺激薬(ベルイシグアト、リオシグアト)は、NOが存在する環境でsGCを活性化するが、酸化ストレス下では効果が低下する可能性がある。
- 一方、sGC活性化薬(アタシグアットなど)は酸化型sGCをターゲットとするため、大動脈弁石灰化においてより有効である可能性が高い。
sGCと骨代謝の関係のまとめ
sGCは、骨代謝と異所性石灰化の両方に関与しており、特に異常な石灰化が進行する疾患(大動脈弁狭窄症など)において新たな治療標的として注目されています。
- sGC活性化により、BMP2シグナルの抑制、Runx2/Osterixの低下が起こり、大動脈弁石灰化が抑制される可能性がある。
- cGMP-PKG経路を活性化することで、炎症性石灰化を抑制し、異所性石灰化の進行を遅らせることが期待される。
- 今後の課題として、骨密度への影響、異所性石灰化との違い、sGC刺激薬と活性化薬の適応の違いを明確にする必要がある。
酸化型sGCを特異的に活性化する薬剤「アタシグアト」
アタシグアト(Ataciguat)は、酸化型sGCを特異的に活性化する化合物であり、NOに依存せずにsGCを活性化することが可能です。本研究では、以下のような多段階の検証が行われました。
1. 細胞および動物モデルにおける検証
- アタシグアトは、酸化型sGCを活性化し、cGMPの産生を増加させました。
- 骨形成因子であるBMP2(Bone Morphogenetic Protein)のシグナル伝達を抑制し、オステリックス(Osterix)やRunx2(Runt-related transcription factor 2)などの石灰化促進因子の発現を減少させました。
- FCAVSモデルマウスでは、アタシグアットの投与により弁石灰化の進行が有意に抑制され、弁機能の低下も軽減されました。
2. 臨床試験(Phase I, II)における検証
- 第I相試験(14日間):n=16(アタシグアト8人(平均70歳)、プラセボ8人(平均73歳))
アタシグアットは安全であり、低血圧や起立性低血圧のリスクは認められませんでした。 - 第II相試験(6か月間):
n=23(アタシグアト12人(平均74歳、男性7)、プラセボ11人(平均72歳、男性8)) - 軽度〜中等度AS、弁面積1.0 ~ 2.0 cm 2、左室駆出率> 50%
- アタシグアト投与群では、弁石灰化の進行速度が約70%低下(P=0.051)。
- 弁狭窄の進行抑制が確認され、左室機能の低下も抑制される傾向を示しました(P<0.05)。
- 特に男性患者で治療効果が高い傾向が認められました。
今後の課題と展望
本研究は、FCAVSの薬物療法に新たな可能性を示しましたが、いくつかの課題も残されています。
- 長期的な有効性の検証:本研究は6か月間の試験でしたが、長期的な効果についてはさらなる研究が必要です。
- 大規模試験の実施:対象患者数が限られており、大規模な臨床試験での再現性が求められます。
- 性差の影響:男性のほうが治療効果が高い傾向があり、性別による薬物動態や病態の違いを考慮する必要があります。
- 血圧への影響:一部の患者で軽度の血圧低下が認められたため、特定の患者層では慎重な投与が求められます。
まとめ
本研究は、FCAVSに対する薬物療法の可能性を大きく広げるものであり、sGCの再活性化が疾患の進行を抑制できることを示しました。アタシグアトの臨床応用にはさらなる検証が必要ですが、これまで外科的治療が唯一の選択肢であったFCAVSに対し、新たな治療戦略を提供する可能性があります。今後の研究により、より広範な患者に適用できる治療法へと発展することが期待されます。
参考文献
Zhang B, Enriquez-Sarano M, Schaff HV, et al. Reactivation of Oxidized Soluble Guanylate Cyclase as a Novel Treatment Strategy to Slow Progression of Calcific Aortic Valve Stenosis: Preclinical and Randomized Clinical Trials to Assess Safety and Efficacy. Circulation. 2025;151:00–00. DOI: 10.1161/CIRCULATIONAHA.123.066523
追記:既存のsGC刺激薬にAS進行抑制効果は期待できるのか?
ベルイシグアト(ベリキューボ)やリオシグアト(アデムパス)は、酸化型sGC(soluble guanylate cyclase)ではなく、還元型sGCを刺激するsGC刺激薬に分類されます。
sGC刺激薬とsGC活性化薬の違い
sGCを標的とする薬剤は大きく2種類に分けられます。
1. sGC刺激薬(sGC stimulators)
- 作用機序: 還元型sGC(ヘムを持つsGC)に作用し、一酸化窒素(NO)の存在下でその活性を増強する。
- 代表的な薬剤:
- ベルイシグアト(ベリキューボ):慢性心不全(HFrEF)の治療薬。
- リオシグアト(アデムパス):肺動脈性肺高血圧症(PAH)、慢性血栓塞栓性肺高血圧症(CTEPH)の治療薬。
- 特徴:
- NOがある環境では、sGCの活性を増強することでcGMPの産生を促進。
- しかし、酸化ストレスによってsGCが酸化・ヘムを失うと、刺激効果が低下する。
2. sGC活性化薬(sGC activators)
- 作用機序: 酸化型・ヘムフリー(ヘムを失った)sGCを選択的に活性化する。
- 代表的な薬剤:
- アタシグアト(Ataciguat)(研究段階)
- シンリオグアト(Cinciguat)(研究段階)
- 特徴:
- NO非依存的にsGCを活性化し、酸化ストレスの強い環境下でも機能する。
- 重度の酸化ストレスにさらされた組織(動脈硬化・大動脈弁石灰化など)において有効性が期待される。
sGC刺激薬(ベルイシグアト、リオシグアト)はASの進行抑制に向かない可能性
大動脈弁狭窄症(AS)では、弁組織の酸化ストレスが非常に高く、NOシグナル伝達が破綻していることが知られています。
- AS患者ではsGCが酸化され、ヘムを喪失している可能性が高い
- 酸化ストレスが増加すると、sGCがヘムを失い、還元型sGC刺激薬(ベルイシグアト、リオシグアト)の標的となるsGCが減少します。
- ヘムを持たないsGCは、これらのsGC刺激薬に反応しないため、効果が期待しにくい可能性があります。
- NOの産生が低下している
- sGC刺激薬は、NOが存在する環境下でより効果を発揮しますが、ASではNO産生が低下しているため、sGC刺激薬の作用が十分に発揮されない可能性があります。
- 酸化型sGCに作用する薬(sGC活性化薬)の方が適している可能性
- 酸化型sGCをターゲットとするアタシグアト(Ataciguat)などのsGC活性化薬は、ヘムを持たないsGCを直接活性化できるため、ASのような強い酸化ストレス下の疾患に適している可能性があります。
追記のまとめ
ベルイシグアト(ベリキューボ)やリオシグアト(アデムパス)は還元型sGC刺激薬であり、酸化型sGCを標的としません。
したがって、酸化ストレスが高度なASに対しては、sGC刺激薬よりもsGC活性化薬の方が適している可能性が高いです。
現時点では、ベルイシグアトやリオシグアトがASの進行を抑制するという明確なエビデンスはなく、むしろ酸化型sGCをターゲットとする薬剤(アタシグアトなど)の方がASの病態に適合する可能性があります。