はじめに
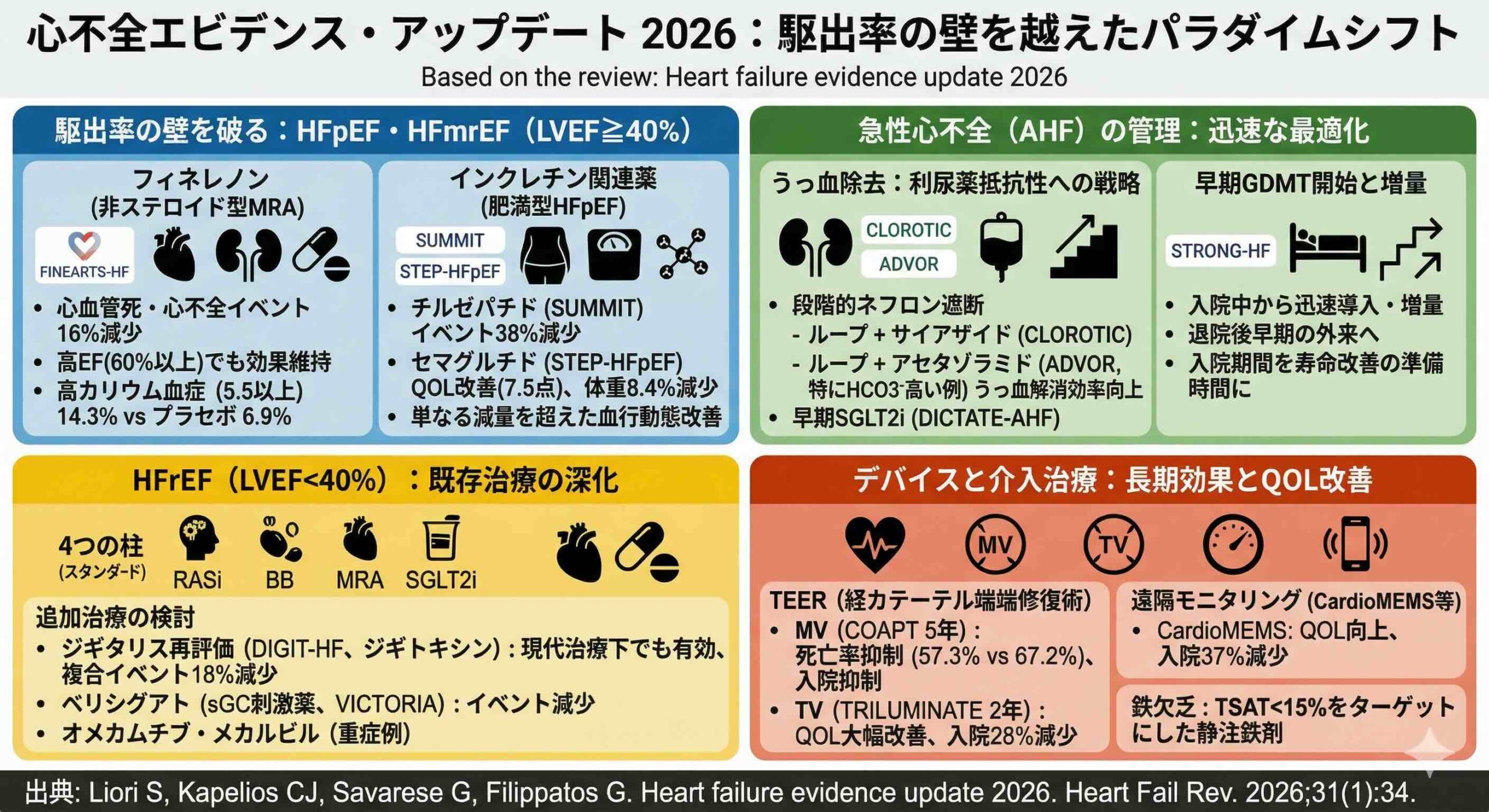
心不全診療は、今、歴史的な転換点に立っています。かつて駆出率が保たれた心不全(HFpEF)や軽度低下した心不全(HFmrEF)は、治療選択肢が乏しく、臨床医にとって苦渋の選択を強いられる領域でした。しかし、2026年現在の最新エビデンスは、この沈黙の領域を希望の光で照らし出しています。本解説では、最新のレビュー論文に基づき、薬物療法からデバイス、さらには急性期管理に至るまで、私たちの臨床を明日から変える知見を解説します。
駆出率の壁を突き破る非ステロイド型MRA
心不全治療の歴史において、ミネラルコルチコイド受容体拮抗薬(MRA)は重要な位置を占めてきましたが、その主戦場はこれまで駆出率が低下した心不全(HFrEF)に限られていました。しかし、FINEARTS-HF試験がもたらしたデータは、その常識を根底から覆しました。
この試験は、LVEF 40%以上の心不全患者6001人を対象に、非ステロイド型選択的MRAであるフィネレノンの効果を検証したものです。結果として、心血管死と心不全増悪イベントの複合プライマリエンドポイントを16%有意に減少させました。特筆すべきは、LVEF 60%以上の患者群においても一貫したベネフィットが確認された点です。これは、従来のステロイド型MRAがこの高EF層で効果を減弱させていたことと比較すると、極めて画期的な新規性と言えます。
分子生物学的な視点で見ると、フィネレノンは心筋の線維化や炎症を抑制するだけでなく、電解質バランスや腎機能への影響を最小限に抑えつつ、ミネラルコルチコイド受容体を強力に遮断します。安全性解析では、カリウム値が5.5 mmol/Lを超える高カリウム血症の頻度は、プラセボ群の6.9%に対しフィネレノン群で14.3%と上昇しましたが、入院を要するような重篤な事例は0.5%と極めて低く抑えられていました。これにより、フィネレノンはSGLT2阻害薬に並ぶ、HFpEF治療の第2の柱としての地位を確立したのです。
インクレチン関連薬;肥満心不全の新たな治療戦略
現代の心不全診療において、肥満は単なるリスク因子ではなく、独立した病態「肥満表現型HFpEF」として認識されています。この病態は、血漿量の拡大、全身性炎症、心外膜脂肪の蓄積、そして心室充満の機械的制限という特徴を持っています。
STEP-HFpEF試験およびSTEP-HFpEF DM試験の統合解析では、GLP-1受容体作動薬であるセマグルチド2.4 mgの効果が示されました。52週時点でのKCCQ臨床サマリースコアは7.5点改善し、体重は8.4%減少しました。さらに注目すべきは、NT-proBNPレベルの有意な低下です。通常、体重減少はナトリウム利尿ペプチド濃度を上昇させますが、セマグルチドによる低下は、単なる減量を超えた血行動態改善効果を示唆しています。
さらに、GIP/GLP-1受容体デュアル作動薬であるチルゼパチドを用いたSUMMIT試験は、さらに強力なインパクトを与えました。肥満を伴うHFpEF患者731人を対象としたこの試験では、心血管死または心不全増悪イベントをプラセボと比較して38%も減少させるという驚異的な結果を叩き出しました。画像下位試験では、チルゼパチドが左室質量や心膜脂肪容積を有意に減少させることも確認されています。これらの薬剤は、単なる減量薬ではなく、心血管リスクを直接的に低減する心不全治療薬へと進化したのです。
急性心不全管理のパラダイムシフト:うっ血除去から早期最適化へ
急性心不全(AHF)の管理目標は、かつての「症状緩和のためのうっ血除去」から「入院中の迅速な薬物療法最適化」へと劇的にシフトしました。この変化の背景には、STRONG-HF試験の追加解析があります。
これまで、ガイドライン推奨薬物療法(GDMT)の導入は、退院後の外来で慎重に行われるのが一般的でした。しかし現在では、入院中からの迅速な導入と増量が、将来のうっ血再発を防ぐ鍵であることが示されています。PUSH-AHF試験では、スポット尿中ナトリウムを指標とした利尿薬調整の有効性が示唆され、DICTATE-AHF試験では入院早期からのダパグリフロジン投与が、腎安全性を保ちつつナトリウム利尿と利尿を有意に促進することが証明されました。
また、利尿薬抵抗性に対する戦略も精緻化されています。CLOROTIC試験では、ループ利尿薬へのヒドロクロロチアジドの上乗せが体重減少を促進することを示し、ADVOR試験ではアセタゾラミド(代表的製品名:ダイアモックス)の併用が、特に代謝性アルカローシスを伴う症例でのうっ血除去効率を高める可能性を示しました。入院期間を「単なる安静と除水の時間」から「生命予後を改善する治療の土台作り」へと変えることが、現在の標準治療となっています。
HFrEF治療の深化:温故知新のジギタリスと新規薬剤の台頭
駆出率が低下した心不全(HFrEF)領域においても、新たな知見が臨床を刺激しています。驚くべきことに、古くから知られるジギタリス製剤が、現代の強力なGDMT下でも有効であることがDIGIT-HF試験によって再確認されました。
この試験では、β遮断薬(95%)、RAS阻害薬(93%)、MRA(76%)、SGLT2阻害薬(19%)といった現代的治療を受けているHFrEF患者1212人を対象に、ジギトキシン0.07 mgの効果を検証しました。結果、全死因死亡または心不全入院の複合エンドポイントを18%有意に減少させました。血中濃度を8から18 ng/mlに維持することで、安全性も確保されています。これは、いわゆる「4つの柱」が確立した現代においても、強心薬としてのジギタリスが高度な治療選択肢の一つであることを示しています。
一方、新規薬剤である可溶性グアニル酸シクラーゼ(sGC)刺激薬のベリシグアトについても、VICTORIA試験とVICTOR試験の統合解析(計11155人)により、心血管死や心不全入院の有意な減少が確認されました。心筋ミオシン活性化薬のオメカムチブ・メカルビルについては、GALACTIC-HF試験で心血管イベントを8%減少させたものの、規制当局の承認に至るほどの臨床的インパクトとはみなされませんでした。しかし、LVEF 28%以下や収縮期血圧 100 mmHg以下の重症例での効果が期待されており、現在COMET-HF試験が進行中です。
デバイス治療の進化と課題:TEERと遠隔モニタリングの現在地
インターベンション治療もまた、大きな進化を遂げています。僧帽弁に対する経カテーテル端端修復術(TEER)は、COAPT試験の5年フォローアップにより、長期的な死亡率の低下(57.3% vs 67.2%)と心不全入院の抑制が確立されました。
この成功は三尖弁閉鎖不全症(TR)治療にも波及しています。TRILUMINATE試験では、TriClipシステムを用いたTEERがQOLを劇的に改善し、2年間の長期解析では心不全入院を28%減少させることが示されました。
また、肺動脈圧センサー(CardioMEMS)を用いた遠隔モニタリングは、MONITOR-HF試験において、NYHA心機能分類3度の患者のQOLを改善し、入院リスクを37%低減させました。
一方で、慎重な解釈が必要なデータも存在します。心房中隔欠損作成デバイス(IAS)を用いたRELIEVE-HF試験では、全体としては中立的な結果でしたが、HFpEFサブグループにおいて死亡や心不全イベントが増加するという害のシグナルが観察されました。これは、HFpEFという病態の複雑さを改めて浮き彫りにしており、全例に対するデバイス治療の導入には時期尚早であることを示唆しています。
鉄欠乏治療の精密化と残された課題
心不全患者における鉄欠乏の重要性は広く認知されていますが、治療のタイミングや対象については、より詳細な検討が進んでいます。IRONMAN試験やAFFIRM-AHF試験では、カルボキシマルトース第二鉄の投与が心不全入院を減少させる傾向を示しました。
しかし、HEART-FID試験では、全般的な臨床的ベネフィットは最小限にとどまりました。この原因の一つとして、参加者の60%がベースラインでTSAT 20%を超えていたことや、厳格な投与制限基準により、追跡期間中に十分な鉄剤が投与されなかった可能性が指摘されています。現在、鉄欠乏の診断基準をより精密化し、単なるフェリチン値だけでなくTSAT 15%未満といった真の鉄欠乏層を特定することの重要性が強調されています。
本研究の限界と未解決の課題
これほど多くのエビデンスが蓄積されているにもかかわらず、実臨床への実装には依然として大きなギャップが存在します。TITRATE-HFレジストリなどのリアルワールドデータによれば、GDMTが目標用量に達していない原因の多くは不耐容ではなく、漫然とした処方の継続、すなわち「臨床的惰性(Clinical Inertia)」によるものです。
また、本レビューの限界として、多くの臨床試験が特定の条件下(厳格な選択除外基準)で行われており、併存疾患の多い高齢者などの多様な集団に対する直接的なエビデンスが必ずしも十分ではない点が挙げられます。特に心房中隔欠損デバイスのように、特定の表現型では害を及ぼす可能性がある介入については、さらなる精密な症例選択基準の構築が不可欠です。
明日からの臨床に活かす実践ガイド
最新のエビデンスを日々の診療に統合するために、明日から以下の行動を実践することを提案します。
- HFpEF患者におけるフィネレノンの検討:LVEF 40%以上の心不全患者に対し、SGLT2阻害薬に加え、フィネレノンの導入を検討してください。LVEF 60%以上の症例であっても、そのベネフィットは期待できます。
- 肥満表現型を見逃さない:BMI 30 kg/m2以上のHFpEF患者には、単なる減量の推奨にとどまらず、チルゼパチドやセマグルチドといったインクレチン関連薬の導入を、心血管イベント抑制の観点から検討してください。
- 急性期管理の「スピード感」の変更:入院直後の急性期から、積極的なうっ血除去と並行してSGLT2阻害薬や他のGDMTの導入・増量を開始してください。退院後の外来まで待つ必要はありません。
- 鉄欠乏の精密な評価:すべての心不全患者において定期的に鉄代謝(フェリチン、TSAT)を測定し、特にTSATが15%を下回る症例には積極的な静注鉄剤投与を検討してください。
心不全治療は、かつての対症療法から、予後を劇的に改善する「精密医療」へと進化しました。2026年の最新知見を武器に、患者一人ひとりの表現型に合わせた最適な治療を届けていきましょう。
参考文献
Liori S, Kapelios CJ, Savarese G, Filippatos G. Heart failure evidence update 2026. Heart Fail Rev. 2026;31(1):34. doi: 10.1007/s10741-026-10609-3.