はじめに
心血管疾患の予防において、LDLコレステロール(LDL-C)の管理は、今や「低ければ低いほど良い(The lower, the better)」という段階から「早ければ早いほど良い(The earlier, the better)」、そして「長く維持するほど良い(The longer, the better)」というフェーズへと進化しています。しかし、強力なスタチンとエゼチミブを併用してもなお、目標値に届かない「ラストワンマイル」の壁に突き当たる症例は少なくありません。2024年にJournal of Cardiovascular Development and Diseaseに掲載された研究は、この停滞した状況を打破するための極めて明快な解答を提示しています。
研究プロトコールの概要(PICO)
対象(P):高強度のスタチンおよびエゼチミブによる治療を3ヶ月以上継続しているにもかかわらず、LDL-C値が70 mg/dLを超えている高リスク心血管疾患患者120名。
介入(I):既存の治療にベムペド酸(Bempedoic Acid)180 mg/日を追加投与する(BA群:60名)。
比較(C):既存のスタチン用量を2倍に増量(タイトレーション)する(ST群:60名)。
結果(O):12週間後のLDL-C値のベースラインからの変化率、および目標値(70 mg/dL未満)の達成率。
分子生物学的視点:スタチンとは異なる機序のシナジー
本研究で主役を演じるベムペド酸(Bempedoic Acid)は、肝臓におけるコレステロール生合成経路において、スタチンが阻害するHMG-CoA還元酵素よりもさらに上流に位置する「ATPクエン酸リアーゼ(ATP citrate lyase;ACL)」を選択的に阻害します。この分子生物学的なターゲットの違いが、スタチンとの併用において重要な意味を持ちます。
ベムペド酸によってACLが阻害されると、アセチルCoAの供給が減少し、結果として肝細胞内のコレステロールが枯渇します。これに反応してLDL受容体の発現がアップレギュレートされ、血中のLDL粒子がより効率的に回収されるようになります。重要なのは、ベムペド酸が「プロドラッグ」として肝臓で特異的に活性化される点です。骨格筋にはこの活性化に必要な酵素(極長鎖アシルCoA合成酵素1(Very long-chain acyl-CoA synthetase 1 / ACSVL1))が存在しないため、スタチンで問題となる筋肉痛などの副作用を回避しつつ、肝臓でのコレステロール合成を強力に抑制できるのです。
スタチン増量の限界と「6%のルール」
臨床医が直面する大きな課題の一つに、スタチンの増量効果の限定性があります。一般に、スタチンの用量を2倍に増やしても、LDL-Cの追加低下率はわずか6%程度に留まるとされており、これは「6%のルール」として知られています。本研究の結果は、まさにこの古典的なルールを再確認させると同時に、戦略的な方向転換を促すものでした。
スタチンの増量は、用量依存的に副作用のリスクを高める一方で、脂質低下効果は対数関数的に鈍化します。それに対し、異なる経路を遮断するベムペド酸を追加することは、生物学的なバイパスを塞ぐ戦略として極めて合理的です。
臨床データが示す圧倒的な格差
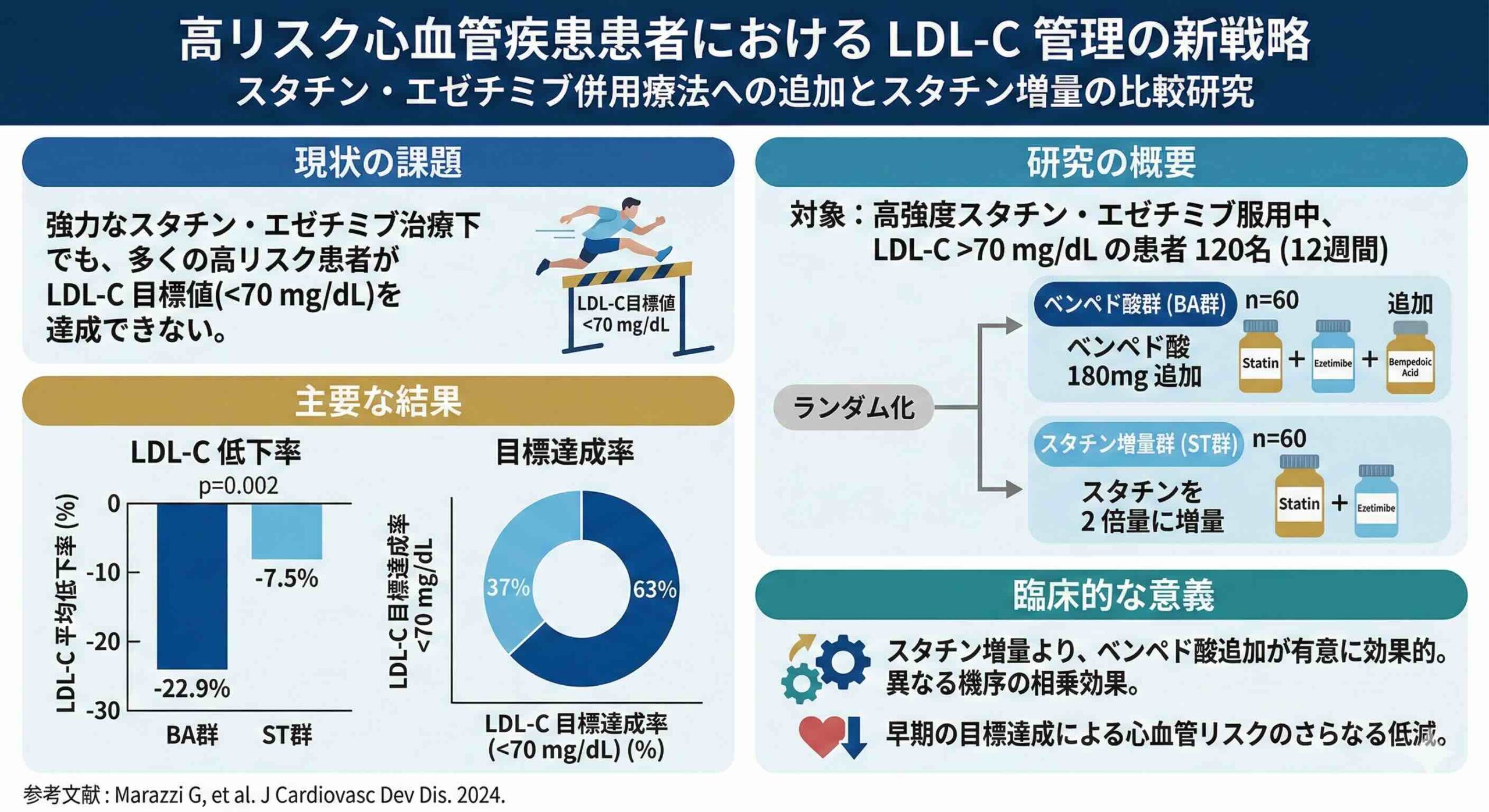
本研究の結果は、BA群(ベムペド酸追加)の優位性を鮮烈に描き出しました。12週間後、LDL-Cの変化率はBA群で22.9%の低下を示したのに対し、ST群(スタチン増量)ではわずか7.5%の低下に留まりました。統計的有意差(p=0.002)は明白であり、介入群と対照群の間の差は13.8 mg/dLに達しました。
さらに注目すべきは、目標達成率です。欧州のエビデンスに基づき、高リスク患者の目標値とされる70 mg/dL未満に到達した割合は、BA群で63%(38名)であったのに対し、ST群では37%(22名)でした。この約1.7倍という達成率の差は、日常診療における薬剤選択がいかに予後を左右するかを物語っています。
脂質プロファイル全体を見ても、総コレステロールはBA群で14.8%減少(ST群は4.7%)、非HDLコレステロールもBA群で25.1%減少(ST群は8.3%)と、ベムペド酸による「トリプル・セラピー(スタチン+エゼチミブ+ベムペド酸)」の強力なベネフィットが示されました。
副作用の懸念に対する回答
新規薬剤の導入に際して懸念される安全性についても、本研究は心強いデータを提供しています。尿酸値の上昇や血糖値の変動、クレアチンキナーゼの上昇といった有害事象について、BA群とST群の間に有意な差は認められませんでした。特に、スタチン増量によって懸念される耐糖能への影響や筋症状の増加を避けつつ、これほどの脂質改善を得られたことは、長期的なアドヒアランスの観点からも重要です。
本研究の新規性と学術的価値
これまでの研究の多くは、スタチン不耐容の患者に対するベムペド酸の効果や、スタチン単剤への上乗せ効果を検証したものでした。本研究の新規性は、すでに「スタチン+エゼチミブ」という標準的な併用療法を受けている高リスク患者を対象とし、臨床現場で最も一般的な判断である「スタチンの増量」と直接比較した点にあります。
この比較により、スタチン増量という「垂直的な強化」よりも、ベムペド酸追加という「水平的な多剤併用」の方が、高リスク患者の目標達成において遥かに効率的であることが科学的に証明されました。
明日からの臨床実践への応用
この論文から得られる知見を明日の診療に活かすためのポイントは、以下の3点に集約されます。
第一に、スタチンとエゼチミブの併用下でLDL-Cが目標値に届かない場合、安易にスタチンを増量するのではなく、早期にベムペド酸の追加を検討すべきです。20%以上の追加低下が期待できるため、現在80 mg/dL前後の症例であれば、高確率で70 mg/dL未満へとガイドできます。
第二に、アトルバスタチンとロスバスタチンのどちらを使用していても、ベムペド酸の効果は同等に発揮されるという点です。ベースの薬剤の種類にこだわらず、柔軟にトリプル・セラピーへ移行する判断が求められます。
第三に、副作用プロファイルの良さを活用することです。特に高齢者や糖尿病合併例など、高用量スタチンによる副作用が懸念される症例において、ベンペド酸は極めて使い勝手の良い選択肢となります。
研究の限界(Limitation)
本研究の成果を解釈するにあたっては、いくつかの制約を考慮する必要があります。まず、単一施設での実施であり、症例数が120名と比較的少数であることです。また、観察期間が12週間と短いため、長期的な心血管イベントの抑制効果や、数年単位での安全性については本研究のみでは断定できません。さらに、オープンラベル試験であるため、バイアスの混入を完全に排除できない点や、プラセボ群が設定されていない点も限界として挙げられます。若年層(50歳未満)の症例が少なかったため、若い世代への一般化には慎重な判断が必要です。
まとめ
脂質管理の歴史は、強力なスタチンの登場によって大きく塗り替えられましたが、現代の医療が求める厳格な目標値の前では、スタチン単剤の限界も浮き彫りになっています。本研究が示した「トリプル・セラピー」の有効性は、高リスク患者を守るための強力な武器となります。スタチンの増量という従来のルーチンを脱却し、分子生物学的な相乗効果を狙った多角的アプローチこそが、心血管疾患予防の新たなスタンダードとなるでしょう。
参考文献
Marazzi, G.; Caminiti, G.; Perrone, M.A.; Campolongo, G.; Cacciotti, L.; Giamundo, D.M.; Iellamo, F.; Severino, P.; Volterrani, M.; Rosano, G. Addition of Bempedoic Acid to Statin-Ezetimibe versus Statin Titration in Patients with High Cardiovascular Risk: A Single-Centre Prospective Study. J. Cardiovasc. Dev. Dis. 2024, 11, 286. https://doi.org/10.3390/jcdd11090286