はじめに
抗生物質の開発は、人類の平均寿命を飛躍的に延ばした20世紀最大の功績の一つです。しかし、その恩恵の裏で、私たちの体内に共生する広大な生態系である腸内細菌叢(マイクロバイオーム)がどのような代償を払っているのか、その全貌は未だ霧の中にありました。2026年にネイチャー・メディシン誌に掲載されたこの大規模研究は、スウェーデンの14,979人という驚異的な規模のデータを用い、私たちが数年前に服用した一剤の抗生物質が、今この瞬間の腸内環境、さらには将来の健康リスクにまで影を落としている可能性を突き止めました。
研究プロトコールの概要とデザイン
本研究の基盤を理解するために、まずはその設計を確認しておきましょう。
P(対象):スウェーデンの3つの大規模コホート(SCAPIS、SIMPLER、MOS)に参加した成人14,979人。
E(暴露):過去8年間に処方・調剤された経口抗生物質。スウェーデン国家処方薬レジストリ(NPDR)の客観的データに基づきます。
なお、抗生物質の長期服用(例えば、ニキビ・酒さの治療でテトラサイクリン12週間など)のケースは除外しています。
C(比較):抗生物質を使用していない、あるいは異なる期間・種類の抗生物質を使用した群。
O(アウトカム):糞便のディープ・ショットガン・メタゲノム解析による細菌種レベルの多様性と存在量、および心代謝疾患に関連する臨床指標。
研究デザイン:処方レジストリと糞便メタゲノムデータを統合した、大規模な横断的観察研究。
既存研究を超越する圧倒的な新規性
これまでの研究でも、抗生物質が腸内細菌叢に短期的かつ劇的な変化をもたらすことは知られていました。しかし、その多くは数十人程度の小規模な介入研究であり、数ヶ月程度の追跡に留まっていました。
本研究がもたらしたパラダイムシフトは、主に3つの点に集約されます。
第一に、自己申告による曖昧な記憶ではなく、公的な処方記録という確実な証拠に基づき、過去8年という極めて長いスパンを解析した点です。
第二に、1万5000人近いサンプルサイズにより、抗生物質の種類ごとの影響を種レベルで微細に分析することを可能にしました。
そして第三に、たとえ「4年から8年前のたった1回の服用」であっても、その痕跡が現代の腸内に刻まれていることを統計的に証明した点にあります。
腸内多様性の減衰と長期的な回復の遅れ
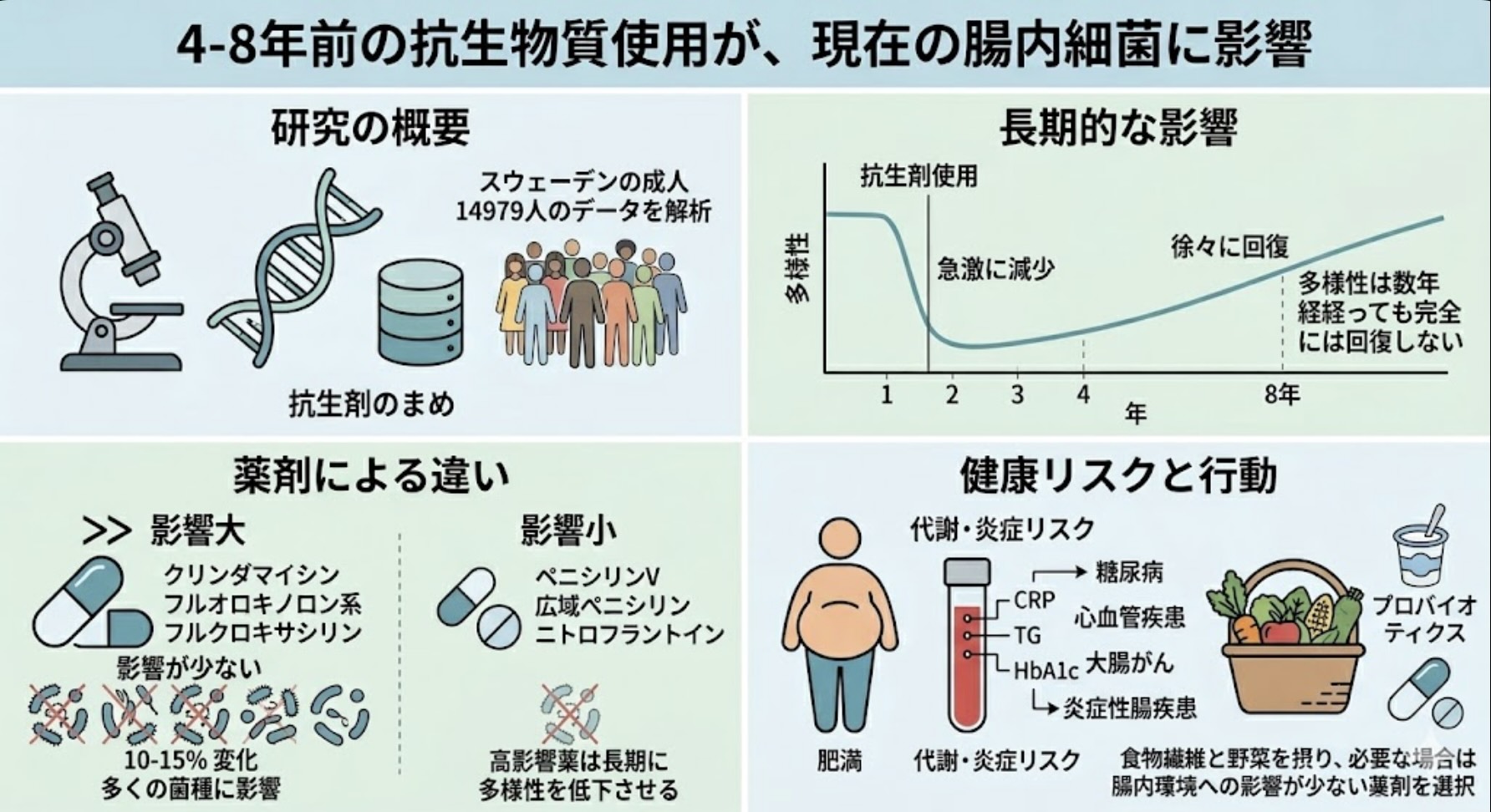
研究グループは、抗生物質の使用と菌種の多様性(アルファ多様性)の関連を、服用からの期間ごとに詳細にモデル化しました。その結果、使用から1年未満での多様性の低下が最も顕著であることは予想通りでしたが、驚くべきはその後です。
服用から1年以上4年未満、さらには4年以上8年前に服用した群においても、抗生物質を使用していない群と比較して、菌種の豊かさ(Richness)が有意に低い状態が維持されていました。特に、多様性の指標の一つであるシャノン指数や逆シンプソン指数においても同様の傾向が確認されました。
特筆すべき数値として、クリンダマイシンを1年以内に服用したケースでは、検出される菌種が平均して47種も減少していました。フルオロキノロン系やフルクロキサシリンでも、それぞれ20種から21種の減少が認められています。機能的回帰モデルによる解析では、服用後の最初の2年間は急速な回復を見せるものの、それ以降の回復曲線は極めて平坦になり、完全な元通りの状態に戻るには想像以上の年月を要することが示唆されました。
参考
・クリンダマイシン内服薬:ダラシンカプセルなど
・フルオロキノロン系
レボフロキサシン(商品名:クラビットなど)
モキシフロキサシン(商品名:アベロックス)
シプロフロキサシン(商品名:シプロキサン)
トスフロキサシン(商品名:オゼックス)
ラスクフロキサシン(商品名:ラスビック) など
・フルクロキサシリン:日本には内服薬なし
3つの「最恐」薬剤:クリンダマイシン、フルオロキノロン、フルクロキサシリン
本研究では、抗生物質を11のクラスに分類して解析を行いましたが、腸内細菌叢へのインパクトは薬剤によって劇的に異なりました。特に広範かつ長期的な影響を及ぼしていたのが、クリンダマイシン、フルオロキノロン系、フルクロキサシリンの3種類です。
これらの薬剤を4年から8年前に服用していた場合、解析対象となった1,340種の細菌のうち、実に10%から15%もの菌種で存在量が変化していました。一方で、スウェーデンで最も一般的に処方されるペニシリンV(フェノキシメチルペニシリン)や、広域ペニシリン、尿路感染症に用いられるニトロフラントインなどは、長期的な菌種組成への影響が極めて限定的であることが判明しました。
分子生物学的、分類学的な視点で見ると、薬剤の作用機序と影響を受ける菌群には明確な関連があります。狭域ながらベータラクタマーゼ耐性を持つフルクロキサシリンは、主にグラム陽性菌であるBacillota A門(旧厚壁菌門)、特にLachnospirales目やOscillospirales目の存在量を大きく変動させました。対照的に、広域スペクトルを持つクリンダマイシンやフルオロキノロン系は、Bacteroidota門やActinomycetota門を含む、より多様な系統の細菌に壊滅的な影響を与えていました。
代謝疾患へのリンク:腸内に潜む病理の兆し
抗生物質が菌叢を変えるだけなら、それは単なる「生態学的変化」に過ぎません。しかし本研究は、この変化が宿主である私たちの代謝健康に直結している可能性を提示しました。
抗生物質使用、特に影響の大きい3剤の使用に関連して増加していた菌種には、Enterocloster bolteae、E. citroniae、Flavonifractor plautii、Ruminococcus B gnavus、Eggerthella lentaなどが含まれていました。これらの菌種は、SCAPISコホートのデータを用いた解析により、BMI(肥満指数)の増加、ウエストヒップ比(WHR)の悪化、血清中性脂肪(TG)の上昇、および炎症マーカーであるC反応性蛋白(CRP)の上昇と相関していることが明らかになりました。
・Enterocloster bolteae:エンテロクロスター・ボルテアエ
・Enterocloster citroniae:エンテロクロスター・シトロニアエ
・Flavonifractor plautii:フラボニフラクター・プラウティ
・Ruminococcus B gnavus:ルミノコッカス・グナバス
・Eggerthella lenta:エガセラ・レンタ
逆に、抗生物質使用によって減少したAlistipes communisやOdoribacter splanchnicusなどは、より健康的な心代謝プロファイルと関連していました。
・Alistipes communis:アリスティペス・コムニス
・Odoribacter splanchnicus:オドリバクター・スプランクニクス
さらに、炎症性腸疾患(IBD)の患者で減少していることが知られる菌種が、抗生物質使用後にも同様に減少しているというパターンも観察されました。
これは、過去の抗生物質使用が腸内細菌叢というフィルターを通じ、数年後の糖尿病や心血管疾患、炎症性疾患の発症リスクを「下地」として形成している可能性を強く示唆しています。
科学的妥当性を担保する厳格な検証
本研究の結果が、単なる「健康意識の差」や「もともとの病弱さ」によるバイアスではないことを証明するため、研究チームは非常に巧妙な感度分析を行っています。
その一つが「ネガティブ・コントロール」としての、糞便採取「後」の抗生物質使用の解析です。もし、もともと感染症にかかりやすい不健康な人の菌叢が乱れているだけなら、採取後に抗生物質を飲む予定の人でも菌叢に異常が見られるはずです。しかし、採取後の服用と採取時の菌叢には一切の関連が認められませんでした。これにより、観察された変化は「以前に飲んだ薬剤そのもの」による影響である可能性が極めて高まったのです。また、入院歴のある参加者を除外した解析でも結果は不変であり、重症感染症自体の影響よりも、外来で処方される抗生物質そのもののインパクトが強調される結果となりました。
限界点(Limitation)
どれほど優れた研究にも限界は存在します。本研究においても、以下の点に注意が必要です。
まず、観察研究である以上、厳密な意味での因果関係を100%断定することはできません。また、スウェーデン国外での調剤や入院中の投与はレジストリに含まれていないため、抗生物質への暴露量は過小評価されている可能性があります。さらに、本研究は細菌の「相対的な割合」を測定するメタゲノム解析を用いており、腸内細菌の「絶対数」がどのように変化したかについては言及していません。加えて、スウェーデンは世界的に見ても抗生物質の使用が非常に慎重で、薬剤耐性率が低い国です。この結果を、抗生物質がより頻繁に使用される日本などの他の地域にそのまま当てはめる際には、地域の処方慣習や耐性菌の分布を考慮する必要があります。
私たちが明日から実践できること
この論文が私たちに突きつけているのは、抗生物質という「諸刃の剣」を扱う際の新しい倫理観です。専門家のみならず、知識ある市民として明日から活かせる教訓をまとめます。
- 慎重な薬剤選択の議論
もしあなたが医師から抗生物質を処方される場面に遭遇したら、その薬剤がどうしても必要か、そして可能であれば腸内環境への影響が少ない選択肢(ペニシリンVなど)がないかを相談する権利があります。もちろん、必要な治療を拒むべきではありませんが、安易な広域抗生物質の使用を避ける意識が重要です。 - 「1回だけ」の重みを再認識する
たとえ数日間の1コースであっても、その影響は8年後まで続く可能性があります。風邪(ウイルス感染症)に対して、念のためにと抗生物質を希望するような行為が、自分の腸内に数年単位の「空白地帯」を作るリスクであることを理解すべきです。 - 長期的な腸内ケアの視点
過去に抗生物質を多用した経験がある場合、自分の代謝リスクや炎症リスクが、通常よりも菌叢の影響を受けている可能性を考慮に入れてください。特定の菌種の消失は不可逆的かもしれませんが、食事やライフスタイルを通じて、残された菌叢の機能を最大限に引き出す努力は無駄にはなりません。 - 医療者への情報提供
過去の病歴を伝える際、単に「どんな病気をしたか」だけでなく、「過去数年間にどの程度の頻度で抗生物質を服用したか」という情報は、将来の心代謝疾患リスクを評価する上での重要な指標になり得ます。
抗生物質は、感染症の脅威から私たちを守る盾です。しかし、その盾を振り回すことで、自分自身の内なる庭を荒らしてしまわないよう、私たちはより賢明な使い手にならなければなりません。
参考文献
Baldanzi, G., Larsson, A., Sayols-Baixeras, S., Dekkers, K. F., Hammar, U., Nguyen, D., Graells, T., Ahmad, S., Volpiano, C. G., Meric, G., Järhult, J. D., Tängdén, T., Ludvigsson, J. F., Lind, L., Sundström, J., Michaëlsson, K., Ärnlöv, J., Kennedy, B., Orho-Melander, M., & Fall, T. (2026). Antibiotic use and gut microbiome composition links from individual-level prescription data of 14,979 individuals. Nature Medicine, 32, 1351-1361. https://doi.org/10.1038/s41591-026-04284-y