高血圧治療における神経解剖学的障壁と新たな希望
現代の循環器内科において、薬剤抵抗性高血圧への挑戦は終わることのないテーマです。カテーテルによる腎デナベーション(renal denervation;RDN)は、低侵襲な自律神経変容療法として大きな期待を集めてきましたが、過去の臨床試験ではその降圧効果が限定的であったり、症例によるばらつきが大きかったりと、必ずしもすべての患者に劇的な恩恵をもたらすわけではありませんでした。その最大の障壁として立ちはだかるのが、腎神経の複雑な解剖学的分布です。
これまでのRDNは、主に腎動脈の周囲を走る末梢神経線維をターゲットにしてきました。しかし、最新の解剖学的知見によると、腎神経の多くは主腎動脈をバイパスして腎臓へ到達する「遅延流入神経」や「超遅延流入神経」として存在し、その割合は63.3%にも達すると報告されています。また、副腎動脈の存在や血管の蛇行、焼灼深度の不足などが、完全な除神経を阻んできました。こうした背景の中、Long氏らによる本論文は、神経線維という「枝」ではなく、神経節という「根」を叩くという、パラダイムシフトを提案しています。その標的こそが、大動脈腎神経節(aorticorenal ganglion;ARG)です。
大動脈腎神経節(ARG)という上流へのアプローチ
ARGは、腹部大動脈と腎動脈の分岐部に位置する前椎体神経節であり、腎臓へ向かう交感神経のいわばゲートウェイとしての役割を担っています。ここには、中枢からの節前線維が節後線維へとリレーされる神経細胞体が高密度に集まっており、ARGを破壊することは、末梢の個々の神経線維を一つずつ焼くよりもはるかに効率的で広範囲な交感神経遮断を可能にします。
本研究において特筆すべきは、その確実な同定手法です。臨床現場では、高周波刺激(
high-frequency stimulation:HFS)を用いて、血圧が5 mmHg以上上昇する部位をARGとして特定しています。これは、解剖学的な位置関係だけに頼らず、機能的に血圧調節に関与している神経組織をリアルタイムで確認しながら処置を行うという、非常に合理的かつ生理学的なアプローチです。この精密なターゲティングが、後の劇的な臨床成績の裏付けとなっています。
研究プロトコール概要およびデザイン
単一の臨床研究におけるプロトコール概要(PICO)は以下の通りです。
P(対象):24時間自由行動下血圧測定(ABPM)で収縮期血圧が130 mmHg以上、または日中平均が135 mmHg以上で、少なくとも1剤以上の降圧薬を服用しているコントロール不良の本態性高血圧患者41名。
I(介入):従来の高周波刺激(HFS)ガイド下腎デナベーション(RDN)に加え、大動脈腎神経節(ARG)領域への追加焼灼を行う群(RDN+ARG群)。
C(比較):従来のHFSガイド下RDNのみを施行する群(RDN群)。
O(アウトカム):術後3ヶ月時点における24時間平均収縮期血圧のベースラインからの変化量。
研究デザイン:多施設共同、プロスペクティブ、非ランダム化探索的臨床試験。
結果:圧倒的な降圧データ
実際の臨床成績は、専門家の目から見ても驚くべきものでした。
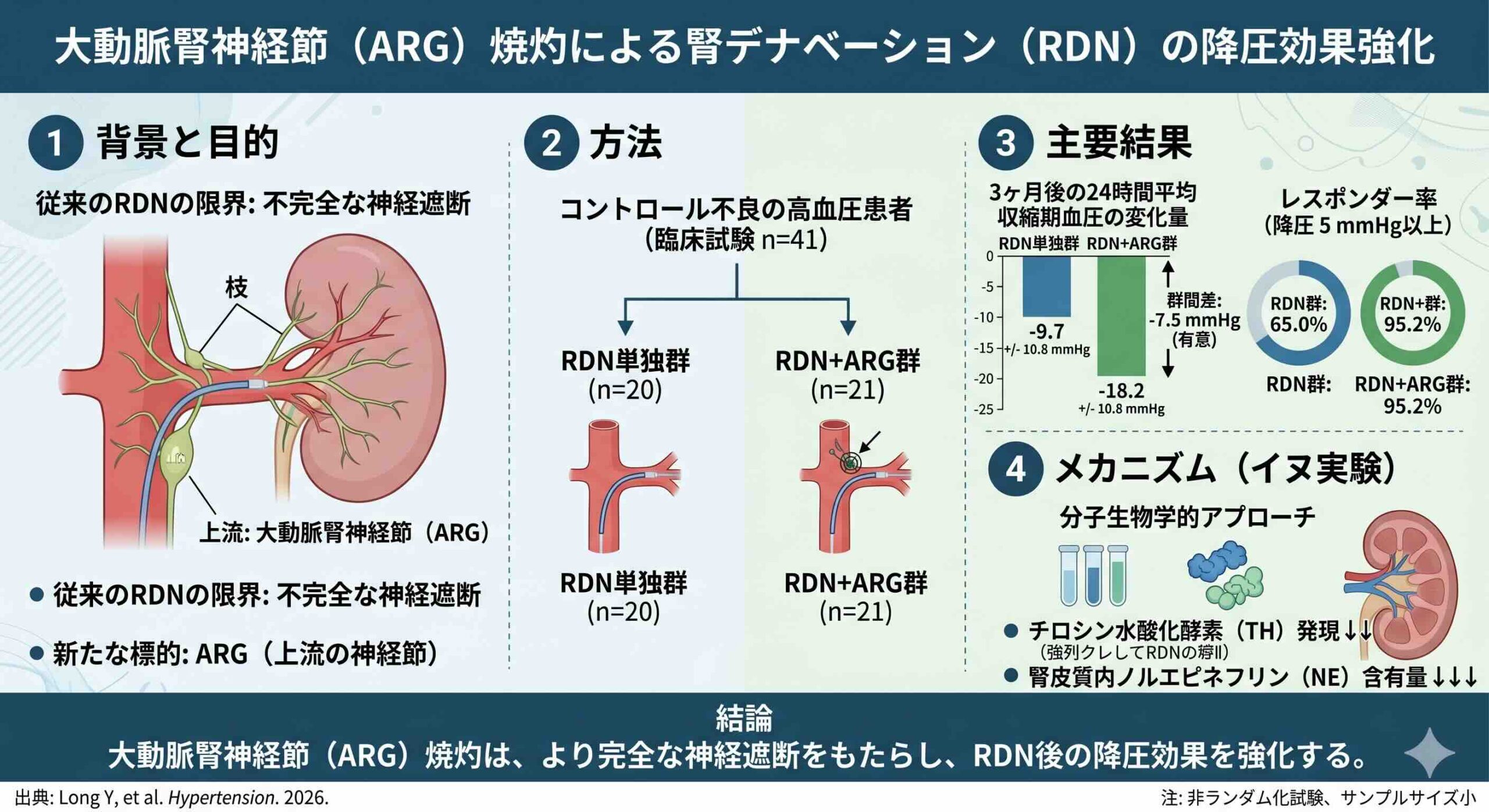
術後3ヶ月の24時間平均収縮期血圧の変化量において、従来のRDN群が-9.7 ±10.8 mmHgであったのに対し、追加のARG焼灼を行ったRDN+ARG群では-18.2±10.8 mmHgという、約2倍に近い降圧を達成しました。ベースラインの血圧で調整した群間差は-7.5 mmHg(95%信頼区間 -13.9〜-1.2、P = 0.021)であり、明確な優越性が示されています。
さらに、治療への反応性を示すレスポンダー率(24時間収縮期血圧が5 mmHg以上低下した割合)においても、RDN群の65.0%に対し、RDN+ARG群では95.2%という極めて高い数値を記録しました。これは、ARGへの介入が、従来のRDNで見られた「効果の不確実性」を克服し、より多くの患者において確実に血圧を下げる手段になり得ることを示唆しています。安全性に関しても、手技に関連した重大な合併症は認められず、推算糸球体濾過量(eGFR)の低下も確認されませんでした。
分子生物学的視点から見た神経節焼灼の優位性
本研究の価値をさらに高めているのが、イヌを用いた動物実験による分子メカニズムの検証です。研究チームは、焼灼後の腎臓および血中における神経伝達物質やマーカーの変動を詳細に追跡しました。
まず、交感神経の活性を示す重要な酵素であるチロシン水酸化酵素(TH)の動態です。ウェスタンブロット法による解析の結果、腎皮質におけるTHのタンパク発現量は、対照群を1.0とした場合、RDN群では0.72 ±0.15まで低下しましたが、ARG焼灼群では0.36 ± 0.10という極めて低いレベルまで抑制されていました。免疫組織化学染色においても、RDN群では神経遮断に空間的なばらつきが認められたのに対し、ARG焼灼群では腎門部における交感神経末端がほぼ完全に消失していることが視覚的にも確認されました。
さらに、交感神経活動の直接的な指標であるノルエピネフリン(NE)とニューロペプチドY(NPY)の濃度変化も見逃せません。腎皮質内のNE含有量は、ARG焼灼群で874.6± 76.2 ng/gとなり、RDN群の1004.0 ±75.9 ng/gを有意に下回りました。血中においても同様の傾向が確認され、ARG焼灼群では全身的な交感神経トーンがより強力に抑制されていることが証明されました。また、免疫蛍光染色によってARG内に高密度の知覚性求心性線維(感作線維)が存在することも明らかになり、ARG刺激による急激な血圧上昇がこれら求心性回路のキャプチャを反映している可能性が示唆されました。この求心性経路の遮断が、中枢からの交感神経出力を減弱させ、全身的な降圧効果をもたらしていると考えられます。
神経調節療法のパラダイムシフト:線維から神経節へ
これまでのRDNの歴史は、いかに効率よく腎動脈周囲を焼くかという「デリバリー」の工夫の歴史でもありました。螺旋状の多電極カテーテルや超音波デバイスの導入はその最たる例です。しかし、本研究が示したのは、デバイスの形状を工夫する以前に、ターゲットそのものをより上流の神経節へとシフトさせることの重要性です。
ARGをターゲットにすることで、解剖学的な多様性、すなわち副腎動脈や迷走する神経線維といった、従来のRDNが抱えていた技術的な「死角」を回避できる可能性が高まります。また、ARG焼灼は、腎臓への直接的な影響だけでなく、全身の交感神経活動を効率よくリセットするためのスイッチとしての役割を果たしていると言えます。これは、単なる局所治療の域を超え、高血圧という全身性の自律神経疾患に対する根源的な介入としての性格を帯びています。
本研究の限界と慎重な解釈
非常に魅力的なデータが示された一方で、臨床応用に向けて解決すべき課題も残されています。本研究の最大の限界(リミテーション)は、臨床試験におけるARGの同定成功率が約50%に留まっている点です。大動脈側からのアプローチでは、血管壁の厚さや神経節との距離により、HFSによる反応が得られない症例が存在しました。動物実験では静脈側(下大静脈や腎静脈)からのアプローチによって成功率を高めていますが、ヒトにおける静脈アプローチの安全性はまだ確立されていません。
また、非ランダム化比較試験であること、サンプルサイズが41名と小規模であること、そして3ヶ月という短期間のフォローアップであることも考慮する必要があります。ARGは上腸間膜動脈神経節(SMG)とも近接しており、誤って他の臓器を支配する神経節を焼灼した場合の長期的副作用、例えば消化管運動や代謝への影響については、より大規模な臨床試験での検証が待たれます。
明日の臨床と研究に活かすための実践的考察
この論文から得られる知見は、明日の医療においてどのように活かせるのでしょうか。まず第一に、RDNを検討する際や、術後の血圧低下が不十分な症例に接した際、「なぜ効かなかったのか」を考える視点が変わります。それは手技のミスではなく、解剖学的な上流に原因がある可能性を常に考慮すべきであるということです。
具体的には、将来的にARG焼灼が標準化された場合、解剖学的に複雑な腎動脈を持つ患者や、従来のRDNで反応が乏しかった患者に対する救済措置、あるいは初回からのより強力な介入手段としての選択肢が生まれます。また、臨床医としては、HFSを用いた機能的な神経マッピングの重要性を再認識すべきです。単に解剖学的な目安で焼くのではなく、電気刺激に対する反応を指標にする「生理学的ガイド」の手法は、他の不整脈治療と同様に、高血圧治療においても精度の向上に直結します。
さらに、ARGが単なる腎神経の中継点ではなく、全身の交感神経トーンを制御する拠点であるという事実は、高血圧以外の疾患、例えば心不全や心房細動、閉塞性睡眠時無呼吸症候群といった、交感神経過緊張が関与する多種多様な病態への応用可能性を示唆しています。私たちは今、カテーテルによる自律神経調節が、単なる降圧治療から「全身の交感神経リセット療法」へと進化する瞬間に立ち会っているのかもしれません。この知見を胸に、個々の症例の背景にある複雑な神経回路を想像し、より最適な治療戦略を練る姿勢こそが、明日からの診療をより高みへと引き上げるはずです。
参考文献
Long Y, Lai Y, Ren Y, Ma X, Li D, Chen L, Liao X, Xia T, Liu Z, Ling Z, Chen Y, Zhou H, Yin Y. Aorticorenal Ganglion Ablation Enhances Blood Pressure Reduction After Renal Denervation. Hypertension. 2026;83:e26719. doi: 10.1161/HYPERTENSIONAHA.125.26719.