はじめに
現代医療において、ウェアラブルデバイスは単なる歩数計の枠を超え、個人の生理学的深淵を覗き見るための窓へと進化を遂げています。今回ご紹介するのは、npj Digital Medicineに掲載された、皮膚温度の動的な変化から心血管系の潜在的な欠損をあぶり出す画期的な研究です。私たちは眠っている間、意識することなく微細な動きを繰り返していますが、その一瞬の動きが心血管系に対する天然のストレステストとして機能しているという事実は、驚きを持って迎えられるべきでしょう。
研究プロトコールの概要
本研究の骨組みを簡潔に整理します。
研究デザイン:ウェアラブルデバイス(Oura Ring Gen2(第2世代モデル))から得られた縦断的データとアンケート回答を用いた、観察的横断コホート研究。
対象(P):TemPredict研究に参加した成人(解析対象者は数万名規模、最終的な条件合致者は約1.5万人以上)。
曝露(E/I):心房細動(AF)、高血圧(H)、糖尿病(D)、冠動脈疾患(CAD)などの自己申告による心血管系疾患の既往。
比較(C):上記疾患の既往がない「健康な」コントロール群。
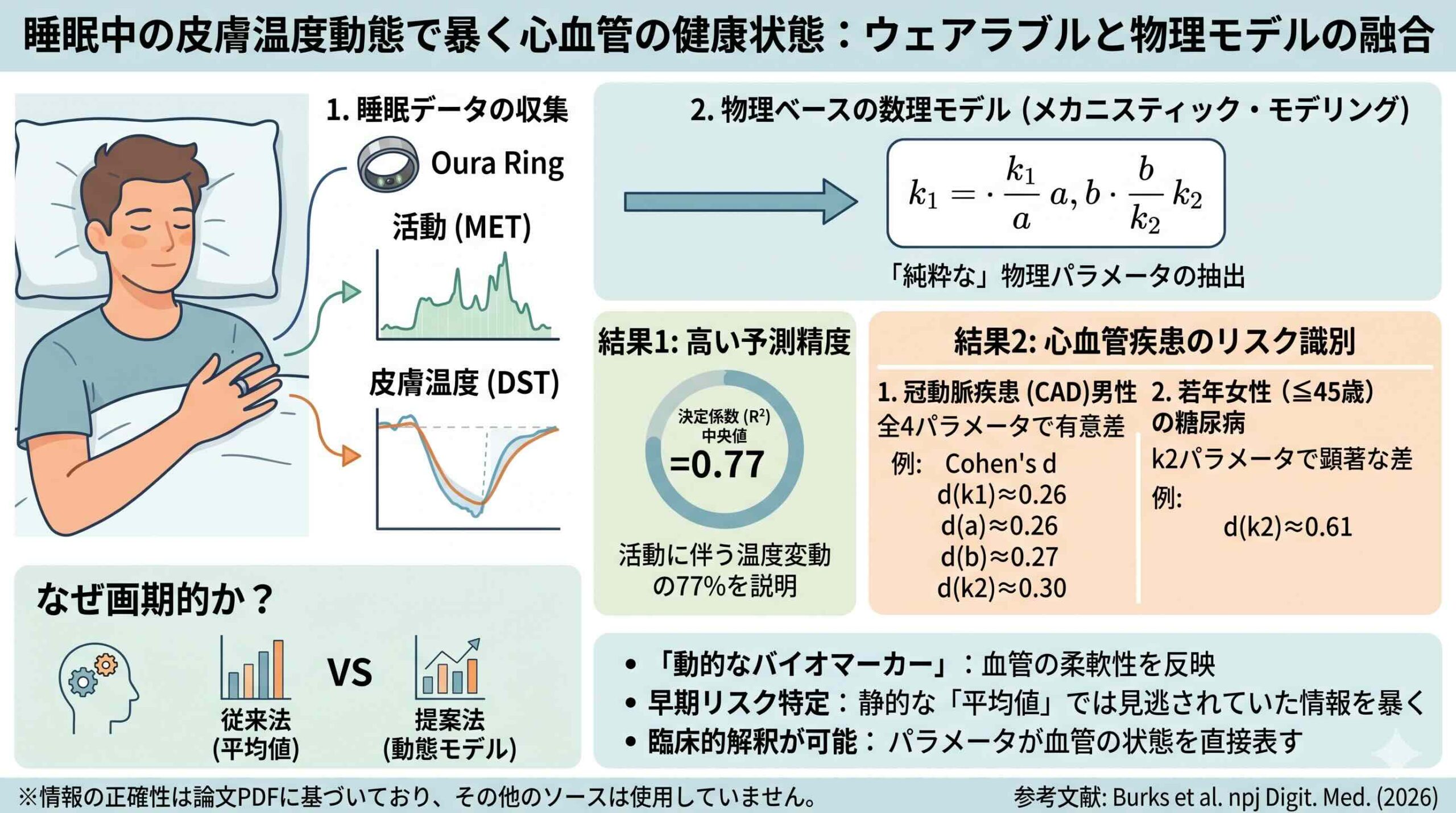
アウトカム(O):睡眠中の微細活動に伴う末梢皮膚温度の応答動態を記述する物理モデルのパラメータ(k1, a, b, k2)。
統計学的平均という霧を晴らす、ダイナミクスの力
従来の皮膚温度解析における最大の障壁は、データの解釈を曇らせるノイズにありました。皮膚温度は外気温、ホルモンバランス、食事、活動量といった無数の要因に左右されます。これまでの研究の多くは、特定の期間における平均温度を比較するという手法に頼ってきましたが、これでは個人間の生理学的な差異を捉えるにはあまりに解像度が低すぎました。
本研究の白眉は、皮膚温度を静的な数値としてではなく、時間とともに変化する動的なシステムとして捉え直した点にあります。研究チームは、睡眠中という外部環境の変動が最小限に抑えられる時間帯に注目しました。そこで発生する「寝返り」のような微細な活動(MET:代謝当量)が、皮膚温度をどのように揺さぶり、そしてどのように回復していくのか。その軌跡(トラジェクトリ)にこそ、心血管系の健康状態が刻まれていると考えたのです。
分子生物学的視点:ノルアドレナリンが紡ぐ血管の対話
なぜ睡眠中のわずかな動きで皮膚温度が変化するのでしょうか。ここには緻密な自律神経系の制御メカニズムが介在しています。指先に装着されたウェアラブルデバイス(オーラリング)が捉える温度変化の背景には、分子レベルのドラマが隠されています。
身体が動くと、それがトリガーとなって交感神経系が刺激されます。具体的には、交感神経アドレナリン作動性経路を通じて、神経末端からノルアドレナリンが放出されます。このノルアドレナリンが血管平滑筋の受容体に結合することで、末梢の微小血管が収縮し、皮膚表面への血流が一時的に遮断されます。その結果、末梢皮膚温度は急激に低下します。
その後、活動が収まると、血管の緊張が解け、暖かい血液が再び指先に流れ込みます。この温度の「降下」と「回復」のパターンは、個人の血管の柔軟性、受容体の感度、そして心拍出量といった心血管系のパフォーマンスを直接反映しているのです。研究チームは、この一連のプロセスを物理的なメカニズムとして数式化することに成功しました。
皮膚温度の変化は、厳密な物理法則と生理学的機序に従っている
本研究では、皮膚温度の挙動を説明するために、2つの異なる位相を組み合わせた物理モデルを構築しました。
第1の位相:熱力学的な平衡を目指すプロセス
第1の位相は、熱力学的な平衡を目指すプロセスです。ニュートンの冷却(加熱)法則に基づき、現在の皮膚温度が定常状態(最終的な安定温度)からどれだけ離れているかに比例して温度が変化すると仮定しました。この回復の速さを規定するのがパラメータk1です。
第2の位相:活動バーストによって引き起こされる摂動(揺らぎ)のプロセス
第2の位相は、活動バーストによって引き起こされる摂動(揺らぎ)のプロセスです。研究チームは、残留する温度変化が時間の経過とともに指数関数的に減衰するモデルを採用しました。ここで用いられるパラメータは、振幅の増幅率を示すa、立ち上がりの鋭さを規定するb、そして減衰の速さを示すk2の3つです。
驚くべきことに、この物理ベースのモデルは、従来の単純な線形モデルを圧倒する精度を示しました。複数の変数を用いた線形モデルの決定係数(R2)の中央値が0.35(95%信頼区間:0.17〜0.56)であったのに対し、物理モデルでは中央値0.77(95%信頼区間:0.52〜0.89)という極めて高い適合率を叩き出しました。
これは、私たちの皮膚温度の変化が、気まぐれなノイズではなく、厳密な物理法則と生理学的機序に従っていることを証明しています。
臨床的数値が語る疾患のシグナル
モデルから導き出された各パラメータは、驚くほど鮮明に心血管疾患の有無を識別しました。特に、冠動脈疾患(CAD)を持つ男性グループにおいて、その差は顕著でした。
冠動脈疾患(CAD)男性に見る顕著な偏差
モデルから導き出された各パラメータは、心血管疾患の有無を識別する強力なバイオマーカーとなりました 。特に、全年齢層の男性における冠動脈疾患(CAD)群は、健康なコントロール群と比較して、すべての物理パラメータにおいて統計学的に有意かつ広範な差異を示しました 。
具体的なエフェクトサイズ(Cohen’s d)は以下の通りです。
- k1(温度回復定数):0.26
- a(MET振幅ゲイン):0.26
- b(立ち上がり急峻度):0.27
- k2(減衰急峻度):0.30
男性のCAD群が「顕著」である理由は、他の疾患群(例えば心房細動など)に比べて、モデルを構成する4つのパラメータすべてにおいて一貫して有意なエフェクトサイズが確認された点にあります 。これは、冠動脈疾患による全身的な血管の変調が、睡眠中のわずかな動きに対する反応の「強さ」「鋭さ」「回復速度」のすべてに影響を及ぼしている実態を浮き彫りにしています 。
女性における疾患とパラメータの関係
女性においては、疾患の影響の現れ方が男性とは異なっていました 。全年齢層の女性では、糖尿病(D)や高血圧との併存(H+D)がパラメータに最も強く影響していました 。
特に45歳以下の若い女性の糖尿病患者グループでは、オフセットの鋭さを示すk2パラメータにおいて、Cohen’s dが0.61という大きなエフェクトサイズが観察されました 。これは、若年女性の糖尿病患者において、末梢血管の収縮からの回復プロセスに特異的な生理学的変化が起きていることを示唆しています 。
多変量解析の結果によれば、糖尿病は性別や年齢を調整した後でも、k1(p < 0.001)、b(p < 0.01)、k2(p < 0.001)に対して有意な負の影響を与えており、血管の応答性が鈍化している実態が数値として裏付けられました 。
この研究が切り拓く新規性
本研究の真の価値は、ウェアラブルデータを「静的なスナップショット」から「動的なバイオマーカー」へと昇華させたことにあります。
これまでのウェアラブル研究の多くは、安静時心拍数や歩数といった分かりやすい指標に終始してきました。しかし、本研究は「一見無意味に見える睡眠中の温度の揺らぎ」の中に、高度な心血管機能の情報が隠されていることを見出しました。
また、複雑な機械学習による「ブラックボックス化」を避け、物理法則に基づくメカニスティック・モデリングを採用した点も特異的です。これにより、単に疾患を予見するだけでなく、なぜそのような変化が起きるのかという生理学的な解釈を可能にしました。パラメータk1は熱慣性や安静時の血管緊張を、bやk2は血管の弾力性や再灌流の効率を反映しているという解釈は、臨床医にとっても極めて納得感のあるものです。
※ おまけ参照
限界と慎重な解釈
優れた研究には必ず限界が存在します。本研究においても、いくつかの制約を理解しておく必要があります。
第1に、データの収集が管理されていない日常生活下で行われたため、周囲の環境温度が不明であるという点です。寝室の温度や寝具の使用状況は、皮膚温度のベースラインや回復速度に直接影響を与えます。疾患群が好んで寒い環境で寝ていた可能性は低いと考えられますが、完全にその影響を排除できたわけではありません。
第2に、活動量の指標であるMETの分解能です。本研究では60秒単位のデータを使用していますが、より高頻度な加速度データを用いることで、摂動の振幅と温度応答の相関をさらに精密に記述できる可能性があります。
第3に、疾患の罹患期間が不明であることです。動脈硬化の進行度は診断からの時間に依存するため、罹患期間という変数が加われば、より強力なモデルとなった可能性があります。
明日から実践できること
この論文から私たちが学べる、具体的で実践的な知見は何でしょうか。
まず、ウェアラブルデバイスを使用している方は、単に「昨晩の平均体温」を見るのをやめてみてください。もしアプリのグラフで、睡眠中に激しい温度の上下動が見られる場合、それはあなたの身体が小さな動きに対しても敏感に、あるいは過剰に応答しているサインかもしれません。
特に、高血圧や糖尿病のリスクを自覚している方にとって、指先の温度は単なる「冷え」の指標ではなく、血管の「しなやかさ」のバロメーターです。本研究が示したように、血管の応答性は加齢とともに低下(k1やk2の減少)しますが、これは適切な生活習慣の改善によってその進行を緩やかにできる可能性があります。
睡眠の質を整えることは、単に脳を休めるだけでなく、心血管系に対する不必要な「夜間のストレステスト」の負荷を軽減することにも繋がります。指先の温度がスムーズに定常状態へと回復するような、質の高い休息を確保することが、長期的な心血管の健康を守る鍵となります。
結論
心血管系は、私たちが意識を失っている睡眠中も、環境や動きに対して絶え間なく応答し続けています。本研究が示した物理モデルによるアプローチは、将来的にスマートウォッチやスマートリングが、医師の診察を待たずとも私たちの心血管系の衰えを早期に察知し、警告を発する未来を約束しています。平均という概念に隠されていた生理学的なドラマを解き明かすことで、デジタル医療は真の意味で「個々の身体に寄り添う学問」へと変貌を遂げようとしているのです。
参考文献
Burks, J.H., Hartogensis, W., Dilchert, S. et al. Wearable-derived skin temperature dynamics during sleep reveal cardiovascular perfusion deficits through mechanistic modeling. npj Digit. Med. (2026). https://doi.org/10.1038/s41746-026-02633-2
おまけ
心血管疾患を予測するのにPPG(光電容積脈波)が利用されることが比較的一般的でした。心血管疾患の予測においてPPGの活用はすでに「確立」されていますが、一般向けのウェアラブルデバイスで測定される皮膚温の「動的な変化(ダイナミクス)」を活用するアプローチは、新規性が高いと言えます。
それぞれの現状と、なぜ皮膚温の活用が新しい(革新的)なのかを整理します。
PPG:心血管予測における確立された主役
PPGは、スマートウォッチやスマートリング(Oura Ringなど)に搭載されている緑色や赤色のLED光を用いて、皮膚下の血管容積の変化を測定する技術です。この技術は、すでに心血管系の健康状態を評価する上で、以下のような多彩な指標を算出するために広く活用されています。
| 指標 | 説明 | 心血管疾患への関連 | 現状 |
| 心拍数 (HR) | 1分間の心臓の拍動数。 | 安静時心拍数の高値はリスク因子。 | 確立・普及 |
| 心拍変動 (HRV) | 心拍と心拍の間隔の周期的な変化。 | 自律神経のバランスやストレス、回復度を反映。低HRVはCVDリスク。 | 確立・普及 |
| 脈波伝播速度 (PWV) | 心臓から送り出された血液の脈波が末梢に届く速度。 | 血管の硬さ(動動脈硬化)を反映。確立された独立したリスク因子。 | 研究・一部実装中 |
| 夜間血圧変動 | 睡眠中の血圧の低下パターン(ディッパー型など)。 | 通常のディッパー型(10-20%低下)が崩れるとリスク上昇。 | 研究段階 |
皮膚温:これまでの限界と「新しい」活用法
これまで、ウェアラブルデバイスで測定される「皮膚温」は、主に「現在の体温(平均値)」として扱われ、CVDの予測に直接用いられることはほとんどありませんでした。
1. これまでの限界
- ノイズが多すぎる: 皮膚温は外気温、運動、食事、ホルモンバランスなどの影響を強く受け、日常生活下では「慢性的な疾患の影響」だけを切り出すことが非常に困難でした。
- 静的なデータの比較: 「寒かったから温度が低い」のか「血管が硬いから温度が低い」のかの区別が、単純な「平均値の比較」ではできません。
2. 新しい活用法:DST(Distal Skin Temperature)ダイナミクス
今回解説した論文のように、日常生活下でのDST(Distal Skin Temperature)の「動的な応答パターン(ダイナミクス)」に着目したアプローチは、非常に新しく注目されています。
何が「新しい」のか:
- 「平均」ではなく「プロセス」: 単なる温度測定ではなく、例えば「睡眠中の微細な動き(METのバースト)」という天然の刺激に対する、Dstの一時的な降下と、その後の回復プロセス全体(トラジェクトリ)を解析します。
- 物理法則に基づくモデル(Mechanistic Modeling): ノイズの多いデータを、ニュートンの冷却法則などの物理ベースの数理モデルで解析します。これにより、ノイズから「血管の応答性能」という純粋な物理パラメータ(k1やk2)を抽出できるようになりました。
- 血管の柔軟性(Perfusion)を捉える: このモデルから得られたパラメータは、これまで難しかった日常生活下での「血管のしなやかさ」や「末梢への血流供給(Perfusion)の欠損」を間接的に捉え、冠動脈疾患(CAD)などのリスクを識別します。
まとめ
- PPG: 確立・普及しており、心拍数、HRV、動脈硬化度など多彩な指標を算出。
- DST(平均): CVD予測にはほぼ未活用。
- DST(ダイナミクス): 非常に新しいアプローチ。 物理モデルを用いて、これまで見逃されていた睡眠中の微細な温度変動から「血管のしなやかさ」を暴き、CVDの早期発見を目指す。
確立されたPPGと、この新しいDSTダイナミクスという2つの視点を組み合わせることで、ウェアラブルデバイスは将来、より早期かつ正確に心血管疾患の予兆を捉える臨床診断ツールへと進化していくことが期待されています。