はじめに
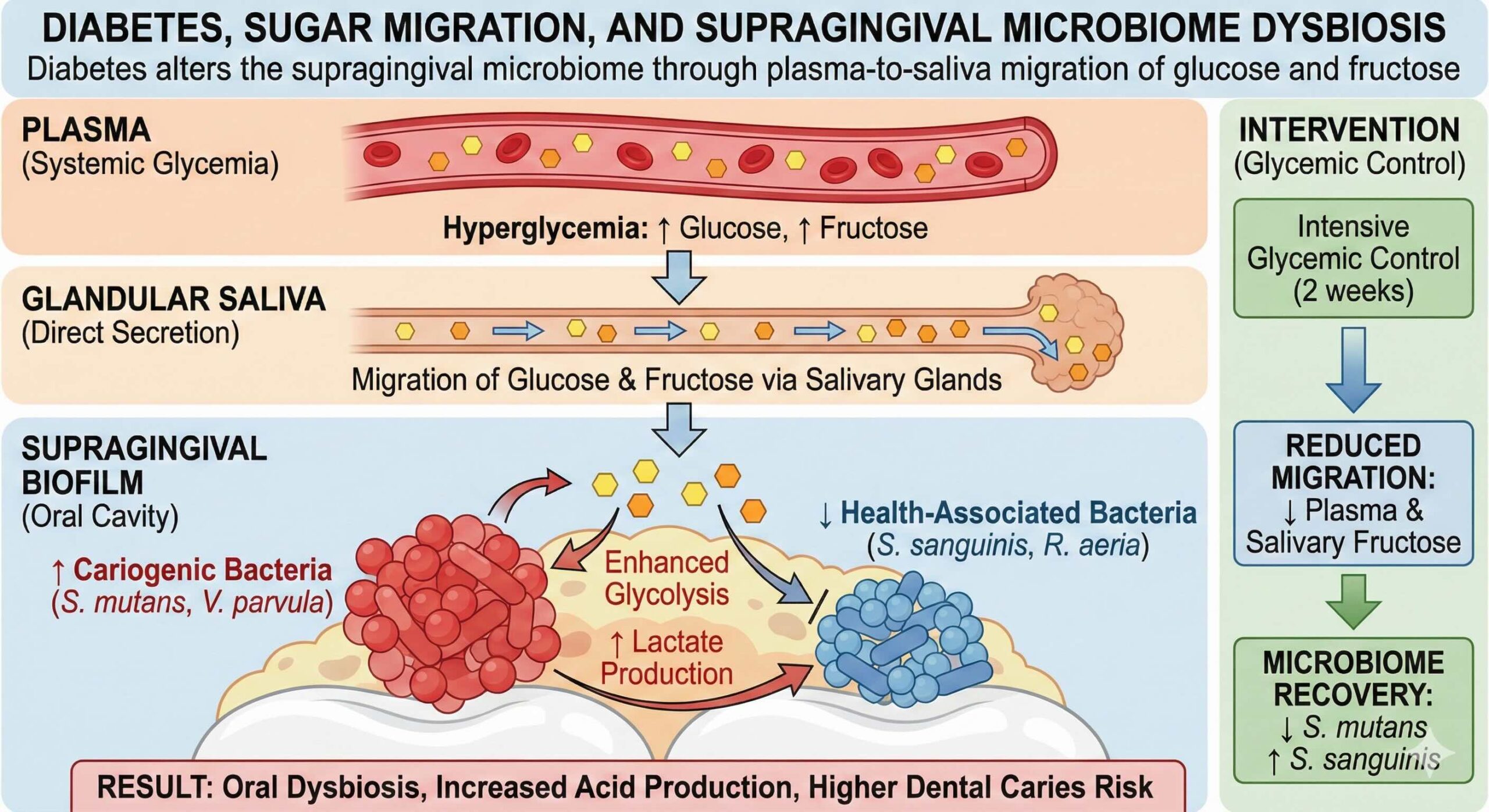
糖尿病患者の口腔内で何が起きているのか。この古くからの問いに対し、最新のメタボロミクスとメタゲノミクスが、驚くべき「体内からの供給」の実態を暴き出しました。私たちは通常、虫歯の原因を「口から摂取した砂糖」に求めますが、本研究は、高血糖状態にある身体そのものが、唾液腺を通じて虫歯菌に栄養を与え続けているという、逃れられないリスクを浮き彫りにしています。大阪大学の研究チームが発表したこの論文は、糖尿病が歯肉縁上微生物叢をいかに変容させ、虫歯(う蝕)の温床を作り出すのかを分子レベルで解明した画期的な成果です。
研究プロトコールの概要(PECO)
P(対象):2型糖尿病患者31名および健常対照者30名
E(要因):高血糖および血漿から唾液への単糖類(グルコース、フルクトース)の移行
C(比較):健常群との比較、および糖尿病患者における集中血糖コントロール前後での比較
O(アウトカム):腺唾液・全唾液の代謝物組成、歯肉縁上マイクロバイオームの種組成および機能、臨床的う蝕指標
口腔代謝解析の技術的ブレイクスルー
これまでの口腔内代謝解析には、大きな壁がありました。口の中に溜まった全唾液を解析しても、そこに含まれる糖分が身体から直接分泌されたものなのか、あるいは口腔内の細菌が摂取して代謝した後の残渣なのかを区別することが極めて困難だったからです。本研究の最大の特徴は、顎下腺および舌下腺から分泌される極微量の唾液、すなわち細菌による修飾を受ける前の純粋な生体由来サンプルである「腺唾液」を直接採取する技術を確立した点にあります。
解析結果
血液(血漿)と、2種類の唾液(腺唾液と全唾液)に含まれる成分を詳しく調べました 。非標的メタボローム解析の結果、血漿で78種類、腺唾液で125種類、全唾液で143種類の親水性代謝物が同定されました。これらのプロファイルを多変量解析(PERMANOVA)で評価したところ、糖尿病という病態を最も明確に反映していたのは血漿(R2(アールスクエア、決定係数)) = 37.5%)でしたが、腺唾液も12.4%という高い説明変数を示し、全唾液の3.7%を大きく上回りました。つまり、腺唾液は血中の代謝状態を口腔内へと投影する鏡であり、全唾液よりもはるかに敏感に全身の血糖状態を反映していることが明らかになったのです。全唾液には細菌が糖を食べて作り出した物質などが大量に混じっており、それが身体本来の情報を隠す「ノイズ」になってしまいます 。
血漿から口腔内へ漏れ出す糖の動態
糖尿病患者の口腔内では、血漿中のグルコースだけでなく、フルクトース(果糖)もまた腺唾液へと移行していることが確認されました。これまで糖尿病患者の唾液中グルコース濃度の上昇は知られていましたが、フルクトースの移行をこれほど精密に捉えたのは本研究が初めてです。
なお、果糖(フルクトース)は、清涼飲料水・加工食品に広く使用され、多量に含有しています。これらを摂取することによる食事由来(外因性)のフルクトース以外に、糖尿病においてはポリオール経路を介して体内にて(内因性に)フルクトースが産生されます。
血漿、腺唾液、全唾液の間で糖濃度が正の相関を示した一方で、1,5-アンヒドログルシトール(1,5-AG)は負の相関を示しており、これは全身の血糖動態が口腔環境へと転写されていることを強く裏付けています。
研究チームは、これら糖の「移行レベル」を評価するために、血漿、腺唾液、全唾液の各段階における糖濃度をランク付けして合算した「糖移行スコア(Saccharide migration score)」を定義しました。例えると、「身体の中から、どれくらい虫歯菌のエサ(糖分)が漏れ出しているか」を数値化したものです。
・血漿:エサの「供給源」です 。
・腺唾液:細菌に食べられる前の、蛇口から出たての「エサの量」です 。
・全唾液:細菌がエサを食べた後に残った「食べ残し」です 。
分析の結果、このスコアが高いほど、未処置の虫歯(ICDASスコア3以上)の数や、プラークの蓄積量を示す歯垢指数が有意に高いことが統計的に示されました。
・う蝕の重症度: 肉眼的な歯質欠損を伴うICDASスコア3以上の歯数が有意に多い 。
・プラークの蓄積: 歯垢指数(Plaque Index)が高い。
・欠損歯数: 喪失した歯の数が多い。
糖尿病患者の口腔内は、食事をしていない就寝中であっても、体内から絶え間なく供給される糖分によって、虫歯菌が常に飼育されている特殊な環境にあると言えます。
虫歯の原因は「食べた砂糖」だけではないのです 。このスコアが高い人は、何も食べていない時でも、身体の中から虫歯菌に「おやつ」を与え続けてしまっている状態なのです。
歯肉縁上微生物叢の機能的および分類学的変容
ショットガン・メタゲノム解析によって明らかになったプラーク(歯垢)内の細菌組成の変化は、極めて劇的でした。糖の移行量が多い被験者の口腔内では、以下の変化が確認されました。
増加した菌:Streptococcus mutans、Veillonella parvula、Scardovia wiggsiae、Actinomyces sp. oral taxon 448
減少した菌:Streptococcus sanguinis、Corynebacterium durum、Rothia aeria、Neisseria elongata
特に、健康な口腔内でH2O2(過酸化水素)を産生して悪玉菌を抑制するStreptococcus sanguinisが減少し、強力な酸産生能を持つStreptococcus mutansが増加するという、生態学的なバランスの崩壊が確認されました。また、Actinomyces sp. oral taxon 448とう蝕の強い相関も示されており、この菌種が糖尿病関連う蝕の新たな指標となる可能性が示唆されています。
さらに機能解析(MetaCyc経路解析)では、糖の移行レベルに比例して、デンプン分解(Starch degradation III)、グリコーゲン分解、および解糖系(Glycolysis IV)に関わる遺伝子群が有意に強化されていました。これに対応する酵素として、シクロマルトデキストリナーゼ(EC 3.2.1.54)や6-ホスホフルクトキナーゼ(EC 3.2.1.11)の蓄積が認められました。これは、単に菌の数が増えるだけでなく、コミュニティ全体が「より効率的に糖を分解し、酸を産生する」モードへと切り替わっていることを示しています。
フルクトースが握る、細菌間競争の鍵
分子生物学的な視点で見ると、移行したフルクトースは単なるエネルギー源以上の役割を果たしています。S. mutansはフルクトース・ホスホトランスフェラーゼ・システム(PTS、EC 2.7.1.202)を介してフルクトースを取り込みます。この代謝の過程で生成されるメチルグリオキサールなどの副産物は、耐性の低いS. sanguinisなどの善玉菌を攻撃する武器となります。
研究チームが行った2種混合バイオフィルム実験では、グルコース単独の場合よりも、フルクトースを添加した環境下において、S. mutansがS. sanguinisに対してより高い増殖優位性を示すことが確認されました。さらに、プラーク中の乳酸濃度と糖移行スコアの間に有意な正の相関(r = 0.268, p = 0.037)が認められたことは、体内からの糖供給が直接的に口腔内の酸性度を高め、歯の脱灰を促進している決定的な証拠と言えます。
血糖コントロールによる迅速な口腔内リセット
本研究の臨床的意義を最も高めているのは、T2D患者を対象とした介入研究の結果です。入院による2週間の集中血糖コントロール治療により、患者のHbA1cは平均9.1%から8.4%へ、空腹時血糖値は8.1mmol/L(146 mg/dL)から6.1mmol/L(110 mg/dL)へと改善しました。この短期間の改善に連動して、腺唾液中のフルクトース濃度が有意に減少し、プラーク中のフルクトースPTS(EC 2.7.1.202)遺伝子の保有量も劇的に減少しました。
これと並行して、S. mutansの相対存在量が減少し、S. sanguinisやRothia aeriaといった健康関連菌が増加に転じました。興味深いことに、この2週間の間に患者のプラーク量そのものは変化していませんでした。つまり、ブラッシングなどの物理的な清掃効率が変わらなくても、全身の血糖状態を管理するだけで、プラークの「質」が病的なものから健康的なものへと改善されることが実証されたのです。
本研究の限界(Limitation)
本研究には、解釈にあたって考慮すべきいくつかの限界点があります。
第一に、被験者の入院前の食事習慣や家庭での口腔清掃頻度について、完全に統一された詳細なデータが得られていない点です。これらが背景因子としてマイクロバイオーム構成に独立した影響を与えている可能性を完全には排除できません。
第二に、サンプルサイズが合計61名と比較的限定的であるため、極めて低頻度の菌種や、微細な発現変化を持つ酵素については、統計的な検出力が不足している可能性があります。
第三に、年齢の乖離という交絡要因です。対照群(平均42.1歳)に対し、糖尿病群(平均63.9歳)は有意に高齢でした。統計的な調整(共分散分析)や、年齢を一致させたサブセット解析(12名対12名)によって、主要な結論である糖移行と菌相の関係は維持されることが確認されていますが、加齢に伴う唾液腺の生理的変化が糖の透過性に与える影響については、今後のさらなる研究が必要です。
明日からの実践
本研究の知見は、歯科および内科の臨床現場にパラダイムシフトをもたらします。明日からの行動に繋がる具体的な実践事項を提案します。
まず、糖尿病患者の虫歯リスク評価において、食事回数やブラッシング指導といった従来の項目に「直近の血糖変動」を最重要項目として加えるべきです。HbA1cが高い状態は、虫歯菌に対して常に点滴で栄養を与えているようなものであると患者に視覚的に説明してください。この「自分自身の血液が虫歯を育てている」という理解は、患者の治療意欲を根本から変える力を持っています。
次に、血糖コントロールの効果を「お口の爽快感」や「歯ぐきの健康」と結びつけて評価することを推奨します。本研究が示したように、わずか2週間の適切な血糖管理が口内の悪玉菌を劇的に減らします。この即効性は、患者にとって血糖管理を継続するための強力なモチベーションとなるはずです。
最後に、食品選択の重要性です。フルクトースが菌種間の勢力図を悪化させる鍵であることが判明したため、果糖ブドウ糖液糖を含むソフトドリンクなどの過剰摂取は、糖尿病の悪化だけでなく、直接的な「口内細菌の凶暴化」を招くことを強調すべきです。歯科医師と内科医師が、この「糖移行」という共通のキーワードで情報を共有し、連携することで、糖尿病患者の全身の健康と、一本の歯の寿命を同時に守ることが可能になります。
参考文献
Sakanaka, A., Furuno, M., Ishikawa, A. et al. Diabetes alters the supragingival microbiome through plasma-to-saliva migration of glucose and fructose. Microbiome 14, 48 (2026). https://doi.org/10.1186/s40168-025-02256-x