はじめに:MASLD-名称変更が示唆するパラダイムシフト
かつてNAFLD(非アルコール性脂肪性肝疾患)と呼ばれていた疾患は、現在、MASLD(Metabolic dysfunction-associated steatotic liver disease)という新たな概念へと進化しました。この名称変更は単なるラベルの貼り替えではありません。「アルコールを除外する」という消極的な定義から、「代謝機能障害を病態の中心に据える」という積極的な定義への転換を意味します。
世界的な有病率は約38%に達し、まさにパンデミックの様相を呈しています。しかし、ここで驚くべき疫学的データがあります。MASLD患者の死因として最も多いのは、肝硬変や肝がんといった肝臓関連死(1000人年あたり1.75)ではなく、心血管疾患(1000人年あたり5.54)なのです。つまり、脂肪肝は単なる肝臓の病気ではなく、全身の代謝異常が引き起こすシステミックな疾患であり、その結末はしばしば心臓に現れるという事実を、我々は直視しなければなりません。
不均一性(Heterogeneity):脂肪肝は「すべて同じ」ではない
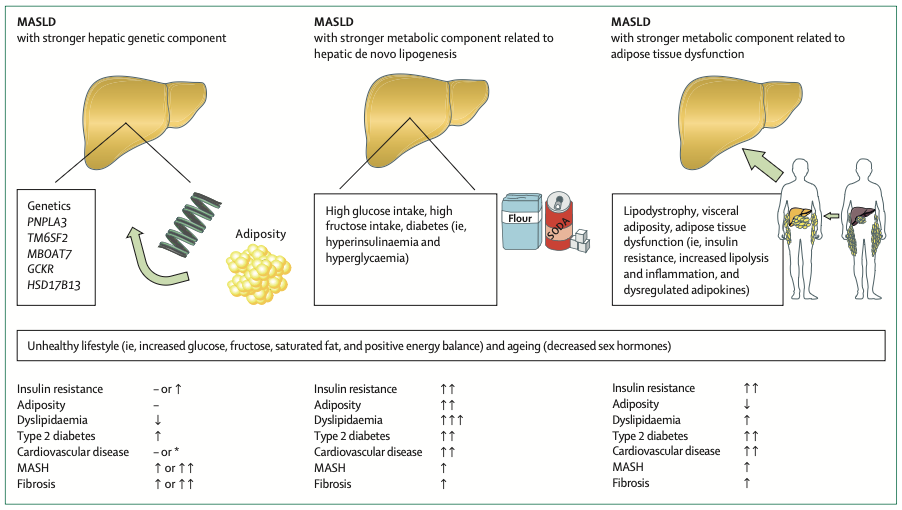
本論文の白眉は、MASLDという巨大な疾患群を「不均一性(ヘテロジェネイティ)」という切り口で解剖した点にあります。すべての脂肪肝が、過食と運動不足だけで説明できるわけではありません。論文では、その病態形成における主要なドライバーを以下の3つのクラスターに分類して論じています。
遺伝的要因が支配するMASLD(The Genetic Cluster)
特定の遺伝子変異、特にPNPLA3(rs738409 Gアレル)やTM6SF2などの変異を持つ群です。興味深いことに、これらの変異を持つ人々は、肝脂肪量が多く、肝炎や肝線維化、肝細胞がんへの進行リスクが高いにもかかわらず、心血管疾患のリスクは必ずしも高くありません。むしろ、冠動脈疾患から保護される傾向さえ見られます。
分子生物学的には、PNPLA3変異により、ミトコンドリア機能障害が生じ、炭素がDe novo lipogenesis(新規脂肪合成)ではなくケトン体生成へとチャネルされること、あるいはVLDL(超低密度リポタンパク質)の分泌障害により肝臓内に脂肪が留まるメカニズムが関与しているとされます。彼らの肝臓には脂肪が溢れていますが、全身的なインスリン抵抗性は比較的軽微であり、これが「肝臓は悪いが心臓は守られる」というパラドックスを生んでいます。
肝臓での新規脂肪合成(DNL)が支配するMASLD
これは、いわゆる典型的な「メタボリックな脂肪肝」です。過剰なグルコースやフルクトースの摂取により、肝臓内でのDe novo lipogenesis(DNL)が亢進しているタイプです。
健常者では肝臓のパルミチン酸の約11%がDNL由来ですが、肥満者では19%、そして肥満を伴うMASLD患者では実に約38〜40%がDNL由来であるというデータが示されています。このタイプは、全身性のインスリン抵抗性、高血糖、脂質異常症を伴い、心血管疾患リスクが著しく高いのが特徴です。
脂肪組織機能不全が支配するMASLD(The Lipodystrophic Cluster)
「痩せ型(Lean)MASLD」として知られるこのタイプは、全MASLDの約7〜20%を占めると推定されています。彼らはBMIが正常範囲内であるにもかかわらず、代謝的には極めて不健康です。
病態の本質は「脂肪組織の容量オーバー」にあります。皮下脂肪(特に臀部や大腿部)に脂肪を貯め込む能力が低く、行き場を失った脂肪酸が肝臓へと流入(オーバーフロー)します。遺伝性あるいは後天性のリポジストロフィー(脂肪萎縮症)に類似した病態であり、肥満を伴うMASLDと比較しても、総死亡リスクが高い(ハザード比 1.61)という衝撃的なデータが提示されています。見た目のスマートさに反して、体内では激しい代謝ストレスが生じているのです。
薬物療法の最前線:メカニズムに基づく治療戦略
治療においても、画期的な進歩が見られます。本論文では、治療薬を「体重減少を伴うもの」と「伴わないもの」に分類し、それぞれの臨床試験データを詳細に分析しています。
体重減少を伴う薬剤:インクレチン関連薬の躍進
現在、最も注目されているのがGLP-1受容体作動薬およびその併用薬です。
セマグルチド(GLP-1受容体作動薬):第3相試験の中間解析において、2.4mgの投与により63%の患者で肝線維化の悪化を伴わないMASH(代謝機能障害関連脂肪肝炎)の消失が達成されました(プラセボ群は34%)。
チルゼパチド(GIP/GLP-1受容体共作動薬):さらに強力な効果が示されています。第2相試験において、15mg投与群の62%でMASHが消失し、さらに約51%で線維化の改善が見られました。
スルボデュタイド(グルカゴン/GLP-1受容体共作動薬):グルカゴンによるエネルギー消費亢進作用が加わり、最大62%のMASH消失率を達成しています。
レタルチド(GIP/GLP-1/グルカゴン受容体トリプル作動薬):第2a相試験において、肝脂肪量を平均82.4%減少させるという驚異的な脂肪除去効果を示しました。
これらの薬剤は、強力な体重減少効果(10〜15%以上)を介して、肝臓の脂肪毒性を劇的に改善します。
体重減少を伴わない薬剤:肝臓特異的アプローチ
体重を減らすことが必ずしも正解ではない、あるいは困難な患者群(痩せ型や遺伝的要因が強い場合)には、以下の薬剤が光となります。
レスメチロム(THR-β作動薬):2024年3月、米国FDAによりMASH治療薬として初めて承認されました。肝臓特異的に甲状腺ホルモン受容体βを刺激し、ミトコンドリア活性を高めて脂肪を燃焼させます。第3相試験では、体重変化を伴わずに、約30%の患者でMASH消失、約26%で線維化改善を達成しました。
FGF21アナログ(ペゴザファーミンなど):代謝調節因子であるFGF21の誘導体は、線維化改善に特化した効果を示しています。第2b相試験では、線維化改善率が他剤と比較しても高い傾向にあり、特に線維化が進んだ症例への応用が期待されます。
Limitations
しかし、手放しで楽観視できるわけではありません。本論文でも指摘されている通り、いくつかの限界(Limitations)が存在します。
第一に、現状の臨床現場では、これらのサブタイプ(遺伝性、DNL型、脂肪不全型)を簡便に識別するバイオマーカーや検査法が確立されていません。遺伝子検査は一般的ではなく、DNLの測定には特殊な同位体解析が必要です。
第二に、遺伝的要因が強い患者において、薬物療法が長期的な予後(特に肝がん発生率)をどこまで改善できるかについての長期データがまだ不足しています。
第三に、高額な新規薬剤へのアクセスや、医療経済的な課題も無視できません。
明日からの実践:知性を健康に転化する
この論文から得られる知見を、明日からどう活かすべきでしょうか。
脂肪肝を指摘された場合、自己のフェノタイプを推測する
BMIを確認
もしあなたが脂肪肝を指摘された場合、BMIを確認してください。肥満(BMI 25以上)であれば、過栄養によるDNL亢進タイプの可能性が高く、減量(体重の7〜10%以上)が特効薬となります。
一方で、BMIが正常(25未満)であるにもかかわらず脂肪肝がある場合、あなたは「痩せ型MASLD」あるいは「遺伝的要因」を持つ可能性があります。この場合、単なるカロリー制限だけでは不十分かもしれません。筋肉量を維持しつつ、質の高い脂質摂取や、インスリン抵抗性を改善する運動療法、あるいは専門医による早期の薬物療法の検討が必要です。
心血管リスクへの警戒
肝臓の数値(ALTやAST)だけに目を奪われてはいけません。MASLDの最大のリスクは心臓にあることを想起し、血圧、脂質プロファイル、血糖値を厳格に管理することが、肝臓を守る以上に生命を守るために重要です。
最後に
「脂肪肝=食べ過ぎ」という単純な図式を捨て、自身の代謝システムがどこでエラーを起こしているのかを俯瞰する。それこそが、現代の知識人に求められる健康管理のあり方なのです。
参考文献
Stefan N, Yki-Järvinen H, Neuschwander-Tetri BA. Metabolic dysfunction-associated steatotic liver disease: heterogeneous pathomechanisms and effectiveness of metabolism-based treatment. Lancet Diabetes Endocrinol. 2025; 13: 134-48. https://doi.org/10.1016/S2213-8587(24)00318-8