はじめに:見過ごされてきた狭心症の真犯人
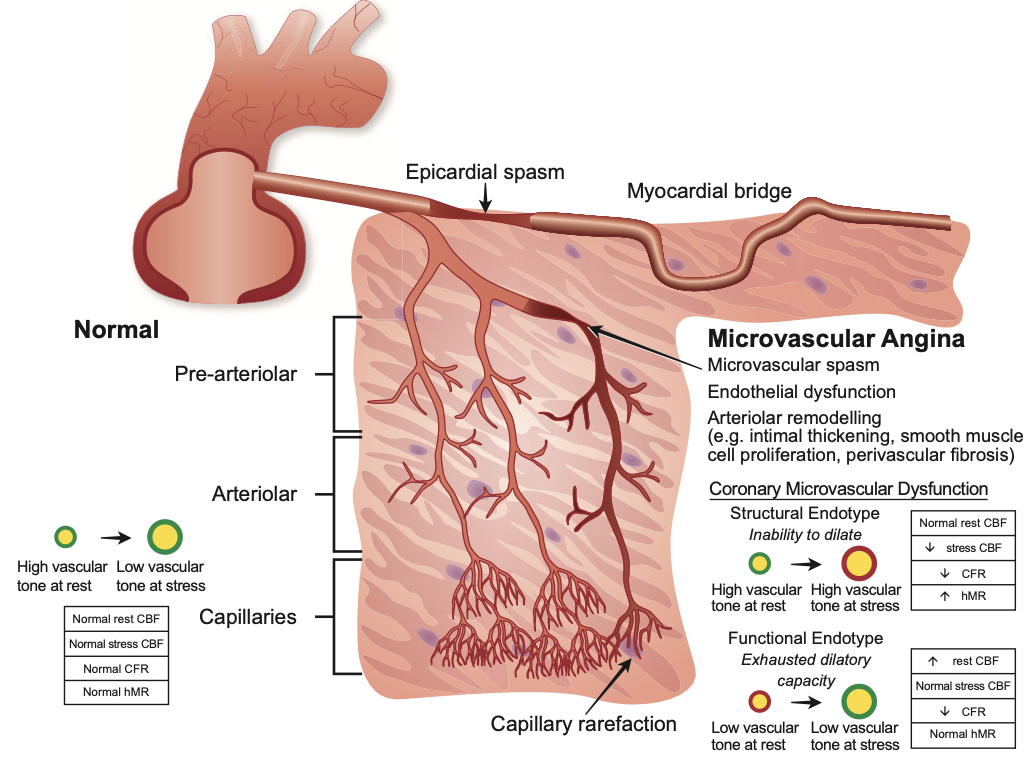
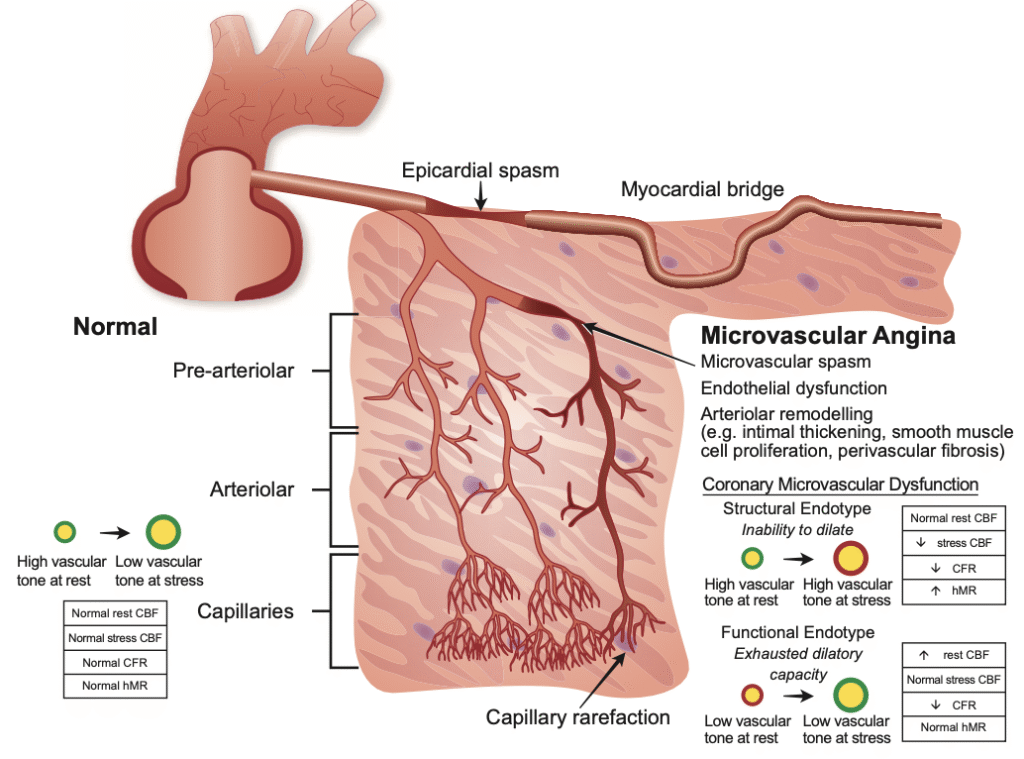
胸痛や呼吸困難といった心筋虚血を疑わせる症状を持ちながら、冠動脈造影では明らかな閉塞性病変が認められない患者群は、非閉塞性冠動脈疾患を伴う狭心症(ANOCA:Angina with Nonobstructive Coronary Arteries)として近年、その臨床的な重要性が再認識されています。歴史的に「異常なし」と片付けられてきたANOCAですが、実際には、冠微小血管機能不全(CMD:Coronary Microvascular Dysfunction)や血管攣縮性狭心症(VSA:Vasospastic Angina)といった病態が潜んでおり、これらは心臓イベントのリスク上昇と関連することが示されています。
しかしながら、CMDやVSAの診断は、特定の手技や専門知識を要するため、日常診療においてはいまだに低診断の状態にあります。既存の侵襲的評価に関する研究の多くは、厳格な患者選択基準とプロトコル化された手技の下で行われており、実際の多様な臨床現場での検査の「使われ方」や、それが治療決定にどのように影響しているのかについては、ほとんどわかっていませんでした。
【参考】(Eur Heart J. 2021 Nov 21;42(44):4601-4604)
研究の目的
このFlowLab研究は、厳密にデザインされた臨床試験とは一線を画し、現実の臨床現場(リアルワールド)における侵襲的CMD/VSA評価の使用状況を前向きに観察しました。
本研究では、患者選択、血管作動薬の中断、検査のタイミング、そして血管攣縮誘発試験(VSA testing)を実施するかどうかを含め、すべての手技的および治療的決定が、術者である医師の裁量に任されました。これにより、多様な臨床的疑いの程度や様々な手技のワークフローの中で、CMD/VSA評価がどのように組み込まれ、その結果が即座に患者管理にどのような影響を与えるかを包括的に捉えることが可能となりました。
FlowLab研究の概要と方法論
FlowLabは、米国の14施設で実施された前向き多施設共同観察研究であり、合計253件の手技が登録されました。対象となった患者は、治療医がCMDの可能性を考慮し、Coroventis CoroFlow Cardiovascular SystemとPressureWire Xガイドワイヤーを用いた侵襲的評価を行うことを決定したANOCAの患者群です。
検査では、ボーラス熱希釈法を用いて、以下の重要な生理学的指標が測定されました。
- 冠血流予備量(CFR:Coronary Flow Reserve): 安静時血流に対する最大冠血流の比。血管拡張能および微小血管の機能的状態を評価し、異常値は<2.5と定義されました。
- 微小循環抵抗指標(IMR:Index of Microcirculatory Resistance): 最大冠血流時における遠位部圧と平均通過時間の積。微小血管の構造的および機能的抵抗性を反映し、異常値は≥25と定義されました。
術前のANOCAに対する疑いの程度は、高疑いが56%(98/176)、中疑いが26%(45/176)、低疑い/除外目的が19%(33/176)と、高リスク群に偏ることなく、幅広い臨床シナリオが含まれていました。
注目すべき主要なデータと診断的インパクト
本研究で得られたデータは、CMD/VSAの侵襲的評価の有用性を強力に支持しています。
検査の迅速性と多様なワークフロー
CoroFlowを用いた手技の中央値はわずか10分(四分位範囲:7〜14分)であり、侵襲的血管造影に最小限の時間追加で済むことが示されました。これは、PCIの最適化のために光学干渉断層撮影(OCT)を行う際の平均的な追加時間(約11分)に匹敵し、臨床ワークフローへの統合が容易であることを裏付けています。
手技のタイミングも多様でした。CoroFlow評価の決定は、手技開始前または開始時に52%(131/253)で行われた一方で、冠動脈造影後(39%、99/253)や、その他の生理学的評価後(6%、16/253)にも決定されており、術者の裁量による「アドホック(ad hoc)評価」の重要性が浮き彫りになりました。
高い診断確定率とCFR・IMRの分布
主要な結果として、全患者の53%(135/253)で最終的にCMDまたはVSAの診断が下されました。これは、胸痛を主訴とする患者群(88%、222/253)において、侵襲的評価がいかに多くの「真の病態」を明らかにしているかを示しています。
生理学的指標の分布を見ると、
CFR異常(<2.5)=冠血流予備能異常は43%(110/253)、
IMR異常(≥25)=微小循環抵抗亢進は28%(72/253)
に認められました。
このうち、CFRとIMRの両方が異常であった患者は18%(44/251)であり、両指標が正常であった患者は47%(119/251)でした。
重要なのは、35%の患者でCFRとIMRの値が事前に定められた閾値において「解離」していた点です。これは、微小血管病態が機能的異常(主にCFRで評価)と構造的・抵抗性異常(主にIMRで評価)の複雑な組み合わせであることを示唆しており、単一の指標だけでなく両方の評価が必要であることの根拠となります。
診断の明確化と治療への反映
診断の推移を見ると、血管造影後にCMD/VSAまたは混合疾患が疑われた患者(184例)のうち、CoroFlow評価後に68%(125/184)でその診断が確認され、残りは閉塞性冠動脈疾患または「どちらでもない」と診断が変更されました。この診断的な「シフト」は、侵襲的評価が診断の曖昧さを減らし、患者の病態理解を深める上で極めて有用であることを示しています。
【参考】( 冠攣縮性狭心症と冠微小循環障害の診断と治療)

IMRに基づく治療決定の即時的な影響
本研究で最もインパクトのある発見は、IMRの値が患者の治療方針に即座に、かつ統計学的に有意に影響を与えたことです。
IMRが上昇している患者群(IMR ≥25)は、IMRが正常範囲の患者群(IMR <25)と比較して、狭心症治療薬の追加が2倍以上(61% [44/72] vs 29% [53/181]、P<0.0001)でした。IMRは微小血管の構造的な重症度を反映する指標とされており、この結果は、IMR高値の患者群が、より積極的な薬物治療を必要とする重症な病態であることを示唆しています。
また、IMR ≥25群では、追加の予防的治療(21% vs 12%、P=0.078)やライフスタイル変更の推奨(25% vs 15%、P=0.058)においても、より高い傾向が見られました。一方、IMRが低い患者群は、非心臓血管系専門医への紹介や追加検査を受ける傾向が高く(9% vs 3%、P=0.108)、これはIMRが低い場合に症状の原因が心臓外にある可能性を考慮し、鑑別診断が広がることを示唆しています。
CFR単独での分類は、PCI実施率の上昇を除き、治療計画との関連性は見られませんでした。このことから、リアルワールドの臨床現場では、IMRが、狭心症薬の追加という具体的な治療介入の意思決定において、特に重要なトリガーとなっていることが示唆されます。
臨床への示唆と実践への応用
このFlowLab研究の知見は、ANOCA患者の診療に携わるすべての医療従事者にとって、明日からの実践に直結する重要な示唆を含んでいます。
- ANOCAを「異常なし」で終わらせない: 胸痛患者の半分以上でCMDまたはVSAが診断されるという事実は、冠動脈造影で閉塞がない場合でも、心筋虚血の原因を特定するための侵襲的機能評価を積極的に検討する必要性を示しています。
- IMRに基づいた治療の個別化: IMRが25以上という閾値は、微小血管の抵抗性が高い、すなわち微小血管病変が重度であることを示唆しています。IMR高値の患者に対しては、強力な血管拡張作用を持つ薬剤や狭心症薬を積極的に追加し、症状の改善と予後の向上を目指した個別化治療を直ちに行うべきです。
- 診断の絞り込みとリソースの最適化: IMRが低い患者では、心臓血管系の病態が原因である可能性が低くなります。このような患者群に対しては、非心臓血管系(例:消化器、呼吸器、筋骨格系)の原因を探索するための専門医への紹介や追加検査を検討することで、診断の迅速化と医療リソースの最適化が期待できます。
本研究の限界(Limitation)
本研究はリアルワールドの知見を提供する一方で、いくつかの限界も存在します。
- 施設選択の偏り: 参加施設はCoroFlowやVSA検査に経験豊富な施設である傾向があり、結果が一般の施設にそのまま外挿できるかには注意が必要です。
- データ収集の限定性: 手技中の変数のみが収集されており、ベースラインの患者特性(心血管リスク因子など)や長期的な臨床転帰のデータがありません。
- VSA検査の不均一性: VSA検査は全患者の50%のみで実施されており、全患者で実施した場合の結果との違いは不明です。
- 血管作動薬の中断プロトコル: 血管作動薬の中断プロトコルが標準化されておらず、検査結果に影響を与えた可能性があります。
最後に
上記の限界を認識しつつも、FlowLab研究は、侵襲的なCMD/VSA評価が、迅速かつ実践的であり、多岐にわたる臨床シナリオにおいて即座に治療方針を決定する上で極めて有用なツールであることを明確に示しました。
参考文献
・Bergmark, B. A., Shah, S., Toleva, O., Maksoud, A., Kearney, K. E., Kobayashi, Y., … & Sabatine, M. S. (2025). Multicenter prospective assessment of coronary microvascular dysfunction: Primary results of the FlowLab study. JACC: Advances, 4(11), 102179.
・de Silva R, Cheng K. Microvascular angina: quo tendimus? Eur Heart J. 2021 Nov 21;42(44):4601-4604. doi: 10.1093/eurheartj/ehab534. PMID: 34480544.
・2023 年 JCS/CVIT/JCC ガイドライン フォーカスアップデート版 冠攣縮性狭心症と冠微小循環障害の診断と治療(日本循環器学会 / 日本心血管インターベンション治療学会 / 日本心臓病学会合同ガイドライン)