はじめに
最新の心不全治療において、私たちの前に立ちはだかる最大の壁は「後手に回る管理」です。今回ご紹介するFUTURE HF II研究の結果は、その壁を打ち破り、患者自身が「預言者」のように自身の状態を予測し、能動的に介入する未来を提示しています。
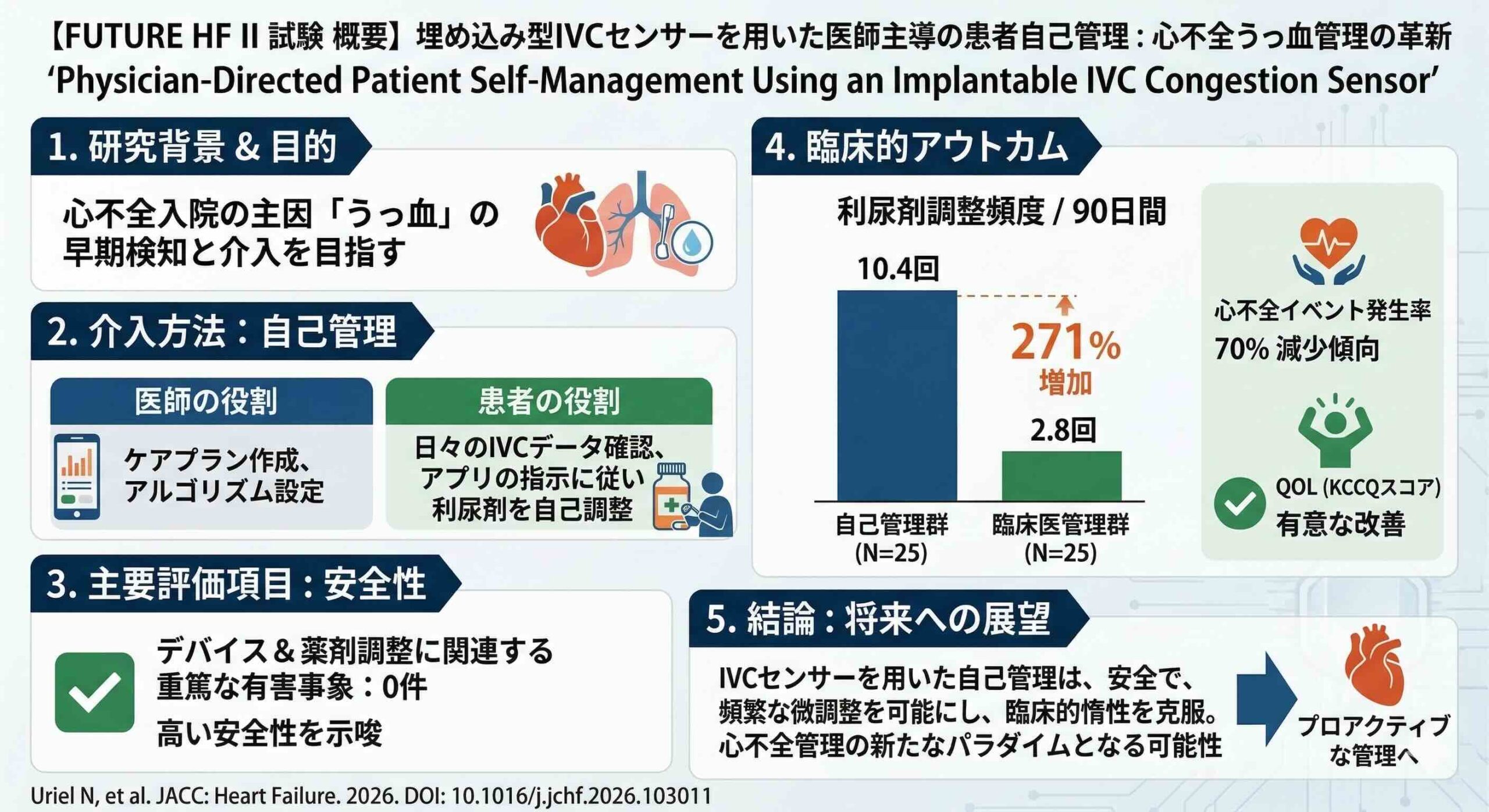
心不全による入院の主因は、心不全そのものよりも、その結果として生じる「うっ血」にあります。これまで、私たちは体重の増減や呼吸困難といった自覚症状を頼りに治療を調整してきました。しかし、こうした指標が変化した時には、すでに生理学的な代償機構は限界に達し、入院を回避するための「黄金の時間」は過ぎ去っていることが多いのです。この臨床的なタイムラグを埋めるために登場したのが、埋め込み型の下大静脈(IVC)センサーです。本研究は、このセンサーから得られるデータを患者自身がスマートフォンで確認し、医師があらかじめ設定したプランに沿って自ら薬を調整する「自己管理」の有効性と安全性を検証した画期的な報告です。
研究プロトコール概要:FUTURE HF II
本研究は、米国の複数の医療機関で実施された前方視的、非ランダム化、逐次コホート研究です。以下にそのPICOフレームワークに準じた概要をまとめます。
対象(P):18歳以上、NYHA機能分類2度または3度、過去12ヶ月以内に心不全入院歴があり、NT-proBNPが1000pg/mL以上の慢性心不全患者。駆出率の低下した心不全(HFrEF)および保存された心不全(HFpEF)の両方を含みます。被験者の総数は25人です 。
介入(I):医師主導の患者自己管理(Phase 2)。IVCセンサーのデータに基づき、スマートフォンアプリを介して医師が事前設定した「ケアプラン(利尿剤の増減など)」を患者に提示し、患者自身が介入を行います。
医師主導の患者自己管理群(Phase 2)は10人です 。
比較(C):従来型の臨床医による管理(Phase 1)。IVCデータは臨床医のみが閲覧し、標準的なワークフローで介入を決定します。
従来型の臨床医による管理群(Phase 1)は15人です 。
アウトカム(O):主要評価項目はデバイスおよび薬剤調整に関連する安全性。副次評価項目としてデバイスの使用率、利尿剤の調整頻度、心不全イベント発生率、生活の質(QOL)の変化を評価しました。
既存研究との決定的な違い:リアクティブからプロアクティブへ
これまでにも肺動脈圧(PA圧)をモニタリングするCardioMEMSなどのデバイスは存在し、心不全入院の減少に寄与してきました。しかし、PA圧の管理には、臨床医が頻繁にデータをチェックし、その都度患者に電話や外来で指示を出すという多大な労力が伴います。
本研究の最大の新規性は、モニタリングの対象を「静脈系」としたこと、そして介入の主体を「患者」に委ねたことにあります。IVCは全身の静脈容量を直接的に反映する生理学的なマーカーであり、体液貯留のみならず静脈のトーン(収縮状態)の変化にも極めて敏感に反応します。この高感度なデータを、医師が事前に作成したアルゴリズムに基づき、デジタルプラットフォームを通じて患者に開放することで、医師の介入を待たずに数時間単位での微調整を可能にした点が革新的です。
生理学的意義:静脈容量というダイナミックな視点
心不全におけるうっ血の進行は、単純な水分過剰(ボリューム・オーバーロード)だけではありません。交感神経系の活性化や血管収縮因子の放出により、全身の静脈が収縮し、末梢にあった血液が中心静脈へとシフトすることでも生じます。IVCセンサーは、IVCの面積と、呼吸に伴う虚脱率(コラプシビリティ・インデックス)を連続的に測定します。
本論文で示されたデータによれば、IVCの面積が大きい、あるいは虚脱率が低い状態は、心臓への還流量が増大し、心不全増悪の直前状態にあることを示唆します。分子生物学的な視点で見れば、内皮細胞の機能不全やサイトカインの放出が静脈のコンプライアンスを低下させている状態を、物理的な直径の変化として捉えていると言えます。この生理学的な変化をリアルタイムで数値化(NORMTスコア)することで、体重計では決して捉えられない「目に見えないうっ血」を可視化したのです。
結果の衝撃:271%という驚異的な介入頻度の向上
本研究で得られた数値は、心不全診療における「臨床的惰性(クリニカル・イナーシャ)」の存在を浮き彫りにしました。
利尿剤の調整頻度において、自己管理グループは90日間で1人の患者あたり平均10.4回の調整を行ったのに対し、従来型の臨床医管理グループではわずか2.8回にとどまりました。これは、自己管理によって介入のチャンスが271%(相対リスク3.71、p値0.01未満)も向上したことを意味します。この圧倒的な頻度の差が、大きな増悪を未然に防ぐ「小さな微調整の積み重ね」を実現したのです。
また、安全性に関しても特筆すべき結果が出ています。自己管理によって利尿剤を頻繁に動かしたにもかかわらず、薬剤に関連する重篤な有害事象は1件も報告されませんでした。これは、医師が事前に設計した「安全柵」の中であれば、患者による調整が十分に安全であることを示しています。
臨床的アウトカム:入院回避とQOLの改善
介入頻度の向上は、目に見える形での臨床的利益をもたらしました。
心不全イベント発生率
90日間の追跡において、臨床医管理グループでは5件のイベント(0.33回/患者月)が発生したのに対し、自己管理グループではわずか1件(0.11回/患者月)でした。これは、イベント率にして70%の減少という強力なトレンドを示しています。サンプルサイズが限定的であるため、統計的な有意差を確定するには至りませんでしたが、その方向性は極めて明確です。
生活の質(QOL)
カンザスシティ心筋症質問票(KCCQ)の臨床サマリースコア(CSS)において、自己管理グループは13.9ポイントの改善を示し、臨床医管理グループの4.4ポイント改善を大きく上回りました。自分の体調を客観的な数値で把握し、自らコントロールできているという感覚(自己効力感)が、心理的な安定とQOLの向上に大きく寄与したものと考えられます。
デバイスへの適応
毎日の測定に対するアドヒアランス(遵守率)は、自己管理グループで90.5%と非常に高く、患者がこのシステムを積極的に受け入れ、生活の一部として活用していたことが分かります。
研究の限界と今後の課題
本研究の結果は非常に有望ですが、解釈には注意が必要です。
まず、総勢25名という小規模なサンプルサイズであり、かつランダム化されていない逐次コホートであるため、選択バイアスや学習曲線による影響を否定できません。
また、90日間という比較的短期間の評価であるため、長期的なアドヒアランスの維持や、繰り返される調整による腎機能への影響についてはさらなる検証が必要です。
さらに、このシステムを実臨床に導入するためには、初期のケアプラン作成にかかる医師の負担や、緊急時のバックアップ体制、そして保険償還モデルの構築といったハードルを越える必要があります。
現在は、より大規模なランダム化比較試験であるNORM-HF試験が計画されており、その結果が待たれるところです。
実践への提言:明日からの診療にどう活かすか
この論文から私たちが学べる最も重要な教訓は、心不全管理のパラダイムを「反応的(リアクティブ)」から「能動的(プロアクティブ)」に変えることの圧倒的な価値です。たとえ明日から全ての患者にIVCセンサーを埋め込むことができなくても、以下の視点を日々の診療に取り入れることができます。
第一に、患者の自己効力感を高める教育です。単に「体重が増えたら受診してください」と伝えるのではなく、どのような症状や変化が介入のサインなのかを事前に具体化し、患者自身が「管理の主体」であるという意識を持たせることが、アドヒアランス向上の鍵となります。
第二に、うっ血の生理学的な理解の深化です。末梢浮腫や体重増加が出る前に、静脈系の鬱滞が始まっていることを意識し、下大静脈エコーなどの非侵襲的な検査をより早期、かつ頻繁に活用することで、症状が出る前の微調整を目指すべきです。
第三に、デジタルツールの積極的な活用です。アプリやウェアラブルデバイスを通じて、患者と医療者が同じデータを共有し、リアルタイムに近いフィードバックループを回すことが、臨床的惰性を克服する唯一の道かもしれません。
IVCセンサーによる自己管理は、心不全という複雑な疾患に対して、患者自身が「守護者」となるための強力な武器を与えてくれました。この技術が標準治療となる日は、そう遠くないかもしれません。
参考文献
Uriel N, Mehra MR, Greene BR, Bhatt K, Kahwash R, Feitell S, Sayer G, Martyn T, Borme C, Sweeney F, Testani J, Fudim M, Physician-Directed Patient Self-Management Using an Implantable IVC Congestion Sensor: Insights from FUTURE HF II, JACC: Heart Failure (2026), doi: https://doi.org/10.1016/j.jchf.2026.103011.