はじめに
脂質異常症治療において、スタチンは心血管疾患リスクを劇的に低下させる「21世紀の特効薬」として君臨しています。現在、世界中で2億人以上の患者に処方されていますが、その輝かしい功績の影で、長年議論されてきたのがスタチン関連筋肉症状(SAMS)です。全服用者の10%から25%が、軽度の筋肉痛から致死的な横紋筋融解症に至るまで、何らかの筋肉トラブルを経験しています。これまでの研究で、骨格筋のカルシウム放出を司るリアノジン受容体1型(RyR1(Ryanodine Receptor 1 ))の遺伝子変異がスタチン不耐症と相関することは知られていましたが、スタチンがRyR1に直接結合し、その機能を操作しているのかという点については、決定的な証拠が欠けていました。
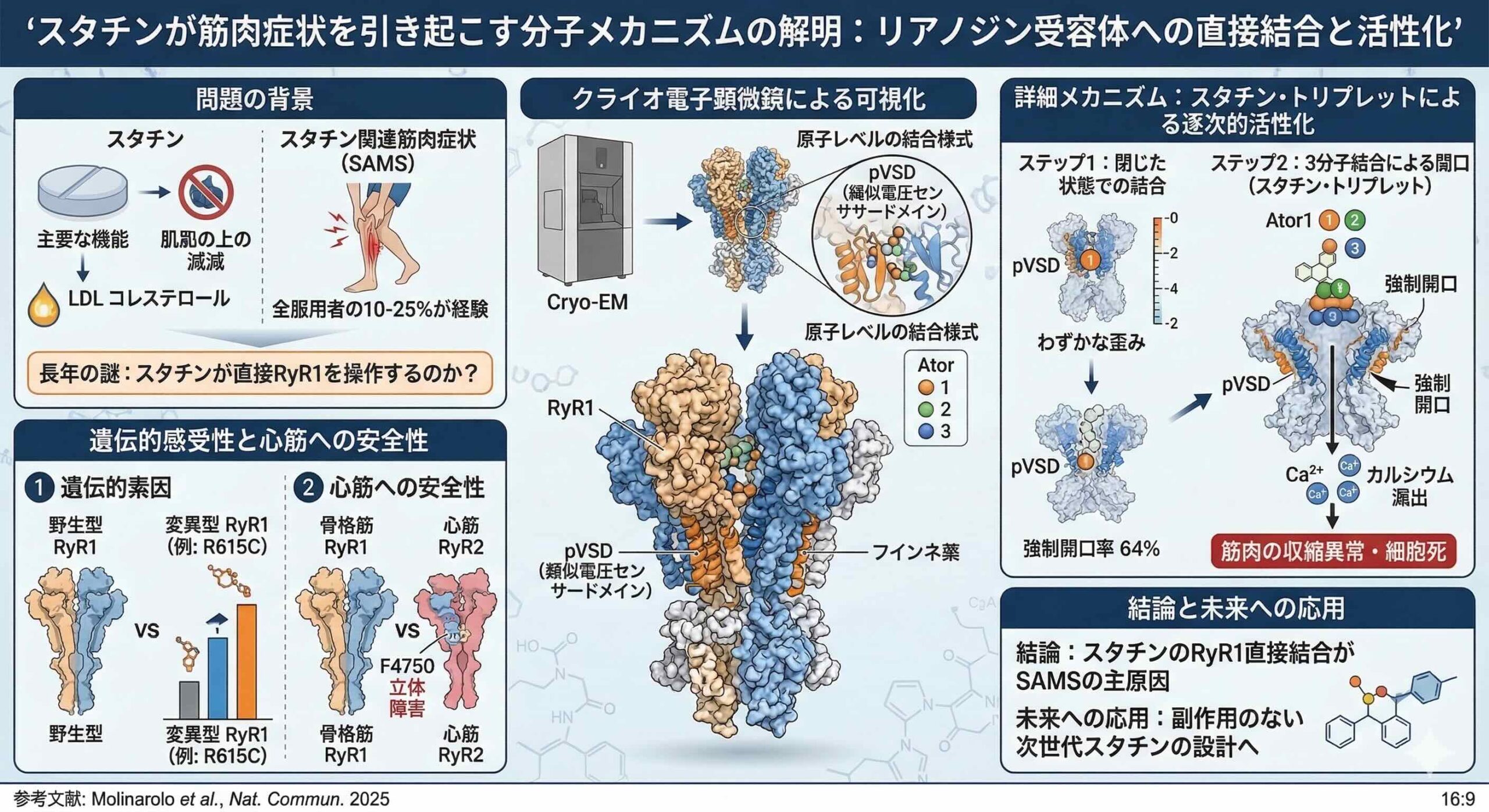
2025年にNature Communications誌に発表されたこの画期的な研究は、クライオ電子顕微鏡(cryo-EM)という最先端の視覚化技術を駆使し、アトルバスタチンがRyR1に直接結合し、それを異常に活性化させる姿を原子レベルで捉えました。そこには、1つの受容体ユニットに3つの薬剤分子が群がって結合するという、薬理学的に極めて異例かつ衝撃的な「三重奏」のメカニズムが隠されていたのです。
なお、RyR1は、細胞内のカルシウム貯蔵庫である小胞体(ER)および筋小胞体(SR)の膜に埋め込まれた巨大なイオンチャネルです 。骨格筋においては、筋小胞体の膜表面に局在し、筋肉の収縮を駆動するために貯蔵されているカルシウムイオンを細胞質へ放出する役割を担っています 。
本研究のPECO概要
この臨床的疑問を解明するために、研究チームは以下の実験的枠組みを設定しました。
P(対象):精製された野生型(ウサギ)RyR1、および悪性高熱症変異(R615C)を持つブタRyR1。
E(介入):アトルバスタチンの曝露(10 mM)。
C(比較):アトルバスタチンを含まないDMSO(ジメチルスルホキシド)コントロール(2%)。
O(結果):クライオ電子顕微鏡による単粒子解析で得られた開口・閉鎖状態の構造、および薬剤結合部位の特定。
既存研究を塗り替える圧倒的な新規性
これまでの研究は、筋組織を用いた生理学的実験や膜小胞を用いた記録にとどまっており、スタチンがRyR1に「直接」触れている物理的な証拠はありませんでした。本研究の新規性は、RyR1単体を用いた構造解析によって、薬剤とタンパク質の相互作用を原子レベルで可視化した点にあります。さらに、スタチンが単に結合するだけでなく、複数の分子が順次結合することで段階的にチャネルをこじ開ける「逐次的活性化モデル」を提唱したことは、既存のチャネル薬理学の常識を覆す発見です。
分子生物学的視点から見たスタチンの三重奏
研究チームが解明した結合様式は、驚異的なものでした。RyR1の1つのサブユニットに対し、合計3つのアトルバスタチン分子(Ator1、Ator2、Ator3)が結合します。
まず、チャネルが閉じている状態(Closed state)では、AtorCと呼ばれる1つのスタチン分子が、擬似電圧センサードメイン(pseudo-voltage-sensing domain;pVSD)とポア形成領域の間の裂け目に滑り込みます。この単分子の結合は、周辺のヘリックス(S4-S5リンカーなど)に約1.5 A(オングストローム)のわずかな歪みを生じさせ、受容体全体の構造を「開口しやすい状態」へとプライミング(予備活性化)させます。実際、アトルバスタチンが存在するだけで、細胞質側のキャップ構造が膜方向に2から3 Aも沈み込む様子が観察されています。
さらに活性化条件(Ca2+とカフェインの存在下)では、追加で2つのスタチン分子(Ator2、Ator3)が同じポケットに押し寄せます。AtorCは「チャネルが開く前の先発隊」であり、チャネルが開いた後はAtor1になります。これら3つの分子(Ator1、Ator2、Ator3)は、単にタンパク質と結合するだけでなく、薬剤分子同士が芳香族環のスタッキング作用(パイ電子相互作用)を通じて強固に連結し、一つの塊(トリプレット)として振る舞います。
この巨大なスタチン複合体がpVSD領域を内側から物理的に押し広げることで、電圧感受性チャネルのゲートが開くのと似たようなメカニズムでポアが強制開口されます。クライオ電子顕微鏡のデータでは、アトルバスタチン非存在下では全ての粒子が閉鎖状態であったのに対し、存在下では64%もの粒子が強制的に開口状態に移行していることが示されました。これは、本来厳密に制御されている筋肉内のカルシウムバランスが、薬剤によって直接的に破壊されることを意味しています。
遺伝的脆弱性が牙を剥くとき:R615C変異の解析
本研究のもう一つの焦点は、悪性高熱症(MH)の原因として知られるR615C変異体を用いた解析です。この変異を持つRyR1は、もともと閉鎖状態が不安定であり、わずかな刺激でカルシウムを放出する性質(gain-of-function)があります。アトルバスタチンをこの変異体に添加すると、閉鎖状態の粒子はわずか19%まで激減し、野生型よりもはるかに高い感度でチャネルが開口してしまうことが分かりました。
これは、RyR1にマイナーな変異を持つ潜在的なMH感受性者がスタチンを服用した場合、劇的なカルシウム漏出、すなわち激しい筋痛や横紋筋融解症へと直結するリスクが高いことを科学的に裏付けています。まさに、個人の遺伝的背景が薬剤副作用の重症度を決定する精密医療の典型例と言えます。
補足:もっと易しく説明
ここまでの説明は、専門用語も多く難しいですね。少し平易な表現で振り返ります。
最新技術で見えた「筋肉のスイッチ」へのいたずら
研究チームは、クライオ電子顕微鏡という、分子を原子レベルで観察できる非常に強力な顕微鏡を使用しました 。この顕微鏡で筋肉の細胞を詳しく調べたところ、スタチンが本来の目的とは異なる場所に迷い込み、勝手にスイッチを押していることがわかりました。
ターゲットにされた「リアノジン受容体」
その「間違った場所」とは、筋肉の細胞内にあるリアノジン受容体(RyR1)という、カルシウムの出口(門)です 。
- 通常、この門は必要なときだけ開き、中からカルシウムを出すことで筋肉を動かします 。
- ところが、スタチンがこの門に直接くっついてしまうことが判明しました 。
3人組で力ずくで扉をこじ開ける「スタチン・トリプレット」
今回の発見で最も驚くべき点は、スタチンが1つではなく、3つセット(トリプレット)になって門をこじ開けていたことです 。
- 準備のステップ: まず、スタチンが1つだけ門の特定の場所にくっつきます 。これだけで門の形が少し歪み、開きやすい「準備状態」になります 。
- こじ開けのステップ: さらに2つのスタチンが合流して、合計3つの分子がひと塊になります 。
- カルシウムの漏出: この「3人組」が力ずくで門を押し広げることで、門が強制的に開かれ、中のカルシウムがダラダラと漏れ出してしまいます 。
この「カルシウムの漏れ」が続くことで、筋肉が休まる暇がなくなり、痛みや細胞のダメージを引き起こす原因になるのです 。
体質によって痛みの出方が違う理由
人によってはスタチンを飲んでも全く平気な人もいれば、すぐに痛くなる人もいます。この違いも今回の研究で説明がつきました。
- もともと「リアノジン受容体(門)」の形が少し緩い、あるいは開きやすいという遺伝的な特徴(変異)を持っている人がいます 。
- そうした特徴を持つ人の場合、スタチンの「こじ開ける力」に対してより弱く、通常の数倍も門が開いてしまいやすくなります 。
- 一方で、心臓にある受容体(RyR2)は形が少し違うため、スタチンがうまく入り込めず、心臓への影響は出にくいという安全な仕組みも確認されました 。
なぜ心臓には影響が出にくいのか
多くの読者が抱く疑問は「なぜこれほどRyR1を活性化するなら、心筋のRyR2には影響が出ないのか」という点でしょう。研究チームはこの点も鮮やかに解明しました。RyR1とRyR2の構造を比較すると、スタチンの結合ポケットにある4820番目のバリン(V4820)が、RyR2ではフェニルアラニン(F4750)に置換されています。フェニルアラニンの大きな側鎖はスタチン分子と立体障害を起こすため、RyR2にはスタチンが結合しにくいのです。このわずかなアミノ酸1つの違いが、心毒性を回避しつつ筋毒性を生むという皮理的な選択性を生み出しています。
明日から活かせる臨床的実践と洞察
この論文から得られる知見は、明日の診療や健康管理に直結します。
まず、スタチンによる筋肉痛を単なる「副作用」として片付けるのではなく、RyR1の潜在的な脆弱性の兆候として捉え直す必要があります。特に、スタチン服用後にクレアチンキナーゼ(CK)が上昇する患者や、激しい筋痛を訴える患者については、RyR1に関連する遺伝的素因を考慮に入れるべきです。
実践的なアドバイスとしては、スタチン不耐症が疑われる場合、薬剤の種類を変更するだけでなく、スタチンがRyR1を直接活性化するというメカニズムを念頭に置き、運動療法とのタイミングを慎重に検討することが挙げられます。激しい運動はRyR1のカルシウム放出を促進するため、スタチンの作用と相乗的に働いてダメージを加速させる可能性があります。
筋肉痛が出現した際には、一時的な休薬や低用量への変更、あるいは水溶性スタチンへの切り替えが有効な場合がありますが、その背後にはこのような構造生物学的な「暴走」があることを理解しておくことが重要です。
さらに、今後の創薬において「RyR1に結合しないスタチン」のデザインが可能になります。スタチンのジヒドロキシヘプタン酸部分はコレステロール低下に必須ですが、RyR1との結合には疎水的な芳香族部分が主に関与しています。この疎水性部位を修飾し、RyR1との立体障害を生むような構造に変えることで、筋肉痛を起こさない次世代の脂質改善薬の開発が期待されます。
補足:水溶性スタチン・脂溶性スタチン
水溶性スタチンとは、化学的な性質として水に溶けやすい性質(親水性)を持つスタチンの総称です。
この論文の文脈と一般的な医療知識を照らし合わせると、以下の点が重要となります。
脂溶性スタチンとの違い
スタチンには、大きく分けて脂溶性(油に溶けやすい)と水溶性(水に溶けやすい)の2種類があります。
- 脂溶性スタチン: アトルバスタチン(本論文で使用)、シンバスタチン など。細胞膜(脂質の二重層)を通り抜けやすく、肝臓以外の筋肉などの組織にも入り込みやすい性質があります。
- 水溶性スタチン: プラバスタチン、ロスバスタチン など。主に肝臓の細胞にある輸送体(トランスポーター)を通って取り込まれるため、肝臓への選択性が高く、他の組織には入りにくいとされています。
リアノジン受容体(RyR1)との関わり
本論文では、アトルバスタチンがRyR1に直接結合してカルシウム漏出を引き起こすメカニズムが詳細に示されています。
- アトルバスタチンは、その疎水的な(油になじみやすい)部分を使ってRyR1の深いポケットに入り込み、結合します。
- 論文内では、プラバスタチンのような水溶性スタチンは、アトルバスタチンとは疎水的な部分の構造が大きく異なると指摘されています。
- そのため、水溶性スタチンが脂溶性スタチンと全く同じようにRyR1に強く結合し、同様のメカニズムでチャネルをこじ開けるかどうかについては、現時点では不明確(さらなる検証が必要)とされています。
臨床的な意義
一般的に、水溶性スタチンは脂溶性スタチンに比べて筋肉への副作用(SAMS)が少ない可能性が議論されてきました。この論文の発見は、その理由の一端として「RyR1への直接結合のしやすさ(親和性)」の違いが関与している可能性を示唆しています。
論文の結論としては、スタチンの構造のうち、RyR1との結合に関わる「疎水的な部分」を改良することで、筋肉への副作用を抑えた次世代のスタチンを開発できる可能性があると述べられています。
本研究の限界(Limitation)
本研究にはいくつかの制約もあります。
第一に、構造解析のために10 mMという非常に高い濃度のアトルバスタチンを使用している点です。実際の血漿中濃度は高用量投与時でも約334 nM程度であり、in vitroの飽和条件がそのまま生体内の現象を100%反映しているとは限りません。ただし、スタチンのRyR1に対するEC50値は300から400 nMと報告されており、臨床的な関連性は極めて高いと考えられます。
第二に、解析対象が精製タンパク質であるため、実際の筋細胞内にある他の調節因子(FKBP12やカルモジュリンなど)との相互作用が完全に再現されているわけではありません。また、アトルバスタチン以外のスタチン(シンバスタチンやプラバスタチンなど)が同様の「三重奏」結合を行うかどうかは、今後の解析を待つ必要があります。
結論
スタチンによる筋肉痛は、薬剤が意図せずRyR1という巨大なカルシウムチャネルのスイッチを物理的に押し広げてしまうことで引き起こされていました。本研究が示した「スタチン・トリプレット」による逐次的活性化は、分子薬理学における新たな知見であると同時に、副作用に苦しむ数百万の人々に対する救済のロードマップでもあります。薬剤の「正の作用」と「負の作用」が原子1つの配置によって分かたれているという事実は、現代医学の精密さと、さらなる改良の余地を私たちに教えてくれます。
参考文献
Steven Molinarolo, Carmen R. Valdivia, Héctor H. Valdivia & Filip Van Petegem. Cryo-electron microscopy reveals sequential binding and activation of Ryanodine Receptors by statin triplets. Nature Communications. 2025;16:11508. https://doi.org/10.1038/s41467-025-66522-0
おまけ:スタチンで筋症状が出るメカニズム
筋肉が正常に動くためには、細胞内のカルシウムイオン濃度の精密な制御が不可欠です。通常、リアノジン受容体1型(RyR1)は、必要な時にだけ一瞬開いてカルシウムを放出し、すぐに閉じます。しかし、本論文が明らかにしたのは、アトルバスタチンがこの門を物理的にこじ開け、閉まらなくさせてしまうという衝撃的な事実です 。
この現象がなぜ痛みや破壊を招くのか説明します。
1. 物理的な強制開口と持続的な漏出
先述のように、アトルバスタチンは、1つのユニットに対して3つの分子がトリプレット(3つ組)として結合します 。この3分子の塊が、受容体の擬似電圧センサードメイン(pVSD)を内側から物理的に押し広げることで、本来は閉じているはずのチャネルを強制的に開口状態へと移行させます 。
実験データでは、アトルバスタチンが存在する環境下では、RyR1粒子の約64%ものチャネルが開口状態に固定されていることが示されました 。これにより、筋小胞体(カルシウムの貯蔵庫)から細胞質内へと、カルシウムイオンが制御不能な状態でダラダラと漏れ続ける「リーク(漏出)」が発生します 。
2. エネルギー(ATP)の枯渇と死の硬直
細胞内に漏れ出したカルシウムイオンを元の貯蔵庫に戻すためには、筋小胞体・小胞体カルシウムATPase(Sarco/Endoplasmic Reticulum Ca2+-ATPase;SERCA)と呼ばれるポンプが大量のエネルギー(ATP)を消費して働かなければなりません。
RyR1が強制的に開かれ、カルシウムが漏れ続ける状態は、いわば「穴の空いたバケツで水を汲み続けている」ようなものです。細胞はこのカルシウムを回収しようとしてATPを使い果たし、最終的にエネルギー枯渇に陥ります。
エネルギーがなくなると、筋肉を緩めるための動作ができなくなり、持続的な筋収縮や硬直が起こります。これが臨床的に観察される筋肉のだるさや、重度の場合は横紋筋融解症の初期段階である筋肉の強張りに繋がります。
3. 細胞内の構造破壊と酵素の暴走
さらに深刻なのは、高濃度のカルシウムイオンが細胞内に留まることで、細胞を維持するための部品が破壊されるプロセスです。
細胞内には、カルシウム濃度が高くなると活性化するタンパク質分解酵素(カルパインなど)が存在します。通常はこれらが細胞の修復を助けますが、慢性的な漏出によってこの酵素が暴走すると、自分自身の筋肉の繊維を溶かし始めてしまいます。
本論文でも、スタチンによる副作用が、血中のクレアチンキナーゼ(CK)の上昇という形で現れることが指摘されています 。これは、細胞膜が維持できなくなり、細胞の中身が外へ漏れ出している、つまり細胞が死滅・破壊されていることの直接的な証拠です。
4. 痛みを感じさせる炎症反応の惹起
細胞が壊れる過程で、ミトコンドリアもダメージを受け、活性酸素などの有害物質が放出されます。また、壊れた細胞からは炎症を引き起こす物質が放出され、周囲の痛覚神経を強く刺激します。これが、患者さんが訴える筋肉痛や倦怠感の実体です。
特に、悪性高熱症変異(R615C)などを持つ患者さんでは、このプロセスがより劇的に進行します。変異型の受容体はもともと閉鎖状態が不安定であるため、スタチンによる開口率が野生型よりも大幅に上昇し、カルシウム漏出の規模が格段に大きくなるためです 。