JAMA誌において心房細動関連のレビューが2024年12月だけで2回目となります。それだけ関心の大きいテーマなのでしょう。確かに、心房細動(Atrial Fibrillation, AF)は世界中で最も一般的な持続性不整脈の一つであり、その罹患率と関連する健康被害の深刻さから、医学的研究の主要な焦点となっています。ここでは、JAMA誌のレビュー、最新の研究結果と臨床ガイドラインをもとに、AFの疫学、病態生理、診断、治療に関し解説します。
1. 疫学とリスク因子
AFの有病率は増加の一途をたどっています。米国では2019年時点で1,055万人がAFを患っていると推定されており、これは全人口の約3人に1人が生涯のいずれかの時点で罹患する計算になります。この増加は主に人口の高齢化や高血圧、糖尿病などの関連疾患の増加、そして診断技術の進歩によるものです。世界的にも、2021年には5,255万人がAFまたは心房粗動を抱えていると報告され、高所得国で特に高い有病率が確認されています。
主要なリスク因子として、加齢(5歳ごとにAF発症リスクが66%上昇)、高血圧、肥満、喫煙、糖尿病、および心疾患(例:心不全、心筋梗塞)が挙げられます。特に肥満は、酸化ストレスや慢性炎症、異常なカルシウムイオン循環を引き起こし、心房の異常電気活動を誘発することでAFの発症に寄与するとされています。また、適度な身体活動がAFリスクを低下させる一方で、男性の持久力系アスリートでは逆にリスクが増加することが示されています。
2. 病態生理:分子メカニズムの解明
AFの発症は、主に肺静脈と左心房の接合部で発生する異所性心房性早期興奮によって引き起こされます。その持続には、心房の電気的および構造的リモデリングが重要な役割を果たします。
- 電気的リモデリング:高血圧がレニン-アンジオテンシン-アルドステロン系を活性化し、心房線維化と肥大を引き起こします。これにより伝導遅延とリエントリー回路形成が促進されます。
- 構造的リモデリング:肥満や高血圧が引き起こす慢性的なストレスは、心房の線維化や細胞外マトリクスの異常沈着を助長します。また、酸化ストレスによりカルシウムイオンチャネルが変異し、心房の興奮性が高まります。
これらのプロセスは、心房の再分極異常や異常な細胞間電気的伝導性をもたらし、持続的なAFを維持する病態基盤を形成します。さらに、肥満では脂肪組織から放出されるアディポサイトカインが炎症を誘発し、心房の病態変化に寄与するとされています。
3. 診断と分類
AFは、無症候性から高度な症候性まで幅広い臨床像を呈します。典型的な症状には動悸、息切れ、胸痛、前失神、運動不耐性、疲労感が挙げられますが、約10%から40%の患者は無症状です。このため、心電図(ECG)やウェアラブルデバイスを活用した早期発見が推奨されます。
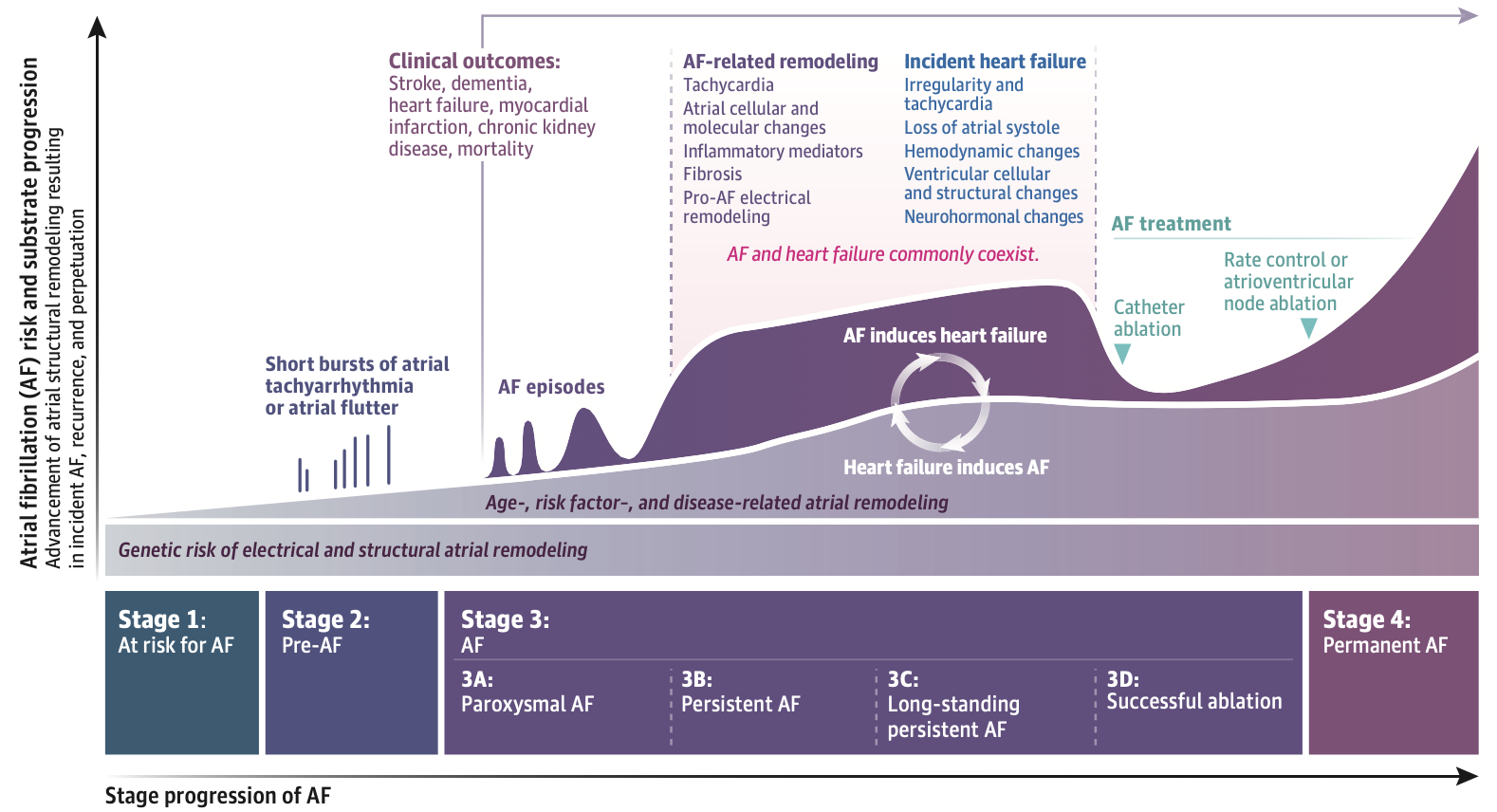
2023年のACC/AHA/ACCP/HRSガイドラインでは、AFを以下の4つの段階に分類しています:
- At risk for AF(Stage 1):肥満や高血圧などの危険因子を有する状態。
- pre-AF(Stage 2):心房拡大や頻繁な心房性不整脈が認められるが、AF診断には至らない段階。
- Clinically diagnosed AF(Stage 3):臨床的に診断された再発性または持続性AF。
3a Paroximal AF:一過性心房細動(≦7日)
3b Persistent AF:持続性心房細動(>7日)
3c Long-standing Persistent AF:長期持続性心房細動(>1年)
3d Successfull Ablation:AFだったがアブレーション治療済み - permanent AF(Stage 4):永続性。リズム制御を行わないと決定された持続性のAF。
また、AFの診断にはCHA2DS2-VAScスコアなどのリスクスコアリングが役立ちます。このスコアリングにより脳卒中リスクを評価し、適切な治療を計画することが可能です。
4. 治療戦略
4.1 ライフスタイルとリスク因子の修正
ライフスタイル改善は、AF発症の予防と進行抑制の両面で極めて重要です。
- 体重減少:体重の10%以上の減少はAFの再発リスクを顕著に低下させる。
- 適度な運動:週210分以上の運動が推奨され、機能的能力と生活の質が向上する。
- 飲酒制限:節酒または禁酒がリズム制御の成功率を高める。
4.2 抗凝固療法
AF患者の年間脳卒中リスクが2%以上であれば、経口抗凝固薬(OAC)の投与が推奨されます。CHA2DS2-VAScスコアに基づき、適切な患者を選定します。直接経口抗凝固薬(DOAC)は、ワルファリンよりも出血リスクが低く、脳内出血リスクを半減させることが示されています。
4.3 リズム制御とレート制御
- リズム制御:抗不整脈薬(AAD)またはカテーテルアブレーションにより、洞調律を回復・維持します。早期リズム制御が心不全、脳卒中リスク、死亡率を低下させるとのデータがあります。
- レート制御:心拍数を減少させる——β遮断薬や非ジヒドロピリジン系カルシウム拮抗薬(例:ベラパミル、ジルチアゼム)を使用。
4.4 カテーテルアブレーション
肺静脈隔離術は、特に症候性再発性AFの患者において第一選択肢とされています。ランダム化試験により、アブレーションを受けた患者の約77%が1年後もAFが発生しないことが示されました。この手技は、心房の異常電気活動を遮断し、再発リスクを低下させることで知られています。
5. AFと併存疾患:心不全および認知症の関連
AFは心不全(HF)と双方向的に関連しています。AFは心拍出量低下や心室リモデリングを引き起こし、HFのリスクを高めます。一方、HFは心房線維化や電気的異常を誘発し、AFのリスクを増加させます。
また、AFは認知症、特にアルツハイマー型認知症および血管性認知症のリスクを1.4倍–1.7倍に増加させることが報告されています。慢性的な低灌流や微小脳卒中の寄与が示唆されており、これが記憶障害や認知機能低下に結びつく可能性があります。
結論
心房細動は、現代の循環器医学において最も重要な課題の一つです。ライフスタイル改善とリスク因子の管理が発症予防および進行抑制の要であり、抗凝固療法や早期リズム制御の重要性も強調されます。さらに、カテーテルアブレーションなどの先進的治療法が、患者の症状改善と生命予後向上に寄与しています。
参考文献
Ko D, Chung MK, Evans PT, Benjamin EJ, Helm RH. Atrial Fibrillation: A Review. JAMA. Published online December 16, 2024. doi:10.1001/jama.2024.22451