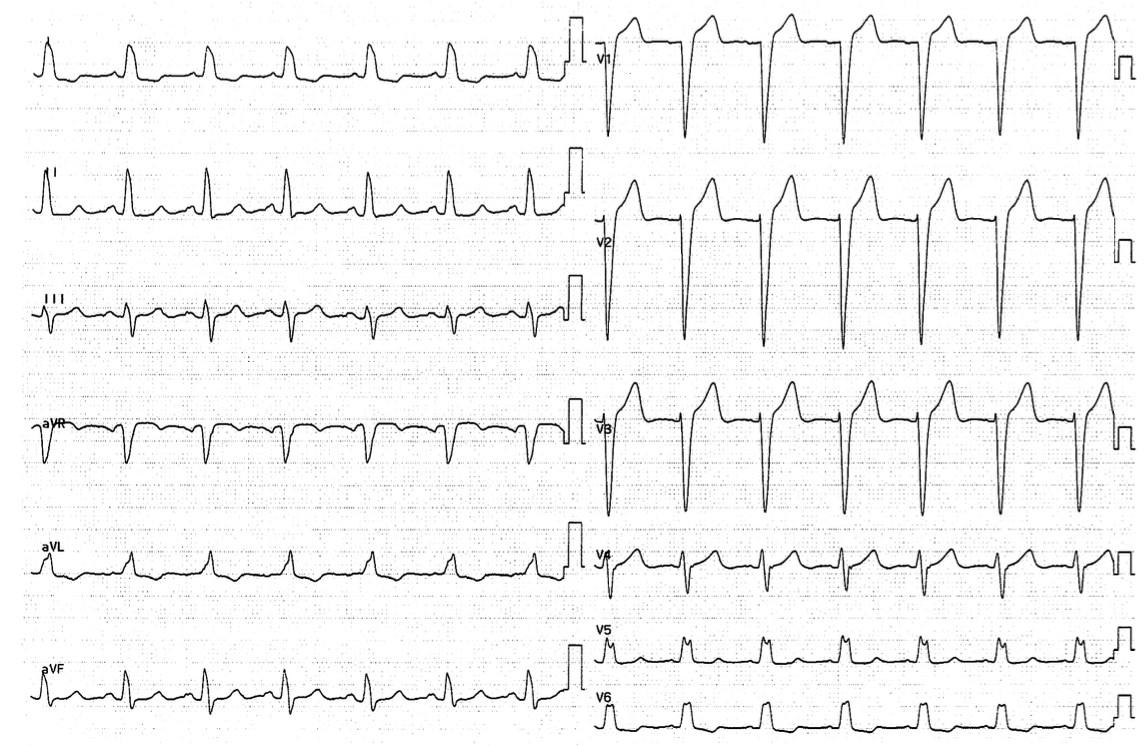
なぜ左脚ブロック(LBBB)が問題か
LBBBは心不全(HF)と低左室駆出率(LVEF)を有する患者で死亡率上昇と結びつき、再同期療法(CRT)が有効であることはよく知られています。一方で、無症候の地域在住者で偶発的に見つかるLBBBが、その後のHF発症や左室機能低下にどう関わるかは十分に分かっていませんでした。本研究は、構造的心疾患を画像で除外した集団で、LBBBが将来のHFリスクと関連するかを問うものです。背景として、LBBBは機械的不同期を介して左室壁応力の増大、偏心性肥大、拡大へ至る可能性が示唆されていました。
研究の新規性と目的
先行研究の多くはICD-9コードへの依存、横断解析、あるいは限定的な追跡時点に留まっていました。本研究はベースライン心エコーで「正常LVEF」を保証したうえで、詳細表現型の地域在住高齢者を縦断追跡した点が大きな新規性です。目的は、LBBBがHF発症、5年後のLVEF低下、HFrEF/HFpEF入院、死亡と関連するかを検証することでした。
研究デザインと対象
Cardiovascular Health Study(CHS)から抽出した前向きコホートで、1989~2013年のデータを用いました。登録時に65歳以上、HF既往なし、LVEF正常を満たす4,541例が解析対象です(平均年齢72.6歳、女性59.4%)。ベースラインLBBBは44例(1.0%)でした。
暴露は12誘導心電図で確認したLBBB(Minnesota Code、コア施設で再読)。アウトカムはHF発症、HFrEF/HFpEF入院、5年後のLVEF低下、死亡です。LVEFはベースラインで正常(≥55%)、境界(45–<55%)、異常(<45%)に分類し、5年エコーでも同一プロトコルで判定しました(読影再現性:読者間94%、読者内98%)。
ベースライン特性では、LBBB群と非LBBB群はそれぞれ、高血圧72.1% vs 55.6%、糖尿病25.0% vs 13.7%、左室質量指数94.6 vs 83.6 g/m²と、LBBB群で負荷が高い傾向でした。
統計解析の要点
HF発症・入院・死亡はCox比例ハザード(非死亡アウトカムは死亡を競合事象として打ち切り)で推定し、5年LVEF低下はロジスティック回帰を用いました。感度解析としてFine–Grayモデル(競合リスク)および左室質量指数での追加調整を実施し、両側P<.05を有意としました(解析期間:2018年2月~2024年10月)。
結果
主要アウトカム:心不全発症
追跡中央値14.6年で、LBBBあり21/44例(47.7%)、なし1,300/4,497例(28.9%)がHFを発症しました。未調整累積リスクはLBBBあり48.6%、なし12.2%。
共変量調整後、LBBBはHF発症リスクを約5倍に上昇させました(HR 4.98、95%CI 2.18–11.39、P<.001)。Fine–Grayモデル(HR 3.07、95%CI 1.33–7.10)や左室質量指数での追加調整後(HR 4.99、95%CI 1.80–13.79)でも結果は頑健でした。
さらに、LBBBのHRは高血圧(HR 1.67)、冠動脈疾患(HR 1.50)など既知の因子より大きく、臨床的重要性が際立ちます。
サブアウトカム:入院、LVEF低下、死亡
入院イベントでは、HFrEF 336件、HFpEF 566件でした。LBBBはHFrEF入院リスクの上昇と関連(調整後HR 5.98、95%CI 1.43–25.00、P=.01)しましたが、HFpEFでは有意差がありませんでした(HR 3.10、95%CI 0.76–12.67、P=.12)。入院時にLVEFが低下していた割合も、LBBB群で高い傾向でした(78.6% vs 54.6%)。
5年エコーが得られた3,020例のうち、253例(8.4%)でLVEF低下を認め、ベースラインLBBBは低下のオッズ上昇と関連しました(OR 4.73、95%CI 1.70–13.70、P=.003)。
死亡については、粗ハザードでHR 1.75でしたが、調整後はHR 1.39(95%CI 0.99–1.94、P=.05)となり統計学的有意性は失われました。
病態生理(組織・細胞レベル)
LBBBは室内伝導障害により、隔壁→側壁の順に遅れて収縮する不同期を生み、収縮効率の低下とリモデリング、拡大、収縮能低下を招きます。動物モデルでは、LBBB誘発心筋症に内膜・心筋の著明な線維化、脂肪変性、空胞化、さらにはプルキンエ線維内の線維化といった組織学的変化が報告されています。CRT(両室ペーシングや左脚領域ペーシング)により収縮不全が可逆的となる事実は、LBBB自体が心筋症の原因となりうることを支持します。
既存知見との比較と本研究の新規性
本研究は、(1)ベースライン心エコーで「正常LVEF」を担保し、(2)詳細に表現型付けされた地域在住高齢者を長期追跡し、(3)死亡を競合リスクとして扱う因果特異的CoxやFine–Grayを用いた堅牢な解析を実施した点が既存研究と一線を画します。ICDコード依存や横断解析に留まった先行研究と比べ、方法論的に格段に強固であり、LBBBとHF発症の関連の大きさ(調整HR 4.98)が、他の確立した危険因子よりも顕著である点も注目すべき知見です。
明日からできること
無症候で構造的心疾患の証拠がないLBBBであっても、将来の収縮不全型HF(HFrEF)への進展リスクは高く、体系的な監視の導入を検討する価値があります。具体的には、定期的なプロトコール化されたフォロー(例:経時的心エコー)に加え、ナトリウム利尿ペプチドの縦断測定による早期の機能低下の検出が提案されています。また、現行ガイドラインに沿った危険因子(高血圧、喫煙など)の厳格な管理に加え、適格例ではACE阻害薬・ARB・β遮断薬の投与を考慮することが示唆されています。ステージA/B HFの枠組みへのLBBBの位置づけを検討することも、実務上の指針整備につながります。これらはLBBBがHFの「原因」か「マーカー」かを問わず有用な介入方針です。
現場での実践ポイントとしては、①偶発的LBBBを見つけた高齢患者に対し「放置」ではなく、フォロー計画(画像とバイオマーカー)を明確化する、②HFrEF予防の観点から血圧・代謝・虚血の修飾可能因子を積極的に是正する、③入院HFの表現型がHFrEFに偏ることを念頭に、労作時息切れや易疲労など微細な症状の早期拾い上げを徹底する、といったアクションが挙げられます。
Limitation
一般化可能性の制限(高齢・白人が主体)、長期追跡に伴う診断・治療パラダイムの時代差の影響、LBBBが潜在的心筋症の初期像である可能性、ベースライン時点でのみLBBBを評価したこと(時変暴露でない)、LBBB症例数の少なさによる検出力の制限、観察研究ゆえの残余交絡—といった限界が明確に述べられています。
まとめ
ベースラインで構造的心疾患が否定された高齢者コホートにおいて、LBBBはHF発症(HR 4.98)と5年後のLVEF低下(OR 4.73)に有意に関連し、入院イベントではHFrEFに偏っていました。死亡リスクは調整後で境界有意にとどまりました。機械的不同期と組織学的傷害(線維化・脂肪変性・空胞化)という病態モデル、そしてCRTによる可逆性は、LBBBが単なる合併所見ではなく、心機能低下の駆動因子になりうることを示唆します。無症候LBBBを「見つけたら終わり」ではなく、「ここから始める」監視・一次予防の入口と捉える視座が、明日からの診療を変えます。
参考文献
Thein AS, Dixit S, Soliman EZ, Heckbert SR, Psaty BM, Gottdiener J, Marcus GM. Left Bundle Branch Block as a Risk Factor for Heart Failure. JAMA Network Open. 2025;8(8):e2525801. doi:10.1001/jamanetworkopen.2025.25801.