はじめに
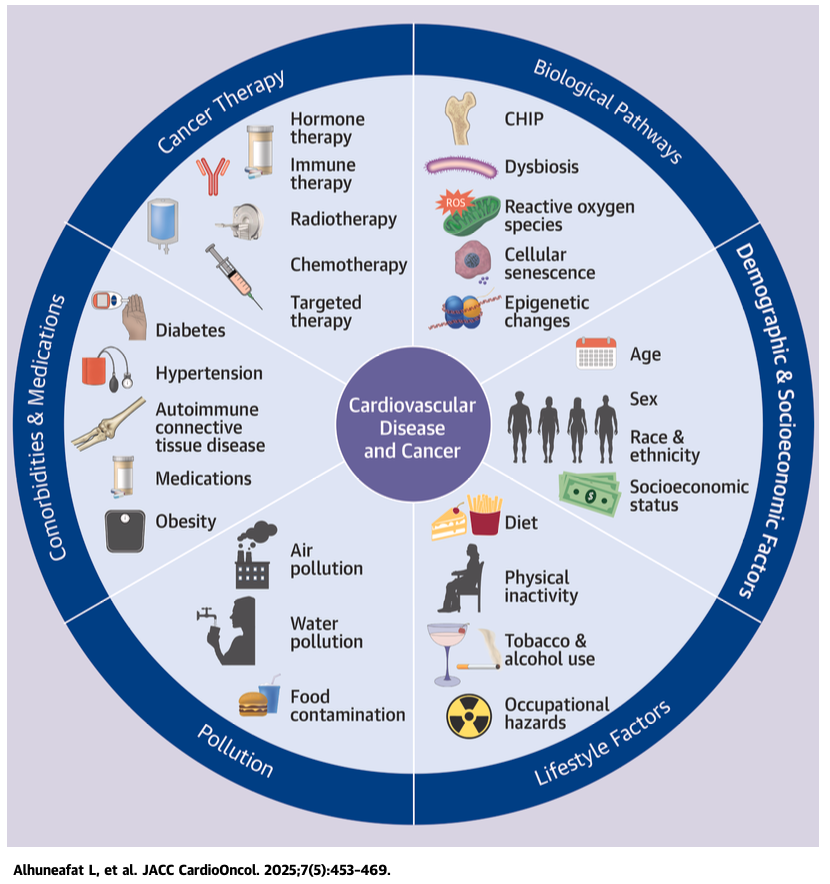
がんと心血管疾患(CVD)は、世界的な死亡の半分以上を占める二大疾患です。かつては別々の領域で論じられてきましたが、近年の知見は両者が深く絡み合い、互いに進展を促す「双方向的関係」を持つことを示しています。加齢、喫煙、肥満、糖尿病といった共有される生活習慣因子だけでなく、炎症や酸化ストレス、クローン性造血(Clonal hematopoiesis of indeterminate potential:CHIP)、腸内細菌叢異常といった分子機序も共通基盤として存在します。本稿では、最新のエビデンスをもとに、その複雑な連関を解説し、臨床・生活の両面で活かせる視点を提示します。
疫学的重なりと二重の負担
2022年には世界の新規がん症例は約2000万件、死亡は970万件に達しました。一方、米国には1800万人を超えるがん生存者が存在します。がん治療の進歩により生存は延長していますが、その陰で心血管死が大きな課題となっています。固形がん生存者では、非がん死のうち49%がCVDによるものでした。
(→固形がん生存者全体では、がん死が最多(おおむね 60〜70% 程度?)で、CVD死10〜15%くらい、非がん死の中ではCVD死が最多(49%)という感じが目安です)
さらに、がんとCVDの併存は予後を大きく悪化させます。がん生存者の5年生存率はCVDなしで87%に対し、CVD合併例では75%に低下します。小児がん生存者はさらに脆弱で、生涯にわたり心不全リスクが15倍、心臓死リスクが7倍に達します。
逆に、心血管疾患を持つ患者は、将来的にがんに罹患するリスクが高いことも判明しています 。具体的な数字を挙げると、心不全と診断された患者は、そうでない人と比べてがんの発症リスクが1.43倍に増加するというメタアナリシス結果があります 。また、心房細動を持つ男性では、がんのリスクが1.41倍に上昇することも報告されています
これらの数字は、両疾患が単なる偶然を超えた、生物学的な必然性によって結ばれていることを強く示唆しています。
共通リスク因子:生活習慣から代謝疾患まで
加齢と社会的要因
米国におけるCVD有病率は40〜59歳で40%、60〜79歳で75%、80歳以上では86%に達します。同様にがんの60%は65歳以上に集中します。加齢は単なる時間の経過ではなく、細胞老化、ミトコンドリア機能不全、エピジェネティクス異常、テロメア短縮といった分子老化の積み重ねです。これらは炎症性環境を形成し、両疾患を促進します。
また、人種差や社会的脆弱性も無視できません。米国の黒人やアメリカ先住民では、CVD・がん死亡率が白人の2倍に達し、居住環境や社会的資源の不足が背景にあることが示されています。
高血圧
高血圧はCVDの主因であると同時に、腎がん(RR 1.52)、大腸がん(RR 1.30)、乳がん(RR 1.10)のリスクを高めます。血圧上昇に伴うアンジオテンシンII過剰は、血管新生やアポトーシス異常を介して発がん性に寄与すると考えられています。
糖尿病
糖尿病患者は肝がん(RR 2.23)、膵がん(RR 2.09)、大腸がん(RR 1.27)など幅広い部位でがんリスクが上昇します。高インスリン血症や慢性高血糖によるIGFシグナル活性化、炎症・酸化ストレスが共通病態です。特筆すべきはメトホルミンで、インスリン経路抑制を介してがん発症を抑える可能性が報告されています。また、SGLT2阻害薬にも心血管・抗腫瘍の二重効果が期待されています。
肥満
肥満はCVDにもがんにも強力なリスク因子です。BMIが5上昇するごとに、心不全や冠動脈疾患のリスクは1.3〜1.5倍に増加します。がんでは全発症の20%が肥満関連と推定され、脳・腎・大腸・肝・卵巣がんなどの発症率が高まります。脂肪組織の炎症化、IL-6やレプチン上昇がその背景です。注目すべきはGLP-1受容体作動薬で、膵がん(HR 0.41)、大腸がん(HR 0.54)、肝細胞がん(HR 0.47)など肥満関連がんのリスク低減が確認されています。
脂質異常症
LDLコレステロールはCVDの主要因ですが、大腸がんや乳がんリスクとの関連も報告されています。スタチンは抗炎症作用を通じてがん抑制の可能性が示唆されるものの、確証は不十分です。PCSK9阻害薬は腫瘍アポトーシス促進やCD8+T細胞免疫強化による抗腫瘍作用が前臨床で観察されており、新しい二重予防の可能性を秘めています。
生活習慣・環境要因
喫煙
喫煙はCVDリスクを63%高め、米国におけるがん死亡の30%を占めます。1日1本の喫煙でも冠動脈疾患リスクが男性で1.4倍、女性で1.5倍上昇します。禁煙すればCVDリスクは25年以内に正常化し、肺がんリスクは10年で半減します。
食事
地中海食は全死亡リスクを28%、非致死性心筋梗塞リスクを52%減少させます。また、がん死亡率を13%低下させます。加工肉や糖質飲料は逆にCVDと大腸がんを増加させます。
アルコール
アルコールは30g/日以上でがん発症リスクを34%増加させ、心血管イベントも悪化させます。
身体活動
週150分の中強度運動は、CVD発症を17%、心血管死亡を23%減少させます。大腸癌患者では、術後運動プログラムにより無病生存率が28%、全生存率が37%改善しました。
PM2.5
さらに、大気汚染のような環境要因も共通のリスクです。特に有害なPM2.5(微小粒子状物質)は、濃度が10µg/m³上昇するごとに心血管死亡率を最大45%も増加させると報告されています 。肺がんリスクも増大させます。微小粒子やマイクロプラスチックによる慢性炎症と酸化ストレスが原因と考えられています。
分子機序の共通基盤
慢性炎症
NLRP3インフラマソームによるIL-1β・IL-6産生は動脈硬化と発がんを結びつけます。CANTOS試験では抗IL-1β抗体カナキヌマブが心血管イベントを減らすと同時に肺がん発症・死亡も減少しました。
酸化ストレス
ROSはDNA損傷、ミトコンドリア障害、脂質過酸化を引き起こし、動脈硬化やがんのゲノム不安定性を促進します。がん細胞はNrf2経路を利用しROSを「ちょうどよい」レベルに調節して腫瘍進展を助ける点が特徴的です。
エピジェネティクスとncRNA
DNAメチル化異常やヒストン修飾は、がんでは腫瘍抑制遺伝子のサイレンシング、CVDでは血管リモデリングを引き起こします。miRNAの異常発現も心筋線維化や不整脈、がん進展に関与し、新たな治療標的として注目されています。
細胞老化とテロメア短縮
細胞老化に伴う炎症性分泌表現型(IL-6、IL-8分泌)はがん微小環境と動脈硬化を悪化させます。がん細胞は逆にテロメラーゼを再活性化して無限増殖を獲得します。
クローン性造血(Clonal hematopoiesis of indeterminate potential:CHIP)
DNMT3A、TET2変異はCADリスクを1.7〜2.0倍に高め、炎症性マクロファージを増加させます。CHIP保有がん患者は心血管イベント率が非保有者の3倍に達しました。
腸内細菌叢と腫瘍微小環境
腸内細菌由来のTMAOは動脈硬化を促進し、Fusobacterium nucleatumは大腸がん増殖を誘導します。腫瘍微小環境では低酸素によりHIFが活性化し、血管新生と心血管リモデリングを同時に進めます。
臨床的意義と明日からの実践
- リスク評価の統合:
- がん患者では心血管リスクを定期的に評価し、その逆も同様に行いましょう。
- 肺がん検診のCTで偶然発見された冠動脈石灰化は、心血管リスク層別化に有用です。
- 生活習慣の改善:
- 地中海食や植物ベースの食事を採用し、加工肉や糖質飲料を避けましょう。
- 週に150分以上の中強度運動を継続することが推奨されます。
- 薬剤の選択:
- GLP-1受容体作動薬は、肥満や2型糖尿病患者において心血管イベントとがんリスクの双方を減少させます。
- SGLT2阻害薬やスタチンも心保護と抗がん効果の両面で期待されています。
- ストレス管理:
- 慢性ストレスはアロスタティック負荷を高めます。マインドフルネスや十分な睡眠でストレスを軽減しましょう。
- 禁煙と節酒:
- 喫煙者は禁煙により10年以内に肺癌リスクを50%減らせます。
- アルコールは少量でもがんリスクを高める可能性があるため、節酒を心がけましょう。
終わりに
がんとCVDは、生活習慣から分子機序に至るまで重なり合い、互いに病態を強め合います。この「二重の負担」を軽減するためには、両者を別々に扱うのではなく、統合的な予防・管理が必要です。今日からできることは明確です。禁煙、バランスの取れた食事、定期的な運動、体重管理。さらに、薬物療法の新知見を積極的に取り入れることです。こうした取り組みが、がんとCVDの双方の未来を変える可能性を秘めています。
参考文献
Alhuneafat L, Guha A, Blaes A, Konety SH. Cancer and Cardiovascular Disease: Shared Risk Factors, Mechanisms, and Clinical Implications. JACC: CardioOncology. 2025;7(5):453–469. doi:10.1016/j.jaccao.2025.07.001