はじめに:血中脂質の運搬体は、ただの「容器」ではない
血中に存在する脂質は、水に溶けないという性質上、運搬のためにタンパク質と複合体を形成して「リポタンパク」として存在します。これらのリポタンパクは、まるで細胞間を行き交う宅配便のようにコレステロールやトリグリセリドを運び、生命活動を維持しています。
密度やサイズによって、カイロミクロン(CM)、超低密度リポタンパク質(VLDL)、低密度リポタンパク質(LDL)、高密度リポタンパク質(HDL)などに分類されます。
これらの粒子に付随する「アポリポタンパク」は、リポタンパクの表面に結合していますが、単なる添え物ではなく、受容体認識、粒子の安定性、代謝経路の選定といった高度な機能制御を担っています。
例えば、ApoB100はLDLの主要な構成成分であり、LDL受容体への結合を介してコレステロールの取り込みを促進します。一方、ApoA1はHDLの主要なタンパク質で、逆コレステロール輸送(血管壁からの過剰なコレステロールの回収)を促進します。
中でも注目すべき存在が「リポタンパク(a)」、すなわちLp(a)(「エルピーリトルエー」と読むみたいです)です。Lp(a)は、LDLに似た構造を持ちながら、Apo(a)というユニークなアポリポタンパクを追加で含んでいます。本稿では、最新の知見に基づいてこの特殊なリポタンパクの構造、生理機能、疾患との関連、さらに臨床応用の可能性を解説いたします。
Lp(a):LDLと似て非なる構造的特異性
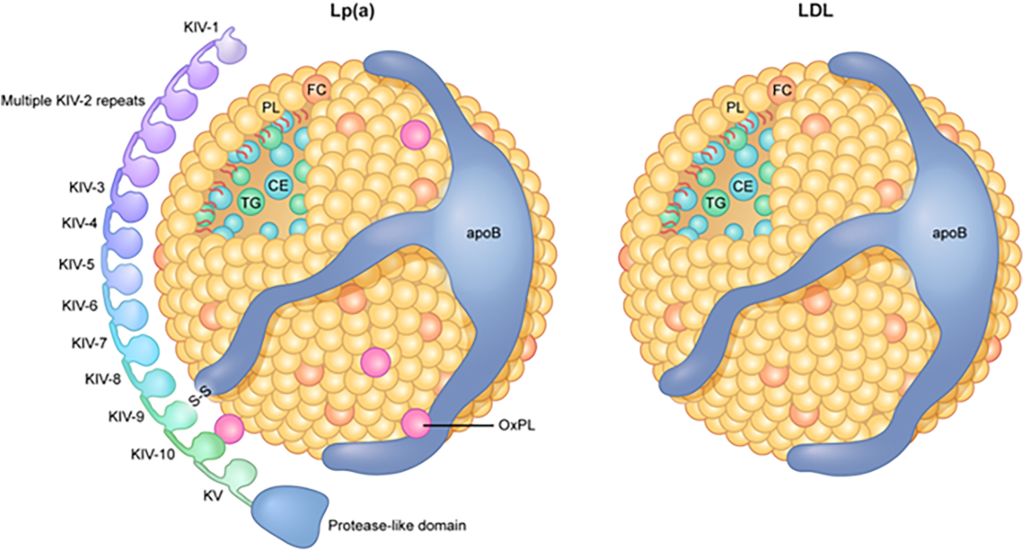
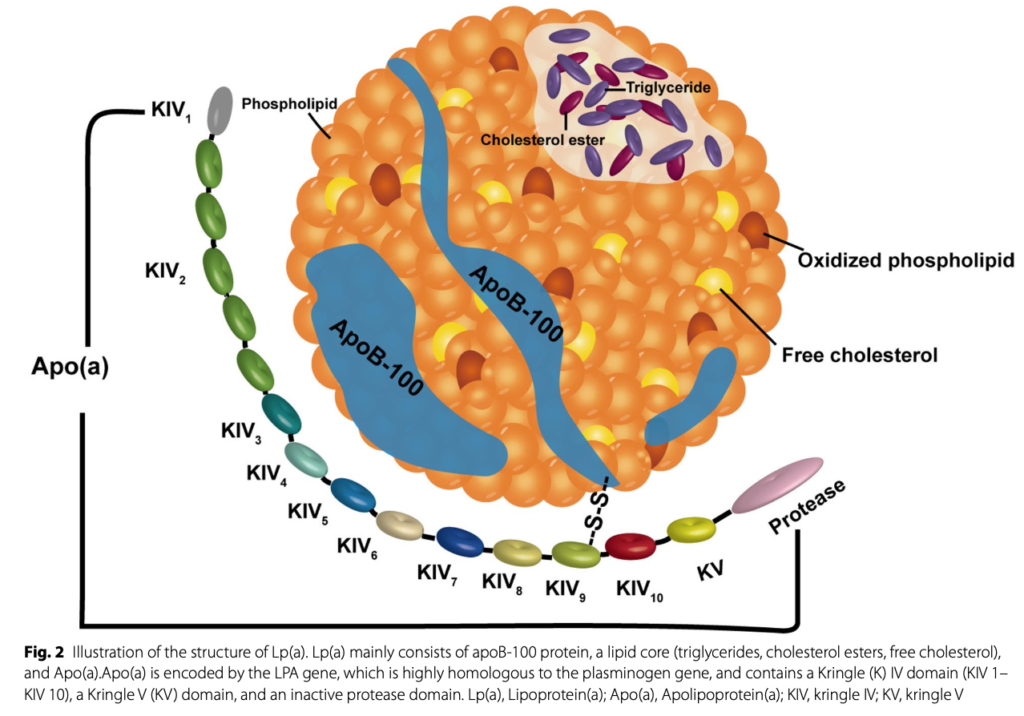
Lp(a)は見かけ上、悪玉とされるLDL(低密度リポタンパク)と類似しています。どちらもApoB-100を持ち、脂質を内包する粒子ですが、Lp(a)にはこのApoB-100に加えて、特徴的な糖タンパク「アポリポタンパク(a)(Apo(a))」が共有結合で結びついています。このApo(a)こそが、Lp(a)の多様性と病原性の鍵を握ります。
Apo(a)は、フィブリン溶解系に関与する「プラスミノーゲン(PLG)」と高度な相同性を持ち、特に「クリングルIV型リピート(KIV-2)」と呼ばれる領域のコピー数が個体差を生みます。その数は13コピー未満から50コピー以上と幅広く、このKIV-2コピー数がLp(a)の分子サイズと血中濃度を左右します。一般に、KIV-2コピー数が少ない個体ではLp(a)濃度が高くなり、これが動脈硬化リスクの上昇と関係していることが知られています。
( J Am Heart Assoc. 2024 Jun 18;13(12):e033654. )
Lp(a)
(Mol Biomed. 2024;5(1):53.)
血中Lp(a)濃度は生涯ほぼ一定:その臨床的意味
他のリポタンパク(例:LDL-CやHDL-C)は、食事、運動、肥満、薬物療法などによって変動するのに対し、Lp(a)濃度は90%以上が遺伝子(LPA遺伝子)で規定されており、生涯を通じて大きく変化しません。閉経や腎機能障害、重度の炎症状態、肝機能障害などが影響を与えることもありますが、生活習慣の介入ではほとんど下げられないのが実情です。
このため、Lp(a)は一次予防や早期スクリーニングにおいて極めて有用な生涯変動の少ないリスクマーカーといえます。欧州動脈硬化学会は、すべての成人に一度はLp(a)の測定を推奨しています。
Lp(a)がもたらす疾患リスク:なぜ危険なのか?
Lp(a)が危険視される最大の理由は、その構造がもたらす多面的な病原性です。
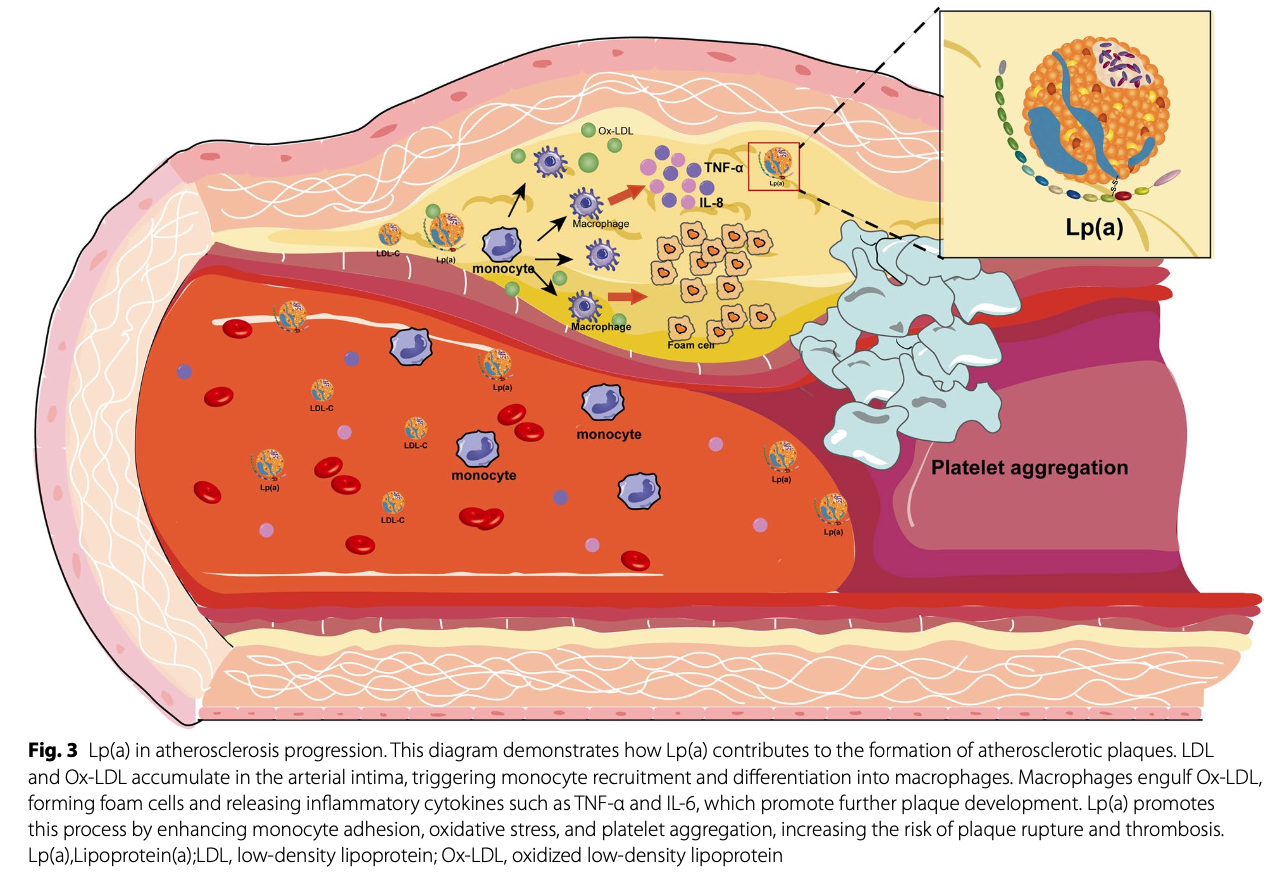
アテローム形成の促進
・ApoB-100を介して血管内皮に侵入し、LDL同様に泡沫細胞形成を助長します。
・LDLと共通の作用です。
炎症の亢進
・Lp(a)は酸化リン脂質(OxPL)をLDLよりもはるかに多く保持しており、マクロファージを活性化し、IL-8やTNF-αといったサイトカインを産生させ、炎症反応をより強く誘導します。
・Apo(a)はマクロファージに対してIL-8やMCP-1(monocyte chemoattractant protein-1)などのケモカインの発現を特異的に誘導します。
・さらに、アポ(a)自体が免疫細胞のケモタキシスやサイトカイン産生を促進する機能を持つとされており、これはLDLにはない特性です。
・これらの炎症により血管内皮機能を障害します。
・OxPLは炎症反応を誘導し、泡沫細胞の形成や血管平滑筋細胞の石灰化を促進します。
血栓傾向の亢進
・Apo(a)がプラスミノーゲンと競合し、線溶系を阻害。線溶系というのは血栓を溶解させるシステムですので、競合することにより血栓が溶解しにくい状態を作り出します。さらに血小板凝集を促進します。
これら3つの機序により、Lp(a)は「血管に沈着しやすく、炎症を起こしやすく、詰まりやすい」という、まさに動脈硬化の三拍子を備えたリポタンパクといえます。
Lp(a)はLDLのおおよそ6倍、動脈硬化惹起性が高いと言われています。
疾患ごとの関連性:疫学と病態から読み解く
冠動脈疾患(CAD)
Lp(a)濃度が高い人では、心筋梗塞や狭心症のリスクが2倍以上に上昇すると報告されています。特に冠動脈疾患の家族歴がある場合や、LDL-Cが低くてもイベントを起こす「残余リスク」の原因として注目されています。
また、Lp(a)は血管平滑筋細胞の軟骨骨形成分化を誘導し、冠動脈石灰化を促進します。CACスコアと併用することでASCVDリスク層別化の精度向上が可能です。
大動脈弁狭窄症(AS)
デンマークの77,680人を対象とした研究では、Lp(a)濃度が上昇するにつれASの発症率が直線的に上昇することが示されました。特に若年男性で強い関連があり、性差・年齢差に対する病因解明が今後の課題です。
末梢動脈疾患(PAD)
99パーセンタイル以上のLp(a)値を示す群では、PAD発症リスクが有意に上昇し、下肢切断や主要な血管イベント(MALE)の予測因子ともなっています。動脈硬化性血管障害全般において、Lp(a)の意義は無視できません。
高血圧
Lp(a)は血管内皮障害や平滑筋細胞機能障害を介して高血圧に関与する可能性。高血圧との相互作用により動脈硬化や炎症作用が増強されると考えられています。
心不全
Lp(a)は心筋梗塞、AS、高血圧との関連を通じて心不全リスクを高めます。心不全におけるLp(a)の役割を明らかにするために、さらなる研究が必要です。
脳卒中と認知症
Lp(a)の高値は、大血管性脳梗塞のリスクを高めるとするメンデルランダム化研究の報告があり、脳血管障害の予防においても無視できません。アルツハイマー病や血管性認知症の患者では、Lp(a)濃度が上昇していることが報告されています。
がん
LDL-Cは乳がん・大腸がん・前立腺がんなどの進行や予後不良と関連しています。一方、Lp(a)は肺がん・頭頸部がんなどとの関連が報告され、免疫チェックポイント阻害薬の反応性にも関与する可能性。
・乳がん:Lp(a)濃度とHER2発現との負の相関が指摘されています。
・肺がん:進行期の肺がん患者ではLp(a)濃度が上昇し、腫瘍のステージと相関することが示されています。
糖尿病
Lp(a)は2型糖尿病の発症とは負の関連を持つが、合併症(腎症・網膜症)リスクは高める可能性があります。LDL-Cはインスリン抵抗性や血管合併症を悪化させます。
慢性腎疾患(CKD)
Lp(a)は腎機能低下に伴い上昇し、糸球体硬化や腎機能悪化を促進する可能性。CKD患者では心血管リスクが高く、Lp(a)の治療標的としての可能性があります。
自己免疫疾患
関節リウマチ(RA)や全身性エリテマトーデス(SLE)で高Lp(a)が認められ、Lp(a)濃度が炎症マーカーと相関します。腎障害との関連が強い。生物学的製剤による治療がLp(a)濃度に影響を与える可能性があります。
Lp(a)の臨床管理:既存薬と新世代治療の狭間で
残念ながら、スタチン、エゼチミブ、フィブラートといった従来の脂質低下薬ではLp(a)はほとんど下がりません。むしろスタチンによってわずかに上昇するという報告さえあります。
唯一、ナイアシン(ニコチン酸)は最大30%程度のLp(a)低下を示しますが、耐容性や副作用の問題から広くは使われていません。
しかし、近年では以下の新規治療が開発されています。
PCSK9阻害薬
エボロクマブやアリロクマブはLDL-Cを60%以上低下させるとともに、Lp(a)を20〜30%低下させる効果が確認されています。
アンチセンスオリゴヌクレオチド(ASO)
ペレカーセンはApo(a)のmRNAを標的とし、Lp(a)合成を阻害します。臨床試験では80%以上の低下が確認されています。臨床試験(第III相試験)が進行中です。
RNA干渉(RNAi)療法
インクライシランやゼルラシランは、Lp(a)の産生を長期的に抑制します。臨床試験が進行中です。
これらの革新的な治療法は、今後の高リスク患者の二次予防戦略の中心になる可能性があります。
明日からできる実践:何を測り、何をすべきか
- 一度はLp(a)の測定を
特に家族歴、早期冠動脈疾患歴、スタチン服用でも再発するなど残余リスクを持つ方は、血液検査でLp(a)の評価を検討しましょう。 - ApoBの測定も併用を
LDL-Cが正常でも、ApoBが高い場合は動脈硬化リスクが高い可能性があります。特に糖尿病・肥満のある方は重要です。(LDL-Cが正常でも、ApoBが高い場合は「小型で密なLDLが多い」可能性があり、リスクが高いと判断されます) - スタチン治療中もリスクはゼロではない
LDL-C管理が良好でも心血管イベントが再発する場合、Lp(a)やApoBなどの「粒子ベース」の指標が重要です。 - 生活習慣は無意味ではない
Lp(a)自体は下がらなくても、他の修飾可能なリスク(高血圧、糖尿病、喫煙など)をコントロールすることで、イベントリスクを大きく下げることができます。
おわりに
Lp(a)は、遺伝的に決定される強力な心血管リスク因子です。そのユニークな構造と多様な病態への関与から、治療ターゲットとしての重要性が高まっています。現在進行中の臨床試験の結果次第では、Lp(a)を特異的に低下させる治療が日常診療に導入される可能性があります。
参考文献
・Ma Z, Zhong J, Tu W, Li S, Chen J. The functions of apolipoproteins and lipoproteins in health and disease. Mol Biomed. 2024;5(1):53. https://doi.org/10.1186/s43556-024-00218-7
・Volgman AS, Koschinsky ML, Mehta A, Rosenson RS. Genetics and Pathophysiological Mechanisms of Lipoprotein(a)-Associated Cardiovascular Risk. J Am Heart Assoc. 2024 Jun 18;13(12):e033654. doi: 10.1161/JAHA.123.033654. Epub 2024 Jun 15. PMID: 38879448; PMCID: PMC11255763.