はじめに
心房細動は、世界で最も一般的な持続性不整脈であり、その負担は単なる脳卒中のリスク増大にとどまりません。臨床データによれば、心房細動患者の実に22パーセントから51パーセントが、持続的な記憶障害を呈しているという驚くべき事実があります。しかし、これほど高い頻度で発生しているにもかかわらず、その背景にある「心臓が脳の構造と機能をどのように変質させるのか」という詳細なプロセスは、これまで霧の中にありました。
本研究において、心房細動患者38名と健康な対照群45名を比較したところ、その知性の乖離は数値として明確に示されました。ミニメンタルステート検査((Mini-Mental State Examination;MMSE)のスコアは、対照群の29.02に対し、心房細動患者では26.53と有意に低下していました。さらに深刻なのは言語学習能力です。聴覚言語学習テスト(Auditory Verbal Learning Test;AVLT)の即時再生スコアにおいて、心房細動群は12.23という数値を記録し、対照群の16.91を大きく下回りました。これは、単なる加齢に伴う物忘れではなく、心疾患が直接的に神経基盤を侵食していることを物語っています。
神経解剖学的変容:脳の萎縮
この研究の新規性は、心臓の物理的な変容が、脳のどの領域を、どのようなメカニズムで破壊するのかを具体的に特定した点にあります。
本研究では、3.0テスラの高磁場磁気共鳴画像法(MRI)を用いたマルチモーダル解析が導入されました 。研究チームは、高解像度の3D T1強調画像を用いた構造的MRI(sMRI)と、脳の活動を血流変化から捉えるボールドMRI(BOLD-MRI)を撮影しました
まず、脳の「容積」という物理的な側面から記憶障害を分析するために、ボクセルベース形態計測(VBM)というMRI解析手法が用いられました 。これは、MRI画像をボクセルという微細な単位に分割し、組織ごとの密度や体積を統計的に比較する手法です 。この解析により、心房細動患者の脳内では、両側の鳥距溝、楔部、舌状回、下および中側頭回、そして左紡錘状回において、灰白質体積が有意に減少していることが判明しました。
本研究の対象となった心房細動群のLVDdの平均値は4.96(標準偏差0.40)センチメートルでした。臨床的な正常上限とされる5.5センチメートルを下回っており、一見すると「正常範囲内」の症例が中心であることが分かります。しかし、解析の結果、この正常範囲内に収まるような微細なLVDdの変動が、左中側頭回(MTG.L)の灰白質体積と有意な正の相関(r=0.460, p=0.016)を示したのです。
心房細動においては、心房の有効な収縮が失われることで、心室への血液の充填(プレロード)が著しく低下します。本研究の対象となった患者群において、LVDdが比較的小さい、あるいは減少傾向にある症例は、心臓が一度の拍動で送り出せる血液量(一回拍出量)が物理的に制限されている状態を反映していると考えられます 。
つまり、この正の相関が真に意味するところは、「心臓の充填容積(LVDd)が不足している患者ほど、脳への血流供給(灌流)が滞り、結果として左中側頭回などの記憶に関わる重要な脳領域が、栄養失調状態に陥って物理的に萎縮(灰白質体積の減少)している」という過酷な現実です 。事実、左中側頭回の体積が小さいほど、記憶テスト(AVLT-Recall)の成績も有意に低下しており(r=0.398, p=0.044)、心臓の「容積の枯渇」が脳の「知性の枯渇」に直結していることが示されました 。
心室が肉眼的な「拡大」を呈する以前の段階、すなわちサブクリニカルなレベルでの心室のコンプライアンスや一回拍出量の変化が、脳の血流灌流パターンに影響を与えている可能性を示唆しています。左中側頭回は、言語情報の処理や記憶の検索において極めて重要なハブ領域です。心室の拡張末期容量が最適に保たれないことによる前向き拍出量の微量な低下が、長期間にわたってこの「エネルギー多消費領域」に軽微な灌流不全を強いているという、極めて繊細なメカニズムが浮かび上がってきます。
さらに、右下側頭回(r=0.519, p=0.006)や左楔部(r=0.427, p=0.026)においても同様の相関が認められました。楔部は視覚情報の統合やエピソード記憶に関与しており、これらの領域が「心臓の構造的ゆらぎ」に敏感に反応しているという事実は、心脳軸の接続がいかに緻密であるかを証明しています。
炎症という名の目に見えない侵略
本論文が提示するもう一つの衝撃的な知見は、心臓の「構造」による萎縮とは全く別の、血液を介した「炎症」による機能障害の経路です 。心房細動は単なるリズムの異常ではなく、全身的な炎症状態を引き起こす疾患でもあります。
研究では、炎症マーカーであるプロカルシトニン(PCT)の値が、右後中心回(PoCG.R)と海馬の間の機能的結合(FC)と有意な負の相関(r=-0.477, p=0.010)を示しました 。さらに、この結合の弱体化は、20分後の遅延再生スコアの低下(r=-0.482, p=0.013)と見事に一致していました。
これは、心臓の物理的な変形(LVDdの変化)とは無関係に、心房細動によって誘発された全身性の炎症反応が、海馬を中心とした精緻な神経回路の「同期性」を直接破壊していることを意味します 。分子レベルで見れば、放出されたインターロイキン-6(IL-6)やPCTといった炎症性メディエーターは、血液脳関門を越えて中枢神経系へと侵入し、ミクログリアを活性化させます。この神経炎症の連鎖が、神経可塑性の基盤であるシナプスの接続強度を弱め、伝達効率を阻害し海馬を中心とした機能的結合(FC)を撹乱、記憶を長期保存するためのネットワーク形成(長期増強:LTP)を妨害していると考えられます 。炎症という分子レベルの嵐が、私たちの記憶の長期保存能力を、回路レベルで遮断しているのです。
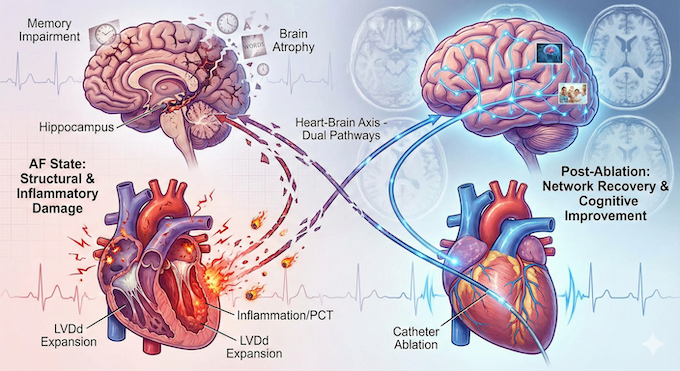
この「構造(LVDdによる萎縮)」と「機能(炎症による結合不全)」という二重の経路(デュアル・パスウェイ)が、心房細動患者の記憶を多角的に攻撃しているのです 。
カテーテルアブレーション:心脳軸の再編と回復の光
しかし、この絶望的な崩壊の連鎖は、現代医学の介入によって希望へと転じることが示されました。本研究の核心的な結論の一つは、カテーテルアブレーション治療が、心臓のリズムを戻すだけでなく、脳の機能的ネットワークをも「再構築」し得るという点です。
治療後わずか7日目の評価において、患者の脳内では劇的な変化が確認されました。「静止期機能的磁気共鳴画像法(resting-state fMRI / rs-fMRI)」により、海馬と右中前頭回、左上前頭回、そして右中帯状回との間の機能的結合が有意に強化されたことが示されました。これらの領域は、実行機能や記憶の定着、認知的制御を司る重要なハブです。
術後、洞調律が回復することで、左心房の圧力が低下し、心拍出量が最適化されます。これにより脳への灌流が改善されるとともに、心臓由来の炎症ストレスが軽減されることで、海馬を中心としたネットワークが「機能的な呼吸」を再開したと考えられます。この急性期の変化は、長期的な認知機能の回復に向けた重要な足掛かりとなるでしょう。
本研究の限界と今後の展望
学術的な厳密さを期すため、本研究の限界についても触れなければなりません。まず、心房細動患者のサンプルサイズが36名と比較的少数であり、特に術後まで追跡できたのが14名にとどまっている点は、結果の普遍性を担保する上でさらなる大規模検証を必要とします。また、術後7日目という評価期間は、カテーテル治療がもたらす長期的な認知改善効果を断定するには短すぎます。
さらに、併存疾患や抗凝固療法などの薬剤使用の影響、あるいは手術そのものが与えるストレスや麻酔の影響を完全に分離して評価することには困難が伴います。今後の研究では、6ヶ月以上の長期追跡によって、この初期の機能改善が果たして永続的な構造回復(灰白質体積の再増大)へとつながるのかを検証する必要があります。
知性を守るための明日からの実践
この論文が提示する科学的事実から、私たちが明日から行動に移せる具体的な教訓は何でしょうか。知識人として、そして自己の健康の管理者として、以下の三つの視点が極めて重要です。
第一に、心房細動を「単なる動悸の病気」ではなく、「脳の構造を破壊する進行性の神経疾患」と再定義することです。記憶力のわずかな衰えを感じた際、それが心機能の低下に由来する可能性を疑うインテリジェンスが求められます。
第二に、早期治療介入の重要性です。研究データが示す通り、カテーテルアブレーションは心臓の解剖学的リモデリングだけでなく、脳の機能的結合を速やかに正常化させる可能性を持っています。萎縮が不可逆的な段階に至る前に、高度な不整脈治療を検討することは、将来の認知機能維持において極めて合理的な選択となります。
第三に、炎症マネジメントの意識です。血液中のPCTやIL-6といった微細な炎症マーカーが脳のネットワークを阻害するという事実は、日常的な抗炎症的ライフスタイル(適切な睡眠、ストレス管理、食事療法)がいかに心脳軸の保護に寄与するかを裏付けています。心臓の健康数値を維持することは、まさにあなたの知性の砦を守ることと同義なのです。
心臓が刻むビートと、脳が紡ぎ出す思考。この二つのハーモニーが乱れたとき、私たちのアイデンティティとも言える「記憶」が脅かされます。しかし、科学はその不協和音を修正する術を今、手に入れつつあります。
参考文献
Chen X, Ni J, Wang Y, Kou D, Ge D, Xue X, Zhao Y, Xu B, Li M and Chen J (2025) Cardiac structure and inflammation drive memory impairment via dual pathways of heart-brain axis dysregulation in atrial fibrillation patients undergoing catheter ablation. Front. Neurosci. 19:1725953. doi: 10.3389/fnins.2025.1725953