不整脈治療における歴史的ジレンマと新たなパラダイム
循環器内科の歴史において、心筋梗塞後の不整脈管理は常に困難な課題であり続けてきました。かつてCAST試験(Cardiac Arrhythmia Suppression Trial)が我々に突きつけたのは、ナトリウムチャネル遮断薬による心室性期外収縮(PVC)の抑制が、必ずしも患者の生存利益に結びつかないばかりか、むしろ死亡率を上昇させるという衝撃的な事実でした。このパラドックスは、イオンチャネルを直接標的とする従来の抗不整脈薬が内包するプロアリスミア(催不整脈作用)のリスクを浮き彫りにし、以来、我々は電気的安定化をもたらすための「イオンチャネルを超えた」新たな機序を模索してきました。
今回紹介するShenらの研究は、従来の常識を根底から覆す可能性を秘めています。彼らが着目したのは、禁煙補助薬として知られるバレニクリン(Varenicline)(商品名:チャンピックス)です。驚くべきことに、この薬剤が心筋細胞に存在する特定のニコチン受容体を介して、心室の電気的安定性を劇的に改善させることが示されました。これは、不整脈治療の主戦場がイオンチャネルの直接遮断から、細胞内シグナルによる基質の安定化へとシフトする歴史的な転換点となるかもしれません。
細胞内に秘められた独自のコリン作動性システム
本研究の根幹を成すのは、研究グループが近年発見した「心室筋細胞に内在する独自のコリン作動性システム」という知見です。これまで、心筋に対するアセチルコリンの作用は主に迷走神経からの遊離によるものと考えられてきました。しかし、Shenらは心室筋細胞自体がアセチルコリンを合成し、小胞に貯蔵・放出する一連の機構(cardiomyocyte-intrinsic cholinergic system)を備えていることを明らかにしました。
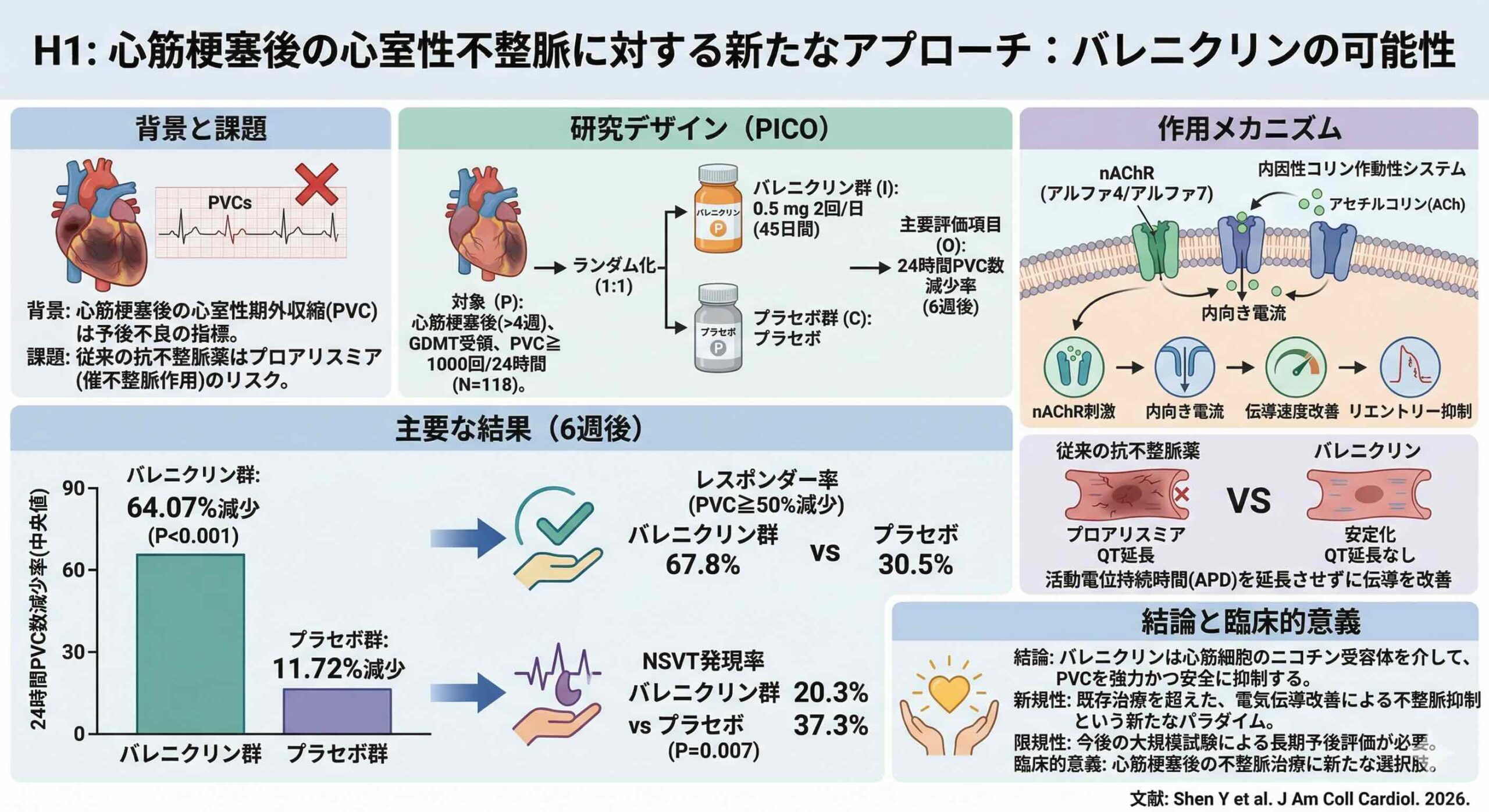
このシステムにおいて、α4およびα7サブタイプを含むニコチン性アセチルコリン受容体(Cardiac nicotinic acetylcholine receptors; nAChR)が重要な役割を果たします。アセチルコリンがこれらの受容体に結合すると、アゴニスト依存性の内向き電流が誘発されます。特筆すべきは、この機序が活動電位持続時間(APD)を延長させることなく、細胞の興奮性を高め、心室の電気伝導速度を加速させる点です。従来の抗不整脈薬が伝導遅延やQT延長を介して不整脈を誘発しやすかったのに対し、nAChRの活性化は伝導を改善することでリエントリーの発生を抑制するという、極めて合理的かつ新しいアプローチを提供します。※ 最下段の補足参照
研究プロトコールの全容(PICO)
本研究は、バレニクリンの心室性不整脈に対する有効性と安全性を検証した多施設共同、ランダム化、二重盲検、プラセボ対照、第2相概念実証(Proof-of-Concept)試験です。
対象(Population):心筋梗塞(MI)発症から4週間以上経過し、ガイドラインに準じた標準的治療(GDMT)を受けている成人患者。かつ、72時間連続心電図において24時間あたりの心室性期外収縮(PVC)数が1,000回以上確認された118名。
対象者の約半数が LVEF 50% 未満。LVEF 35%未満 の症例は、全体で22名(18.6%)。NYHA心機能分類においては、クラス I が約42%、クラス II が約58%。
介入(Intervention):バレニクリン 0.5 mgを1日2回、45日間投与(最初の3日間は0.5 mgを1日1回の導入期、最後の3日間は漸減期を設定)。
比較(Comparison):プラセボの投与。
アウトカム(Outcome):主要評価項目は、ベースラインから6週時点までの24時間平均PVCカウントの変化率。主要な二次評価項目は、PVC数が50%以上減少したレスポンダー率、および非持続性心室頻拍(NSVT)の発現率。
治療効果:60%のPVC減少とNSVTの半減
解析の結果、バレニクリン群はプラセボ群と比較して、圧倒的な治療効果を示しました。主要評価項目である24時間PVCカウントの減少率において、バレニクリン群はプラセボ群よりも60.1ポイントも大きな改善を認めました(平均値;バレニクリン群-40.9%,プラセボ群+19.1%)(95% CI:21.3-98.8ポイント、p = 0.001)。具体的な中央値で見ると、バレニクリン群では64.07%もの減少が得られたのに対し、プラセボ群では11.72%の減少に留まっています。
さらに、臨床的に重要な二次評価項目でもその優位性は揺るぎませんでした。PVC数が50%以上減少したレスポンダー率は、バレニクリン群で67.8%に達し、プラセボ群の30.5%と比較して2倍以上の高い反応を示しました(相対リスク:2.22、p < 0.0001)。また、致死的不整脈の予兆ともなるNSVTの発現率についても、バレニクリン群では20.3%に抑制され、プラセボ群の37.3%と比較して有意に低い結果となりました(相対リスク:0.49、p = 0.007)。
特筆すべきは、これらの効果がβ遮断薬(メトプロロール)を含む最適化された背景治療下で、上乗せ効果として確認された点です。これは、nAChRを介した経路がβアドレナリン経路とは独立した、強力な不整脈抑制機序であることを強く示唆しています。
優れた安全性プロファイルと「催不整脈作用」の不在
本研究において最も注目すべき成果の一つは、強力な不整脈抑制効果を実現しながらも、重大な安全性上の懸念が認められなかった点です。バレニクリン群において、死亡や持続性心室頻拍、心室細動などの悪性心室性不整脈の発現はゼロでした。一方、プラセボ群では2名の突然死と2例の持続性心室頻拍が報告されています。
心電図パラメータの解析においても、バレニクリン群ではPR間隔、QRS幅、およびQT間隔(QTcF)に臨床的な悪影響を認めませんでした。特にQT延長が見られなかったことは、従来のカリウムチャネル遮断薬とは決定的に異なる利点です。また、バレニクリンの禁煙治療において懸念されることのある神経精神医学的な副作用や消化器症状についても、本試験の対象となった非喫煙者の心血管疾患患者においては、プラセボ群と同程度の低い発現率に留まりました。これは、ニコチン離脱に伴う症状が混在しない状況下では、バレニクリンが極めて良好な忍容性を持つ可能性を示しています。
本研究の新規性と学術的インパクト
本研究の最大の新しさは、禁煙補助薬という既存の薬剤に、全く新しい「心臓保護・抗不整脈薬」としての顔を見出したことにあります。これまでの抗不整脈治療は、イオンチャネルという「門」を閉じることで異常な電気信号をブロックしようとしてきました。しかし、これは同時に正常な電気伝導までも阻害し、新たな不整脈の火種を作るというリスクと隣り合わせでした。
対して、本研究が示したnAChRの刺激は、心筋細胞が本来持っているコリン作動性の安定化機構を活性化させます。いわば「門を閉じる」のではなく、「電気の通り道を整える」ことで、心臓全体の電気的な調和を取り戻すというアプローチです。この分子生物学的なターゲットの発見は、心筋梗塞後の再構築された心筋における不整脈基質を改善するための、全く新しい戦略を提供したと言えます。
研究の限界点(Limitation)
本研究は極めて有望な結果を示しましたが、いくつかの限界点も正しく認識しておく必要があります。
第一に、本試験は第2相の概念実証試験であり、症例数が118名と比較的少数であることです。また、観察期間が45日間と短く、総死亡や心不全入院といった長期的なハードアウトカムを評価するまでには至っていません。
第二に、登録患者の約90%が男性であり、かつ漢民族が中心であるため、性差や民族差に関する汎用性には議論の余地があります。
第三に、NYHA心機能分類がIまたはIIの比較的安定した患者を対象としており、より重症な心不全患者における安全性と有効性は未解明です。
第四に、PVC数というサロゲートマーカーを用いた評価であるため、PVCの抑制が最終的な生存率の向上に直結するかどうかは、今後の大規模な第3相試験を待つ必要があります。
明日から実践できること、活かせる知見
この論文から得られる知見は、直ちにバレニクリンを不整脈治療薬として処方することを推奨するものではありませんが、臨床現場において以下の視点を持つことは非常に有益です。
まず、喫煙者で心筋梗塞後の不整脈を合併している患者において、禁煙治療としてバレニクリンを選択することの心理的・臨床的な妥当性が、これまで以上に強固になったと言えます。不整脈を悪化させる懸念が少なく、むしろ抑制的に働く可能性があるというデータは、患者指導において強力なエビデンスとなります。
次に、抗不整脈治療の未来像として「伝導速度の改善による安定化」という概念を意識しておくことです。今後、nAChRを標的とした薬剤開発が進む中で、心機能が低下した症例やQT延長リスクの高い症例において、この機序が第一選択となる時代が来るかもしれません。最新の不整脈治療薬のニュースをチェックする際、コリン作動性システムやニコチン受容体といったキーワードに注目しておくことは、専門家としてのアンテナを高く保つことに繋がります。
最後に、心室筋自体がアセチルコリンを産生しているという発見は、自律神経管理の重要性を再認識させます。ベータ遮断薬による交感神経抑制だけでなく、副交感神経系の賦活化がいかに心臓保護に寄与するかを理解することは、多角的な治療戦略を構築する上での助けとなるでしょう。
参考文献
Shen Y, Guo X, Zeng C, et al. Varenicline and Ventricular Ectopy After Myocardial Infarction: A Randomized Phase 2 Study. J Am Coll Cardiol. 2026; (in press). doi: 10.1016/j.jacc.2025.12.090.
補足:心筋細胞内因性コリン作動性システムの生理学的役割
心筋細胞内因性コリン作動性システム(Cardiomyocyte-intrinsic cholinergic system)は、心室心筋において電気的な安定性を維持するために不可欠な役割を担っています。このシステムは、心臓の外部から作用する迷走神経などの自律神経系とは独立して、心筋細胞そのものがアセチルコリンを合成・貯蔵・放出し、自身の受容体を介して機能する独自の制御機構です 。このシステムが本来果たしている主要な役割について解説します。
心筋の興奮性と伝導速度の調節
このシステムの最も中心的な役割は、心室筋細胞の興奮性と電気的な伝導速度を最適に保つことです。心筋細胞内で放出されたアセチルコリンが、ニコチン性アセチルコリン受容体(nAChR)、特にα4およびα7サブタイプに結合することで、細胞内に内向き電流を誘発します 。
この機序により、以下の生理的作用がもたらされます。
- 細胞興奮性の増強:内向き電流の発生により、心筋細胞が電気的刺激に対して反応しやすくなります 。
- 伝導速度の加速:心室全体における電気信号の伝わり(伝導速度)を速めます 。
- 活動電位持続時間の維持:重要な点として、活動電位の持続時間(APD)を延長させることなく伝導速度のみを改善します 。
従来の抗不整脈薬の多くが、伝導を遅らせたりQT間隔(APDに相当)を延長させたりすることで新たな不整脈を誘発するリスクを持つのに対し、この内因性システムは「素早く、かつ安定した」電気伝導を実現する役割を担っています 。
不整脈基質の安定化とリエントリーの抑制
このシステムが正常に機能することで、心室筋は電気的な不安定性から保護されています。伝導速度を適切に維持することは、不整脈の主要な発生機序である「リエントリー」の防止に直結します 。
もしこのシステムが障害(機能低下や受容体のダウンレギュレーション)を受けると、以下のような悪影響が生じます 。
- アゴニスト依存性の内向き電流が減少する 。
- 活動電位の発生閾値が上昇し、細胞の興奮性が低下する 。
- 結果として心筋の伝導速度が低下し、電気的な興奮が旋回しやすくなる(リエントリー感受性の亢進) 。
つまり、内因性コリン作動性システムは、心室における電気伝導の「潤滑油」のような役割を果たしており、心筋梗塞後などの病的な状態においても、電気的な調和を保ち、心室性期外収縮(PVC)や心室頻拍(VT)の発生を抑制する防波堤として機能しているのです 。
分子生物学的構成要素
このシステムが「内因性」と呼ばれる理由は、心筋細胞が神経系に頼らずとも独立して機能できる以下のコンポーネントをすべて備えているためです 。
- アセチルコリン合成酵素
- 小胞への貯蔵機構
- 放出のための装置(release machinery)
- 機能的なニコチン性アセチルコリン受容体(nAChR)
これらの要素が協調して働くことで、心臓は刻一刻と変化する負荷やダメージに対し、自身の電気的特性を微調整し、致命的な不整脈から身を守るための恒常性を維持しています 。
ちなみに、バレニクリンが禁煙治療薬として作用する機序
バレニクリンが禁煙治療薬として作用する機序は、心筋保護のメカニズムとはターゲットとする場所が異なりますが、受容体に対する「部分作動薬(パルシャルアゴニスト)」としての性質を利用している点では共通しています。
禁煙薬としての主な作用機序は、以下の2つの柱で成り立っています。
1. ニコチン離脱症状の緩和(中枢神経への作用)
バレニクリンは、脳内の報酬系に存在するニコチン性アセチルコリン受容体(主に α4β2サブタイプ)に結合します 。
- 部分作動薬としての働き: 完全なアゴニストであるニコチンほどではありませんが、この受容体を適度に刺激します 。
- 効果: これにより、禁煙時に不足するドーパミンが少量放出され、タバコを吸いたいという切実な欲求や、イライラなどの離脱症状が和らげられます。
2. 喫煙による満足感の抑制
タバコを吸ってしまった場合、バレニクリンが先に受容体に結合しているため、ニコチンが受容体に結合するのをブロックします 。
- 拮抗薬(アンタゴニスト)としての働き: ニコチンが本来もたらすはずの強烈なドーパミン放出を阻害します。
- 効果: 「タバコを吸っても以前ほど美味しくない」「満足感が得られない」と感じさせることで、再喫煙の意欲を削ぎます。
心筋保護メカニズムとの違い
今回の論文で示された心筋に対する作用は、これらの中枢神経(脳)への作用とは別の、心筋細胞そのものに存在する受容体を介したものです。
- 共通点: どちらも「ニコチン性アセチルコリン受容体(nAChR)」をターゲットとし、部分作動薬として受容体を活性化させる点 。
- 相違点: 禁煙薬としては脳の報酬系に作用して「依存」を制御しますが、不整脈に対しては心筋の「電気伝導速度」を加速させ、リエントリー(電気信号の空回り)を防ぐことで「不整脈」を抑制します 。
このように、バレニクリンは同じ受容体を介しながらも、作用する部位(脳か心筋か)によって全く異なる治療効果を発揮します。今回の研究は、禁煙薬として確立されていたこの薬剤の「心筋における新たな側面」を臨床的に証明したという点で、非常に画期的なものです 。
禁煙治療と不整脈治療の用量比較
今回の第2相試験(Var-PVC試験)では、循環器領域における安全性を最優先し、慎重な用量設定が行われました 。
- 禁煙治療(標準用量): 通常、1回1 mgを1日2回服用します 。
- 不整脈治療(本研究の用量): 1回0.5 mgを1日1-2回服用します 。これは禁煙治療に用いられる標準用量の2分の1に相当します 。
おまけ:心筋梗塞の既往がない「正常な心臓」の心室性期外収縮への効果は?
現時点では、心筋梗塞の既往がない「正常な心臓」の患者さんに対して、バレニクリンが同様の効果を発揮するかどうかは未知数であり、慎重な判断が必要です。
研究対象の限定性
この臨床試験は、対象者を厳格に「心筋梗塞(MI)発症から4週間以上経過した患者」に限定して実施されました 。 論文内でも、「今回の結果は、女性や他の民族、あるいはより進行した心不全患者など、対象外の集団にそのまま当てはめることはできない(cannot be generalized)」と明記されています 。したがって、心筋梗塞のない集団への効果を期待するには、科学的根拠が不足しているのが現状です。
不整脈が発生する「土壌」の違い
バレニクリンが効果を発揮した背景には、心筋梗塞によって生じた「特定の病態」が深く関わっています。
- システムの破綻: 本研究の理論的根拠は、心筋梗塞後の心臓において「内因性コリン作動性システム」が障害され、ニコチン受容体(nAChR)の機能が低下しているという点にあります 。バレニクリンはこの「低下した機能」を補うことで効果を発揮します 。
- 電気的基質の安定化: 心筋梗塞後のPVCは、梗塞巣の周囲にある不安定な心筋(基質)が原因で起こることが多いですが、正常な心臓で起こるPVC(特発性PVC)は、心室流出路など特定の部位からの「局所的な異常興奮(フォーカス)」が原因であることが一般的です。
一見正常な心臓の人におけるPVCは、nAChRの機能低下を伴っていない可能性があり、その場合、バレニクリンによる「伝導速度の加速」や「基質の安定化」が、不整脈の抑制に繋がるかどうかは分かっていません。
生物学的ターゲットの存在と今後の展望
一方で、ポジティブな側面もあります。 心筋細胞固有のコリン作動性システム自体は、ヒトやマウスの正常な心室筋細胞にも共通して存在していることが確認されています 。このため、将来的には「正常な心臓」であっても、特定の機序で起こるPVCに対して効果を持つ可能性は否定できません。
おまけの結論
心筋梗塞既往のないPVC患者に対しては、以下の理由から、現段階でバレニクリンの効果を期待して使用することは推奨されません。
- エビデンスの不在: 正常な心臓を対象とした臨床試験データが存在しないため 。
- 機序の不一致: 特発性PVCの発生メカニズムが、本研究で想定されている「nAChR機能低下による伝導遅延」と合致しない可能性があるため。
- 安全性の未確立: 正常な心臓における長期投与の安全性が評価されていないため 。
現在の臨床現場においては、既存のガイドラインに沿った治療(ベータ遮断薬、カルシウム拮抗薬、あるいはカテーテルアブレーションなど)が優先されるべきです。この研究はあくまで、「ダメージを受けた心臓の電気回路をリフォームする新しい手法」としての証明(Proof-of-Concept)であることを認識しておく必要があります 。