はじめに
競技アスリートの心血管異常は、突然の心停止や心臓死(SCD)のリスクを高めることが知られています。このリスクを適切に評価し、アスリートの競技参加をどのように管理するかは、スポーツ医学における重要な課題です。競技アスリートの心血管リスク評価は、長らく画一的なスポーツ制限を基盤としていました。
本稿では、2025年のAmerican Heart Association(AHA)およびAmerican College of Cardiology(ACC)による最新の科学的声明に基づき、競技アスリートの心血管異常に関する最新の臨床的考察を解説します。
共有意思決定(Shared Decision Making, SDM)
過去のガイドラインでは、医師が一方的にアスリートの競技参加を制限する「パターナリズム」が主流でした。しかし、今回の声明では、アスリートと医師が共同でリスクとベネフィットを評価し、個別化された決定を行う「共有意思決定(Shared Decision Making, SDM)」が強調されています。SDMは、アスリートの価値観や選好を尊重し、競技参加に関する意思決定をより倫理的かつ現実的なものにします。
例えば、肥大性心筋症(HCM)を持つアスリートの場合、過去のガイドラインでは一律に競技参加が制限されていました。しかし、最新の研究では、HCMを持つアスリートが競技を続けても、心臓イベントの発生率が必ずしも高くないことが示されています。このデータに基づき、SDMを通じて競技参加を検討することが推奨されています。
競技スポーツと心血管リスクの評価
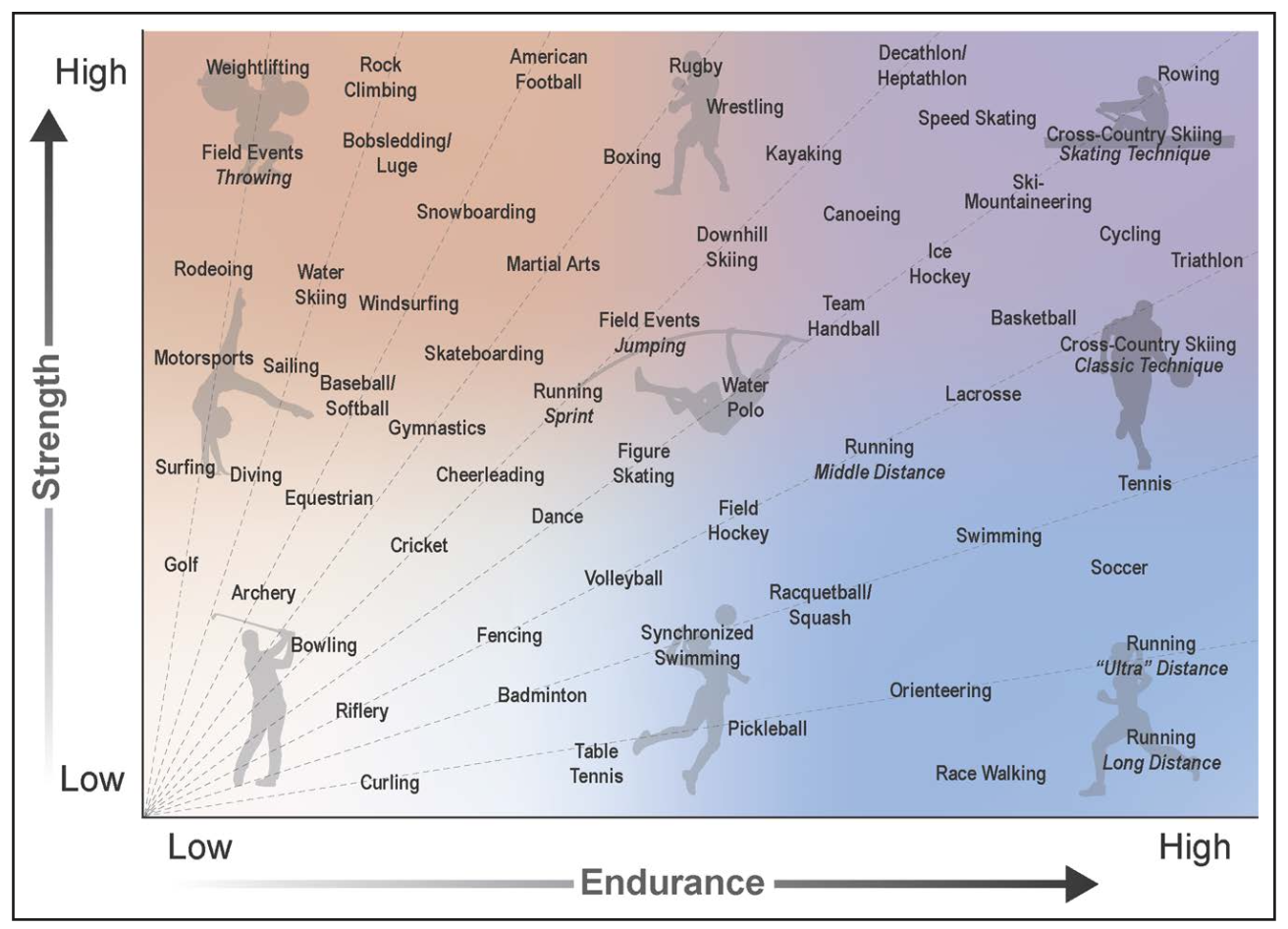
競技スポーツは、持久力(エアロビック運動)と筋力(アネロビック運動)の両面から心血管系に大きな影響を与えます。本声明では、従来の「競技スポーツの固定的分類」を見直し、スポーツを「持久力・筋力の連続体」として評価する新しい枠組みを導入しました。例えば、マラソンランナーとアメリカンフットボールのラインマンでは、心血管系への負荷が異なるため、一律の基準でリスク評価を行うのは不適切です。
最新のデータでは、35歳未満の競技アスリートにおける突然心停止(Sudden Cardiac Arrest, SCA)の年間発生率は約1/63,682とされており、特に男性、アフリカ系アメリカ人、バスケットボールやアメリカンフットボールの選手でリスクが高いことが示されています。一方で、35歳以上のマスターズアスリートでは、冠動脈疾患が主要な原因として浮上しています。
事前心臓評価の進化
12誘導心電図(ECG)スクリーニングの意義
従来の事前心臓評価(Preparticipation Cardiac Evaluation, PPE)では、問診と身体診察が中心でしたが、それだけでは感度が10〜20%と低く、心血管異常を見逃すリスクがありました。近年の研究では、12誘導ECGの導入により感度が94%まで向上することが示されており、適切な専門家による解釈があれば、心筋症やイオンチャネル異常の早期発見に役立つことが確認されています。
このように、ECGを含む心臓スクリーニングは、アスリートの心血管異常を検出するための重要なツールです。しかし、特に黒人アスリートでは、ECGの偽陽性率が高いことが知られています。このため、スクリーニングプログラムには、適切な解釈とフォローアップが不可欠です。
最新のガイドラインでは、ECGスクリーニングの実施には、専門家による解釈と適切なリソースが確保されていることが前提です。特に、黒人アスリートのスクリーニングでは、文化的な配慮や健康格差への対応が重要です。
心血管異常を持つアスリートの競技参加の考え方
心筋炎
COVID-19パンデミックは、アスリートの心臓健康に新たな課題を投げかけました。特に、SARS-CoV-2感染後の心筋炎が注目されています。従来、心筋炎の回復後は3〜6ヶ月の競技制限が推奨されていましたが、最新の心臓MRIデータによると、炎症の解消が4〜6週間で確認される場合があり、早期の競技復帰が可能であることが示されています。つまり、症状が完全に消失し、MRIで炎症が認められない場合、4〜6週間後の競技復帰も可能になりました。
この知見は、COVID-19感染後のアスリートの管理に大きな影響を与えます。特に、心臓MRIを用いた炎症の評価が重要であり、競技復帰の判断には、症状の解消と心機能の正常化が必須です。この新しいアプローチは、アスリートの早期復帰を可能にし、競技生活の継続を支援します。
肥大型心筋症(HCM)
HCMは、左心室の壁が異常に厚くなる遺伝性の心疾患で、若年アスリートの突然死の主要な原因の一つです。従来のガイドラインでは、HCMを持つアスリートは競技参加を禁止されていましたが、最新のデータでは、競技を継続したHCMアスリートの追跡調査において、SCA発生率が予想よりも低いことが報告されています。
例えば、LIVE-HCM研究では、HCMを持つアスリートが激しい運動を行っても、心臓イベントのリスクが増加しないことが報告されています。
LIVE-HCM試験は、HCM患者における激しい運動の安全性を評価するために設計された観察研究です。この試験では、1,660人のHCM患者が参加し、運動習慣と心臓イベントの関連性が調査されました。参加者は以下の3つのグループに分類されました:
- 激しい運動を行う群:全体の42%
- 中程度の運動を行う群:43%
- 運動をほとんど行わない群:16%
研究期間中、参加者は6ヶ月ごとに運動習慣や症状に関するアンケートに回答し、平均3年間の追跡調査が行われました。追跡期間中、重大な心臓イベント(全死亡、心停止、植込み型除細動器による治療を要する心室性不整脈、失神など)は、全体の約5%の参加者に発生しました。具体的には、激しい運動を行う群の4.7%、中程度または運動を行わない群の4.6%で心臓イベントが報告され、統計的に有意な差は認められませんでした。
この結果に基づき、HCMを持つアスリートでも、SDMを通じて競技参加を検討することが推奨されています。ただし、リスク評価には心臓MRIや遺伝子検査が不可欠です。
遺伝性不整脈(心筋チャネル病;QT延長症候群、CPVTなど)
心筋チャネル病(心臓チャネロパシー)は、イオンチャネルの遺伝子変異によって引き起こされる疾患群で、long QT症候群(LQTS)やカテコラミン誘発性多形性心室頻拍(CPVT)が代表例です。これらの疾患は、突然の心停止や心室細動を引き起こすリスクが高いため、アスリートの競技参加には慎重な評価が必要です。
遺伝性イオンチャネル障害を持つアスリートに関しても、従来はスポーツ禁止が基本でした。
しかし、最新の研究では、LQTSやCPVTを持つアスリートでも、適切な管理と監視の下で競技参加が可能であることが示されています。特にβ遮断薬を適切に使用すれば、運動誘発性の致死的不整脈を抑制できることが確認されています。
LQTSの場合、β遮断薬の使用や遺伝子型に応じたリスク評価が重要です。特に、LQTSタイプ1(LQT1)を持つアスリートでは、水泳中の心室性不整脈のリスクが高いため、AEDの設置や監視下での競技参加が推奨されます。
分子生物学的視点から見ると、これらの疾患は特定の遺伝子変異(例:KCNQ1、RYR2)に起因しており、遺伝子検査を用いたリスク評価が可能です。このような分子レベルの理解は、個別化された治療や競技参加の判断に役立ちます。
先天性心疾患:解剖学的および生理学的評価
先天性心疾患を持つアスリートの競技参加に関するガイドラインも更新されました。特に、解剖学的および生理学的な評価に基づいた個別化されたアプローチが推奨されています。例えば、修正大血管転位(ccTGA)やフォンタン手術後のアスリートでは、心機能や不整脈のリスクを慎重に評価する必要があります。
先天性心疾患を持つアスリートの競技参加は、疾患の種類や重症度に応じて異なります。例えば、軽度の心房中隔欠損(ASD)や心室中隔欠損(VSD)を持つアスリートは、競技参加が可能ですが、重度の大動脈狭窄や肺高血圧を持つアスリートは、競技参加が制限される場合があります。
大動脈疾患:二尖弁大動脈弁と大動脈瘤
大動脈疾患を持つアスリートの競技参加は、大動脈のサイズや疾患の進行状況に応じて慎重に評価する必要があります。特に、二尖弁大動脈弁(BAV)や遺伝性大動脈疾患(HTAD)を持つアスリートでは、大動脈解離のリスクが高いため、高強度のスポーツは避けるべきです。
最新のガイドラインでは、大動脈径が45mmを超える場合、競技参加は制限されます。ただし、BAVを持つアスリートでも、大動脈径が40〜44mmの範囲内であれば、SDMを通じて競技参加を検討することが可能です。このような個別化されたアプローチは、アスリートの競技生活を継続するための重要な指針となります。
不整脈と植込み型除細動器(ICD)
不整脈を持つアスリート、特に植込み型除細動器(ICD)を装着したアスリートの競技参加に関するガイドラインも更新されました。ICDを装着したアスリートでも、競技参加が可能であることが示されています。ただし、スポーツの種類やリスクに応じた慎重な評価が必要です。
例えば、ICDを装着したアスリートが衝突や衝撃の多いスポーツ(例:アメリカンフットボール、ラグビー)に参加する場合、ICDの損傷や誤作動のリスクが高まります。このため、SDMを通じて競技参加のリスクとベネフィットを慎重に評価することが推奨されています。
マスターズアスリート:高齢アスリートの心血管リスク
35歳以上のマスターズアスリートでは、冠動脈疾患や心房細動のリスクが高まります。特に、長年の激しい運動によって冠動脈石灰化や大動脈拡張が進行する場合があります。このため、マスターズアスリートの心血管リスク評価は、若年アスリートとは異なるアプローチが必要です。
最新のガイドラインでは、マスターズアスリートの心血管リスク評価には、冠動脈CTや心臓MRIが推奨されています。特に、冠動脈石灰化スコアが高い場合でも、高い心肺機能が保護的に働くことが示されています。このため、リスク評価には、従来のリスクスコアに加えて、運動耐容能や心機能を総合的に評価することが重要です。
緊急対応計画(EAP)の重要性
いかなる予防的アプローチも SCA を完全に防ぐことはできません。競技中の心停止に備えて、心肺蘇生法(CPR)や自動体外式除細動器(AED)の使用を含む緊急対応計画(EAP)が必須です。すべてのスポーツ施設でEAPを整備し、定期的な訓練を行うことが推奨されています。特に、競技中の心停止は、迅速な対応が生死を分けるため、EAPの重要性は計り知れません。
アスリートのための実践的提言
この声明をもとに、競技アスリートが心血管リスクと向き合いながらスポーツを続けるために、以下の実践的提言が示されました。
- 定期的な心血管評価を受ける:特に12誘導ECGのスクリーニングは簡便かつ有効であり、適切な専門家の評価を受けることが重要です。
- 共有意思決定(SDM)を活用する:一律のスポーツ制限ではなく、医師とアスリートがリスクを共有し、最適な選択をすることが推奨されます。
- 心筋炎後の復帰は慎重に行う:新しい知見を踏まえ、MRIで炎症が収束していれば4〜6週間での復帰が可能な場合があります。
- 遺伝性心疾患を持つアスリートも競技継続が可能:ただし、β遮断薬などの適切な治療と定期的なリスク評価が必須です。
- 緊急対応計画(EAP)の策定:競技会場やトレーニング施設にはAEDを常備し、迅速な対応ができる体制を整えることが求められます。
結論
本声明は、心血管疾患を持つアスリートに対するスポーツ参加の新たな指針を提示し、一律なスポーツ制限から、個別リスク評価とSDMへ移行する重要性を強調しています。競技アスリートと医療従事者が協力しながら、安全でパフォーマンスを最大化する環境を構築することが求められます。
参考文献
Kim JH, Baggish AL, Levine BD, et al. Clinical considerations for competitive sports participation for athletes with cardiovascular abnormalities: A scientific statement from the American Heart Association and American College of Cardiology. J Am Coll Cardiol. 2025;XX(X):XXX-XXX. https://doi.org/10.1016/j.jacc.2024.12.025