はじめに
心房細動(AF)は、脳卒中や死亡のリスク要因として知られていますが、近年は脳卒中がなくても認知症や軽度認知障害のリスクを上昇させることが報告され、臨床上の注目が高まっています。
また、AFが全原因性認知症や血管性認知症のみならず、アルツハイマー病(AD)を発症する確率も高め、さらに、AFはすでにADを有する患者においても認知機能の低下を進行させることが明らかになっています。
これらの知見は、AFと認知症の関係が多因子的であり、単に血栓塞栓や脳血管イベントによるものではないことを示唆しています。
今回ご紹介する研究では、AFと認知機能低下の間にある未解明の機序に対して、「脳のゴミ掃除システム」であるグリンパ系=グリアリンパ系(glymphatic system)という観点から新たな光が当てられました。
この研究は、AFが脳のグリンパ機能を障害し、それが認知機能の低下を媒介している可能性を提示し、さらにカテーテルアブレーションによりその機能が改善しうることを、非侵襲的な拡散テンソル画像(DTI)によって実証した初のヒト研究です。
グリアリンパ系(glymphatic system)=脳内クリアランス機構
グリアリンパ系とは、脳脊髄液(CSF)が動脈周囲腔(perivascular space, PVS)を通って脳実質に流入し、神経細胞の間質液を通って老廃物を回収し、静脈周囲を通じて排出する脳内クリアランス機構です。グリア細胞の一種である星状細胞が形成するトンネルと、そのトンネルを通って流れる脳脊髄液によって構成されています。この仕組みは、体内のリンパ系と同様に、脳内の老廃物処理に重要な役割を果たしています。
近年では、動物およびヒトの神経画像研究において、グリアリンパクリアランスの低下が神経毒性タンパク質(アミロイドβやタウなど)の蓄積に寄与し、認知機能障害の進行において重要な役割を果たすことが示唆されています。
特に、正常な心臓の拍動がグリアリンパ系機能および脳内の神経毒性物質のクリアランスにおいて潜在的な役割を果たしている可能性が指摘されています。PVSに沿った液体の流れは、心拍に依存する拍動性の機械的な力によって促進されていると考えられています。
一方で、不整脈によって心拍が不規則になると、血管壁の波動的な動態が乱され、細動脈の収縮期の拍動周期が破綻する可能性があります。
このシステムは、心拍に伴う動脈の拍動を動力源としており、拍動のリズムがCSF流を維持するうえで極めて重要なのです。したがって、AFのようなリズム不整は、この流れを阻害し、アミロイドβやタウなどの神経毒性物質の蓄積を促す可能性があると考えられています。
研究デザインと参加者
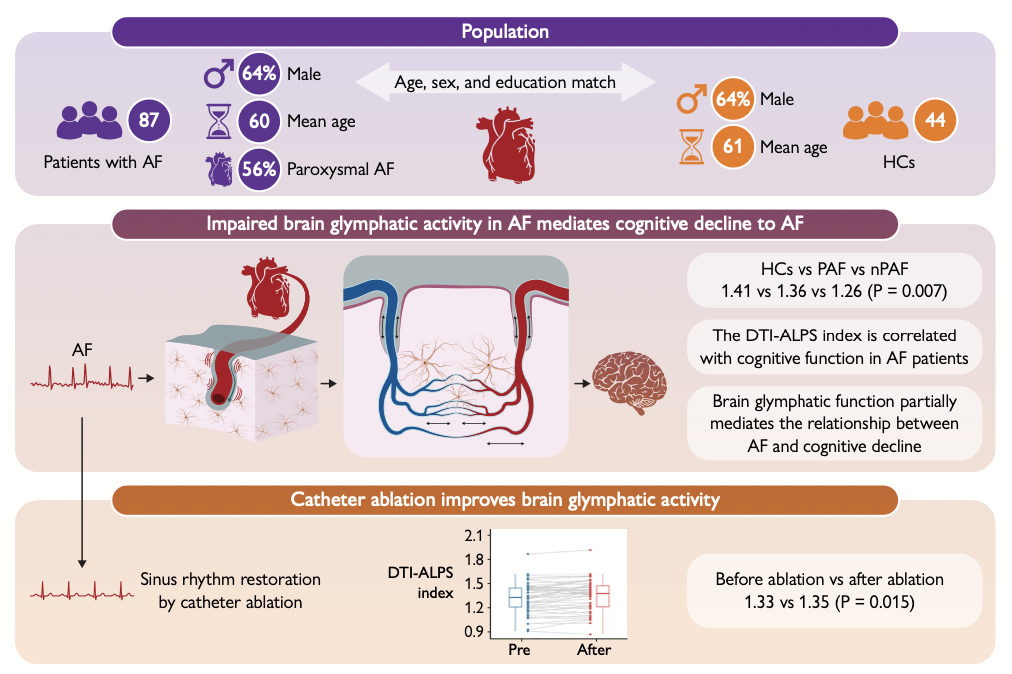
本研究は、症例対照研究および前後比較型の縦断研究として設計され、AF患者87名と健常対照(HC)44名が登録されました。AF患者は、発作性AF(PAF)と非発作性AF(nPAF)に分類され、50名がカテーテルアブレーションを受けました。全例において認知機能検査とMRIが行われ、グリアリンパ機能はDTI-ALPS index(perivascular spaceに沿った水拡散の解析)によって定量化されました。
主な結果
グリアリンパ機能の低下
AF群では、グリアリンパ機能を示すALPS indexがHC群より有意に低値でした(1.32 vs 1.41, P = .016)。特にnPAF群では最も低く(1.26)、PAF群(1.36)およびHC群との間に有意差が確認されました(P = .002および.044)。
PAF群とHC群の差は統計的に有意ではない(P = .192)ものの、PAF群でも低下傾向を示しており、中間的な値を示しています。
認知機能との関連
ALPS indexの低下は、処理速度・注意・実行機能の低下と関連していました。たとえば、Digit Span Test(DST)forwardとDST backwardのスコアはALPS indexと正の相関を示し(それぞれr = .379, P < .001;r = .374, P < .001)、Trail Making Test(TMT)やStroop Test(SCWT)でも負の相関が確認されました。
媒介分析:AF→グリアリンパ低下→認知機能障害
媒介分析では、ALPS indexがAFとTMT、DST、SCWTスコアとの間の有意な媒介因子であることが示されました。たとえばSCWT-Bでは、媒介率(Pm)が20.9%、間接効果はβ = 1.296(95%CI: 0.279–2.726)でした。
カテーテルアブレーション後のグリアリンパ機能の改善
アブレーションを受けた50名のAF患者において、術前後のALPS indexを比較した結果、有意な改善が認められました(1.33→1.35, P = .015)。特に、AF診断からの経過が短い群では改善効果がより顕著であり(10.5ヶ月 vs 48.0ヶ月, P = .023)、早期治療の意義が示唆されました。
なお、アブレーション後の認知機能の再評価は未施行のようです。
分子メカニズムの考察
AFによる拍動の不整は、脳血管壁の周期的な伸縮を乱し、グリアリンパ流の動力である動脈拍動を不規則化させます。さらに、AFに伴う慢性炎症やレニン・アンジオテンシン系の活性化により、アクアポリン4(AQP4)の偏位や機能障害が生じ、CSFの流れが阻害される可能性も指摘されています。
アクアポリン4(AQP4)とは、中枢神経系で最も豊富に存在する水チャネルタンパク質で、細胞膜に存在し、脳内の体液運動や水移動に重要な役割を果たしています。
発作性心房細動(paroxysmal AF:PAF)でもグリアリンパ機能が低下している可能性
PAF群とHC群の差は統計的に有意ではない(P = .192)ものの、PAF群でも低下傾向を示しており、中間的な値を示しています。
論文の考察部分では、以下のように言及されています。「MRI撮影前に心電図と心拍数を確認し、洞調律であることを確認した上で撮影を実施している。しかし、撮影中に一過性の無症候性AFエピソードが発生していた可能性は否定できない。また、PAFでは発作がない時間帯でも、累積的な影響によりグリアリンパ機能が低下している可能性がある。」
つまり、発作性AFは「たまに乱れるリズム」であっても、日常的に繰り返されることで、脳の拍動駆動性のCSF流に慢性的な影響を与えうると解釈されています。
拍動の周期性や整合性がグリアリンパ流の鍵となるため、たとえ一時的に洞調律であっても、長期間にわたるリズム不整の履歴(メモリー効果)が血管壁のコンプライアンスやAQP4極性化などに影響を与える可能性があります。
このように、発作性心房細動(paroxysmal AF:PAF)の患者においても、発作が起きていない洞調律時であっても、脳のグリアリンパ流(glymphatic activity)は低下している可能性が高いと考えられます。
本研究の新規性
本研究の最大の新規性は、AFが脳グリンパ系を障害し、それが認知機能低下のメカニズムの一部であることを、非侵襲的にヒトで実証した点です。また、洞調律回復によってグリアリンパ機能が改善することを画像的に示したことで、アブレーション治療の神経保護的意義に新たな視点を提供しています。
臨床的意義と実践への応用
この知見は、「AFは心臓だけでなく脳の排泄機能にも影響を与える」という新たな理解を提供します。特に、カテーテルアブレーションによる洞調律の維持は、単なる不整脈の治療にとどまらず、認知症予防にも資する可能性があります。認知症ハイリスク患者において、治療介入のタイミングを早める判断材料となりうる重要な知見です。
Limitation
- DTI-ALPSは間接的指標であり、ゴールドスタンダードであるガドリニウム造影MRIに比べて精度は劣る可能性があります。
- 心拍変動のリアルタイム計測が行われておらず、MRI中のAF発作との正確な対応は不明です。
- 本研究は無作為化試験ではなく、アブレーションを受けた症例数も限られているため、因果関係の確証は得られていません。
- アブレーション後の評価は短期間のみに限定されており、長期的な効果は今後の研究課題です。
- アブレーション後の認知機能の再評価は未施行です。
おわりに
心房細動が脳に及ぼす影響は、これまで以上に多層的であることが明らかになりつつあります。本研究は、脳の老廃物排出という観点からAFと認知症をつなぐ新たな回路を示し、早期のリズムコントロール介入が神経保護につながる可能性を浮き彫りにしました。今後は、グリアリンパ機能の定量化が認知症予防の指標となる可能性があり、脳と心臓の統合的な治療戦略が求められます。
参考文献
Guo J, Zhang Z, Meng X, et al. Atrial fibrillation catheter ablation, brain glymphatic function, and cognitive performance. Eur Heart J. 2025;46(18):1733–1743. doi:10.1093/eurheartj/ehaf036