はじめに
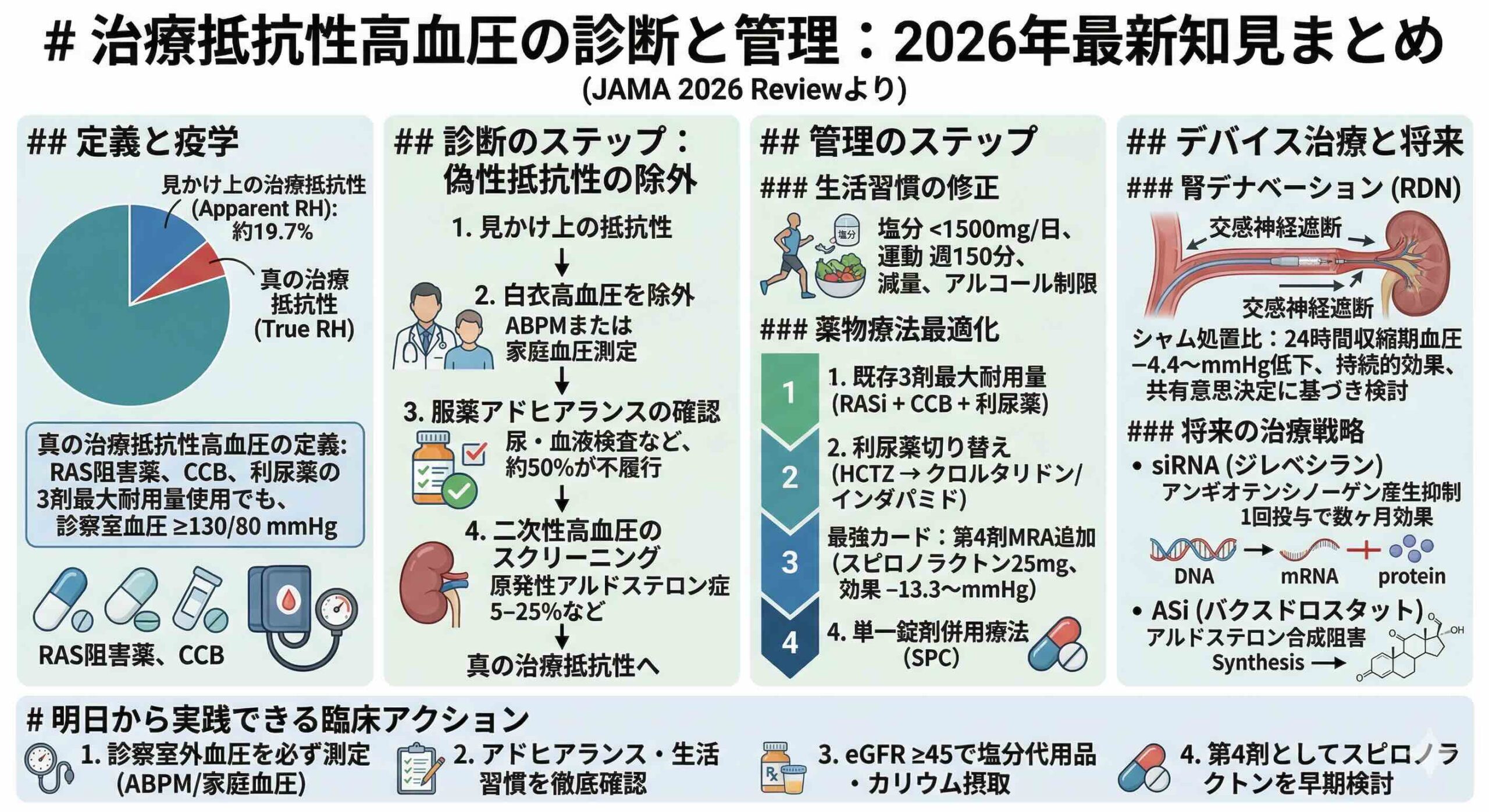
現代医療において、高血圧は依然として最大級の公衆衛生上の課題です。米国では成人女性の43.9%、男性の49.5%が罹患しており、その対策は急務となっています。中でも、複数の薬剤を投与しても目標血圧に到達しない「治療抵抗性高血圧」は、脳卒中や心不全、腎不全といった致命的な合併症に直結する非常にリスクの高い病態です。本稿では、2026年に発表された最新のJAMAレビューに基づき、見かけ上の数値に隠された真実と、分子生物学的視点を取り入れた次世代の治療戦略について詳しく解説します。
「見かけ上の治療抵抗性高血圧(apparent resistant hypertension)」19.7%の仮面を剥ぐ
臨床現場において、3剤以上の降圧薬を最大耐用量で使用しても血圧が130/80 mmHgを超えている患者、すなわち「見かけ上の治療抵抗性高血圧(apparent resistant hypertension)」は、治療中の患者の約19.7%に達します。しかし、このうち約10%だけが「真の治療抵抗性高血圧」であるという事実は驚くべきものです。残りの約半数(19.7%-10%)は、診断のプロセスで除外されるべき要素を含んでいます。
まず、最も頻度の高い落とし穴が「白衣高血圧」です。見かけ上の治療抵抗性を示す患者の約37.5%が、診察室のみで血圧が上昇するこのタイプに該当します。これを正確に判別するためには、24時間自由行動下血圧測定(ABPM)や家庭血圧測定による、診察室外での評価が絶対に欠かせません。
次に重要なのが「服薬アドヒアランス」の欠如です。驚くべきことに、抵抗性とされる患者の約50%が処方通りに薬を服用していません。患者との非難を交えない対話や、処方履歴の確認、さらには尿や血液中からの薬剤成分の直接検出といった手法が、真の病態を把握するために必要とされています。
最後に、二次性高血圧のスクリーニングです。真の抵抗性高血圧患者の5%から25%に「原発性アルドステロン症」が潜んでおり、これを見逃さないことが、根治に向けた重要なステップとなります。
(この論文では、真の治療抵抗性高血圧とは、明らかな原因疾患(二次性)が見つからないにもかかわらず、標準的な3剤併用療法に抵抗する「本態性高血圧の極めて重症な病態」と定義されています。 )
分子生物学的視点から解き明かす抵抗性の正体
なぜ一部の患者では、標準的な3剤併用療法が効かないのでしょうか。その背景には、複雑に絡み合う神経体液性因子の過剰活動が存在します。
本論文が強調するのは、不適切かつレニン非依存性の「アルドステロン過剰」です。これは単なる原発性アルドステロン症だけでなく、診断基準(カットオフ値)には至らないが血中レベルが高めの状態や、血中レベルが正常範囲内であっても、体液量に対してアルドステロンが過剰に作用している状態(低レニン)を指します。このアルドステロンの暴走は、腎臓でのナトリウム再吸収を促進し、循環血液量の増加を招きます。
これに加えて、交感神経系の過緊張、エンドセリン1やバソプレシンの過活動、さらにはナトリウム利尿ペプチド系の機能不全などが、不適切かつレニン非依存性の「アルドステロン過剰」を助長し、そして血管内皮機能の障害も生じ、血管抵抗を上昇させ、腎臓の線維化や動脈硬化を加速させます。特に食事からの過剰なナトリウム摂取(1日2300 mg以上)は、レニン活性を抑制し、レニン・アンギオテンシン系(RAS)阻害薬の治療効果を減弱させる大きな要因となります。
薬物療法のパラダイムシフト:スピロノラクトンの圧倒的力
治療抵抗性を打破するための薬物戦略は、単なる増量ではなく、病態生理に即した最適化が必要です。
まず実践すべきは、利尿薬の最適化です。一般的なヒドロクロロチアジドから、より長時間作用型で強力なクロルタリドンやインダパミドへの切り替えが推奨されます。特に腎機能が低下した症例(eGFR 30 mL/min/1.73 m2未満)では、ループ利尿薬の併用が体液管理の鍵となります。
そして、真の抵抗性高血圧に対する第4選択薬として、ミネラルコルチコイド受容体拮抗薬(MRA)であるスピロノラクトンの追加が極めて強力なエビデンスを有しています。ネットワークメタ解析によれば、スピロノラクトンの追加は、プラセボと比較して診察室収縮期血圧を13.3 mmHg、24時間収縮期血圧を8.46 mmHgも低下させます。
副作用として懸念される女性化乳房(男性の約9.1%)や性機能障害に対しては、より選択性の高いエプレレノンや、ナトリウムチャネル遮断薬のアミロライドが代替案となります。また、配合剤(Single-Pill Combination)の導入は、複雑な処方を簡略化し、血圧をさらに3.99 mmHg低下させる効果があることも見逃せません。
デバイス治療の最前線:腎デナベーションの臨床的意義
薬物療法に限界がある、あるいは副作用で継続が困難な患者に対する革新的な選択肢が、カテーテルによる「腎デナベーション」です。
この処置は、高周波や超音波エネルギーを用いて腎動脈周囲の交感神経を遮断し、レニン分泌の抑制やナトリウム排出の促進、中心交感神経活動の減衰を図るものです。10件のランダム化比較試験(RCT)を含むメタ解析では、シャム処置(模擬手術)と比較して、24時間収縮期血圧を4.4 mmHg、診察室収縮期血圧を6.6 mmHg有意に低下させることが示されました。
特筆すべきは、腎デナベーションを受けた患者の約3分の2が、収縮期血圧で5 mmHg以上の明確な反応を示すという点です。長期的にも、平均4.4年の追跡で診察室血圧が23 mmHg低下するという持続的な効果が報告されています。これは、生涯にわたる多剤併用の負担を軽減する可能性を秘めた、低侵襲なアプローチと言えます。
未来の治療戦略:siRNAとアルドステロン合成阻害薬
本論文は、現在進行中のエキサイティングな治験薬についても言及しています。
その一つが、低分子干渉RNA(siRNA)製剤の「ジレベシラン」です。これは肝臓でのアンギオテンシンノーゲン産生を遺伝子レベルで抑制する薬剤で、1回の皮下投与で数ヶ月にわたる強力な降圧効果を発揮します。第2相試験では、アムロジピンやインダパミドに追加することで、24時間収縮期血圧をさらに9.7から12.1 mmHg低下させることが確認されています。
また、選択的アルドステロン合成阻害薬である「バクスドロスタット」や「ロルンドロスタット」は、副作用となるコルチゾール合成抑制を避けつつ、血圧とアルドステロン値を直接引き下げる次世代のMRAとして期待されています。
明日から実践できる臨床アクション
専門家レベルの知識を日々の実践に活かすため、以下のステップを明日から導入してください。
ステップ1:診察室血圧だけで判断しない。
見かけ上の抵抗性の3割以上が白衣高血圧です。必ずABPM、最低でも1週間の家庭血圧(1日2回、各2回測定)を実施し、真の抵抗性であることを確認してください。
ステップ2:薬剤の見直し。
降圧効果を阻害するNSAIDs、ステロイド、抗うつ薬、そして過度のアルコール摂取がないか徹底的にチェックします。これらを除去するだけで、困難だったコントロールが可能になる場合があります。
ステップ3:ナトリウム制限とカリウム摂取。
1日ナトリウム摂取量を1500 mg未満に制限するよう具体的に指導してください。一方で、eGFRが45以上であれば、塩分代用品やカリウム摂取の増加が、収縮期血圧をさらに4.6 mmHg低下させる強力な手段となります。
ステップ4:スピロノラクトンの早期検討。
eGFRが45以上、血清カリウムが4.5 mmol/L以下であれば、迷わずスピロノラクトン25 mgの追加を検討してください。これが現時点で最も強力な抵抗性打破のカードです。
新規性とlimitation
本レビューの新規性は、2025年に改訂された最新のAHA/ACCガイドラインを完全に反映し、かつジレベシランなどの最新の治験データまでをも統合した包括的な管理アルゴリズムを提供している点にあります。これまでの「3剤、だめなら4剤」という単純な加算から、分子メカニズムに基づいた「診断の精密化と多角的な介入」へと治療の質を一段階引き上げています。
一方で、リミテーションも存在します。掲載された多くのRCTは、厳格に選択された患者群(比較的低リスクや若年層)を対象としており、複数の併存疾患を持つ高齢者やステージ4以上の重症CKD患者における安全性や効果については、まだ十分なデータが揃っていません。また、腎デナベーションの効果を予測する決定的なマーカーが未だ確立されていないことも、今後の課題として残されています。
治療抵抗性高血圧の克服は、医師と患者のパートナーシップ、そして最新の科学的知見の融合によってのみ成し遂げられます。数値の裏にある生理学的真実を見抜くことが、患者の命を守る第一歩となるのです。
参考文献
Azizi M, Vongpatanasin W, Fisher NDL, Mahfoud F, Amar L, Kirtane AJ. Diagnosis and Management of Resistant Hypertension: A Review. JAMA. 2026. doi:10.1001/jama.2026.1221
補足:不適切かつレニン非依存性の「アルドステロン過剰」
不適切かつレニン非依存性のアルドステロン過剰は、治療抵抗性高血圧の病態生理において中心的な役割を果たしています 。通常、塩分摂取や体液量が増大すればフィードバック機構によりレニン・アンギオテンシン系が抑制されますが、抵抗性患者ではこの系が破綻しています 。
以下に、そのフィードバック機構を阻害する主な要因を整理します。
1. 食事因子による体液量と電解質の不均衡
- ナトリウムの過剰摂取 1日 2300 mg(塩分5.8g) 以上の過剰な食塩摂取は、血漿レニン活性を低下させます 。本来ならば同時にアルドステロンも抑制されるべきですが、抵抗性患者では分泌が持続し、ボリュームオーバーロード(体液過剰)を招きます 。この状態はRAS阻害薬の有効性を減弱させ、より高用量または多種類の利尿薬を必要とする悪循環を生み出します 。
- カリウムの摂取不足 1日 1500 mg 未満の低カリウム摂取は、腎臓におけるナトリウム保持を促進します 。また、血管緊張度を直接的に高めることで血圧上昇に寄与します 。
2. 合併疾患による神経ホルモン系の活性化
- 閉塞性睡眠時無呼吸(OSA) OSAは、交感神経の過緊張(オーバードライブ)を引き起こします 。これにより、レニン・アンギオテンシン・アルドステロン系(RAAS)が体液量に関わらず不適切に活性化され、血管内皮機能障害やさらなる体液貯留を誘発します 。
- 肥満と代謝因子 肥満は、交感神経やエンドセリン1、バソプレシンの過活動と密接に関連しており、これらがナトリウム利尿ペプチド系の活性低下と相まって、血管抵抗の増大と腎臓の線維化を促進します 。
3. 外因性物質による生理学的干渉
- 薬剤による直接的・間接的作用 非ステロイド性抗炎症薬(NSAIDs)や一部の抗うつ薬(SNRIなど)は、腎血流量を変化させる、あるいは交感神経を刺激することで、正常な血圧調節メカニズムを阻害します 。また、ステロイドや合成エストロゲンもRAASの活性化やミネラルコルチコイド過剰状態に関連します 。
- 偽性アルドステロン症を引き起こす物質 リコリス(甘草)に含まれるグリチルリジンなどは、アルドステロン受容体を刺激することで、実際にはアルドステロンが過剰でなくても体液貯留と血圧上昇を引き起こし、フィードバック系を攪乱します 。
4. その他の神経体液性因子の暴走
アルドステロン以外にも、エンドセリン1、バソプレシン、交感神経系の過活動、そして血管内皮機能の低下が複雑に絡み合っています 。これらは血管の柔軟性(コンプライアンス)を損なわせ、動脈硬化や腎臓の線維化を加速させる要因となります 。
結論
治療抵抗性高血圧におけるフィードバック機構の不全は、単一の原因ではなく、過剰な塩分摂取、OSAなどの合併症による神経刺激、そして外部薬剤による干渉が重なり合った結果です 。これらによりアルドステロン分泌がレニンの制御から切り離された「レニン非依存性の過剰状態」となり、標準的な治療を困難にしています 。
この病態生理を踏まえると、生活習慣の徹底した修正と、不適切なアルドステロン作用を直接遮断するスピロノラクトンの追加が極めて論理的な選択となります 。