はじめに
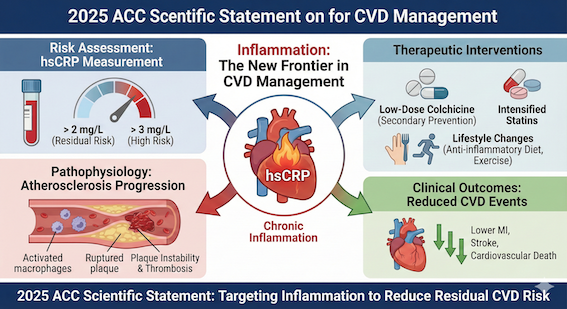
長年、心血管疾患(CVD)予防の主戦場は低比重リポ蛋白コレステロール(LDL-C)の低下にありました。しかし、強力なスタチン療法によってLDL-Cを極限まで下げてもなお、再発を繰り返す患者が絶えません。2025年に発表されたACC(米国心臓病学会)の最新科学声明は、そのミッシングリンクが「慢性炎症(chronic low-grade inflammation)」にあることを決定づけました。本稿では、この「静かなる火種」をどのように評価し、制御すべきか、声明が示す新時代の戦略を詳細に解説します。
コレステロール管理の限界と残余炎症リスクの発見
これまで心血管疾患(CVD)のリスク管理の主役は脂質低下療法でした。しかし、今回の声明は、脂質が十分に管理されている患者においてさえ、炎症がイベントの強力な予測因子であり続けていることを明確に示しています 。
声明の中で強調されているのが「残余炎症リスク(Residual Inflammatory Risk)」という概念です 。これは、スタチン治療によってコレステロール値が目標を達成していても、高感度C-reactive protein(hsCRP)が2 mg/L以上を示す状態を指します 。
CRP(C-reactive protein)とは、炎症が起きたときに主に肝臓で作られて血中に増えるタンパク質で、体内の「炎症の強さ」の目安になります。一般的には感染症(とくに細菌)、膠原病、組織障害などで上がります。hsCRP(高感度CRP)は、通常のCRPでは拾いにくいごく低い濃度まで測れるCRP検査で、微弱な慢性炎症の把握に向きます。
3万人以上のスタチン治療患者を対象とした最近の統合解析では、hsCRPは将来の血管イベントや心血管死の予測において、低比重リポ蛋白(LDL)コレステロールと同等、あるいはそれ以上に強力な指標であることが判明しました 。つまり、コレステロールという燃料を減らすだけでは不十分であり、血管というインフラを焼き尽くそうとする炎症という火を消さなければならないというパラダイムシフトが、今まさに起きているのです。
分子生物学的機序
炎症が心血管系を蝕むメカニズムは、精密な分子生物学的カスケードによって説明されます。中心となるのは、自然免疫系における「IL-1βからIL-6、そしてCRPへと至る経路」です。
動脈壁内に蓄積したコレステロール結晶や酸化ストレスは、マクロファージ内のNLRP3インフラマソームを活性化します。これにより活性化されたIL-1βが放出され、肝臓でのIL-6産生を誘導、最終的に急性期反応タンパクであるCRPの血中濃度を上昇させます。この経路は、内皮細胞の機能不全を招き、白血球の動員を促進し、プラークの線維性被膜を薄くすることで、脆弱なプラーク(Vulnerable Plaque)を作り上げます。
局所から全身へ:歯周病と血管周囲脂肪が導く病態
炎症の火種は、必ずしも血管そのものにあるわけではありません。声明は、歯周病、内臓脂肪、喫煙、不健康な食事といった要因が、どのように血管の炎症を助長するかを「パラインフラメーション(Parainflammation)」という概念を用いて解説しています 。パラインフラメーションとは、組織が低レベルの持続的なストレスにさらされた際に生じる、慢性的な適応応答の状態です 。完全な免疫活性化には至らないものの、細胞機能を阻害する低レベルの炎症状態を指します。
例えば、歯周病菌による局所の炎症は、持続的にサイトカインを放出し、前述の肝臓増幅ルートを介して全身の血管を蝕みます 。
また、内臓脂肪の蓄積も同様で、脂肪組織自体が巨大な内分泌器官として炎症性物質を撒き散らします 。
特に注目すべきは「血管周囲脂肪(PVAT)」です 。冠動脈の外側を包む脂肪組織が炎症を起こすと、そこから直接サイトカインが血管壁に浸透し、プラークの形成や破綻を促します 。
「外敵(病原菌)」がいないのに、自分の細胞や組織が受けている「ストレス」を免疫系が感知して反応してしまうのです。
本来、急性ストレスに対する救済システムである免疫が、慢性炎症(=慢性ストレス)に作用することで、結果的に悪影響を及ぼしてしまいます。
画像診断とクローン性造血(CHIP)
血管周囲脂肪(Perivascular fat )
診断技術も血清マーカーの枠を超えつつあります。CT画像から得られる「血管周囲脂肪減衰指数(Perivascular fat attenuation index;FAI)」は、動脈硬化が顕在化する前の段階で、冠動脈の炎症を捉えることが可能です。上記にもでてきた、この血管周囲脂肪(Perivascular fat)とは、「冠動脈の壁(外膜)に密着しているごく薄い層の脂肪」のことです。これはカルシウムスコア以上に将来のイベントを予測する可能性を秘めています。
クローン性造血(clonal hematopoiesis of indeterminate potential ;CHIP)
さらに、血液学的な視点として「不明な原因によるクローン性造血(clonal hematopoiesis of indeterminate potential ;CHIP)」の重要性が強調されています。CHIPとは、造血幹細胞の中に「後天的に」生じたコピーミス(体細胞変異)、遺伝子変異です。TET2やDNMT3Aといった遺伝子の体細胞変異によって生じる血球クローンの増殖は、心血管リスクを2倍、心不全の死亡リスクを3倍以上に高めます。これらの変異を持つ個体ではマクロファージが過剰に炎症性サイトカインを放出しており、抗IL-1β抗体(カナキヌマブ)の治療効果が非変異者よりも顕著であった(MACEの相対リスク62%減少)という知見は、精密医療(プレシジョン・メディシン)の到来を予感させます。
抗炎症療法:コルヒチンとスタチンが切り拓く地平
本声明は、複数の大規模臨床試験の結果をもとに、具体的な治療戦略を提示しています。本声明は総説的性質を持つため、主要な引用試験の概要をここにまとめます。
- 一次予防におけるJUPITER試験P:LDL-Cが130 mg/dL未満と正常だが、hsCRPが2.0 mg/L以上の健康な男女17,802人I:ロスバスタチン 20mg投与C:プラセボO:心血管イベントの発生結果:介入群で主要エンドポイントが47%減少しました(HR 0.53)。これは「コレステロールが低くても炎症が高い」群に対する介入の有効性を決定づけました。
- 二次予防におけるコルヒチン(COLCOT試験、LoDoCo2試験)慢性安定期の動脈硬化性疾患患者において、安価な抗炎症薬である低用量コルヒチン(0.5mg/日)の投与は、血管イベントのリスクを約25%減少させました。これにより、コルヒチンは心血管イベント抑制を目的としてFDAに承認された初の抗炎症薬となりました。
一方で、CLEAR-SYNERGY試験のように、急性心筋梗塞直後の介入では効果が認められなかったケースもあり、炎症を抑える「タイミング(Timing of Taming)」が極めて重要であることが浮き彫りになっています。
生活習慣という抗炎症戦略
薬物療法のみならず、生活習慣そのものが強力な「抗炎症薬」として機能します。
食事
食事に関しては、地中海食やDASH食が推奨されます。果物、野菜、全粒穀物、ナッツ、オリーブオイルの摂取は、全身の炎症負荷を軽減します。特にオメガ3脂肪酸(EPA/DHA)については、1日1g以上の摂取が心筋梗塞や心血管イベントのリスクを線形的に減少させることが示唆されています。
そのメカニズムとして、EPA/DHAの代謝産物である「特殊分化炎症収束性脂質メディエーター(Specialized pro-resolving lipid mediator;SPM)」が注目されています。SPMは、単に炎症を抑えるだけでなく、エフェロサイトーシス(死細胞の清掃機能)を促進し、炎症を能動的に終息させる役割を担っています。
運動
また、週150分の中強度の運動は、脂肪組織からのサイトカイン放出を抑制し、インスリン感受性を改善することでhsCRPを低下させます。
本声明の新規性と今後の課題(Limitation)
本声明の新規性は、これまで「指標」でしかなかったhsCRPを、治療の優先順位を決定する「必須のスクリーニング項目」へと格上げした点にあります。「測っていないものは治療できない(Clinicians will not treat what they do not measure)」という強いメッセージは、今後の臨床ガイドラインを大きく塗り替えるでしょう。
しかし、いくつかのLimitation(限界)も存在します。
第一に、抗炎症薬の一次予防における大規模なランダム化比較試験は未だ不足しており、健康な個人に対して長期間の薬物介入を行うことのベネフィットとリスク(感染症リスクなど)のバランスは完全に解明されていません。
第二に、CLEAR-SYNERGY試験の結果に見られるように、急性期の炎症と慢性の低悪性度炎症では介入に対する反応が異なり、最適な投与開始時期についての議論が続いています。
第三に、CHIPのような先端的なリスク因子のスクリーニングを、一般的な臨床現場でどのように実装していくかというコストと体制の課題が残されています。
明日からの臨床と生活への提言
本声明から導き出される、明日から実践すべきアクションは以下の通りです。
- hsCRPのルーチン測定:高血圧や脂質異常症の患者において、hsCRPを測定してください。(※ただし、hsCRPは、日本では保険適応外です)
3.0 mg/Lを超える場合は、たとえコレステロール値が目標内であっても、リスクが高いと認識する必要があります。 - 治療の強化hsCRPが2.0 mg/L以上で推移する安定期動脈硬化患者に対しては、既存の脂質低下療法に加え、低用量コルヒチンの併用を検討してください。(※ただし、日本では保険適応外です)
- ライフスタイルの処方患者に対し、週150分の運動、禁煙、そして魚類を中心とした抗炎症食の摂取を具体的に推奨してください。これらは単なる健康習慣ではなく、分子レベルで炎症の火を消す直接的な治療介入です。
炎症の火種を放置せず、適切にコントロールすること。それが2025年以降の循環器診療における、最も重要なパラダイムシフトとなります。
参考文献
Mensah GA, Arnold N, Prabhu SD, Ridker PM, Welty FK. Inflammation and cardiovascular disease: 2025 ACC scientific statement: a report of the American College of Cardiology. J Am Coll Cardiol. 2025;XX:XXX-XXX. (doi: 10.1016/j.jacc.2025.08.047)
補足:日本の保険診療で一般的なCRP測定を用いて慢性炎症(心血管リスク)を評価できるのか?
単位換算とリスクの境界線
日本の臨床現場では単位として mg/dL が使われますが、国際的な基準(ACC声明など)では mg/L が標準です 。この2つの単位には10倍の差があります。
- 換算式: 1.0 mg/dL = 10 mg/L
- 低リスク: 0.1 mg/dL 未満(1.0 mg/L 未満)
- 平均的リスク: 0.1 〜 0.3 mg/dL(1.0 〜 3.0 mg/L)
- 高リスク: 0.3 mg/dL 超(3.0 mg/L 超)
日本の一般的な検査(LA法など)で 0.01 mg/dL 単位まで測定できる場合、実質的に高感度CRP(hsCRP)と同等の精度でこれらの境界線を判別することが可能です。
「残余炎症リスク」の重要性
今回の声明で最も強調されているのが 残余炎症リスク(Residual Inflammatory Risk) です 。
- 定義: LDLコレステロールが十分に管理されているにもかかわらず、炎症値が持続的に高い状態を指します。
- 基準値: 0.2 mg/dL 以上(2.0 mg/L 以上)。
- 臨床的意義: スタチン治療を受けている患者において、この基準を超える炎症がある場合、再発性心筋梗塞や心血管死の強力な予測因子となります。
日本のCRP値を用いた評価の実践
高感度専用の検査項目名でなくとも、以下の点に注目することで慢性炎症の評価が可能です。
- 0.1 mg/dL 刻みの変化に注目: 通常の健診で「0.3 mg/dL 以下は正常」とされていても、0.1 なのか 0.2 なのかによってリスク評価が変わります 。
- 測定のタイミング: 慢性炎症を評価するためには、風邪や怪我などの急性疾患がない、安定した状態で測定する必要があります。
- 再確認の原則: 数値が 1.0 mg/dL (10 mg/L) を超える場合は、一時的な急性炎症の可能性が高いと考えます。その際は2〜3週間後に再測定し、低い方の値をリスク評価に使用することが推奨されています。
留意点
- 感度の限界: 測定機器の限界値が 0.1 mg/dL までである場合、0.05 などのより微細な変動を捉えることはできず、真の低リスク群の特定には限界があります。
- 画像指標との併用: 血清マーカーだけでは血管局所の炎症を完全には把握できません。将来的な実用化が期待される血管周囲脂肪指標(FAI)などの画像バイオマーカーとの統合的な評価が望まれます。
- 原因の特定: 高い数値が出た場合、それが歯周病、肥満、喫煙、あるいはクローン性造血(CHIP)のどれに起因するのかを特定し、個別に介入する必要があります。
補足のまとめ
日本の保険診療におけるCRP測定であっても、0.01 mg/dL 単位の精度があれば、ACCが推奨する心血管リスク評価に十分活用できます。「0.2 mg/dL 以上」 を一つの警戒ライン(残余炎症リスク)として捉え、ライフスタイルの改善や治療の強化に繋げることが重要です。