はじめに
現代の糖尿病治療および代謝疾患のマネジメントにおいて、グルカゴン様ペプチド1受容体作動薬(GLP-1 receptor agonists, 以下GLP-1RA)は、インスリンや経口血糖降下薬に次ぐ“第3の軸”として注目されています。また肥満治療薬としても確立されつつあります。
GLP-1は、「プログルカゴン」と呼ばれるひとつの大きな前駆体タンパク質から作られるホルモンです。このプログルカゴンは、腸のL細胞や脳幹に存在する孤束核(nucleus of the solitary tract, NTS)の神経細胞など、特定の細胞で作られます。これらの細胞では、酵素によってプログルカゴンが切り出され、GLP-1という活性のあるホルモンに変わります。GLP-1はインスリン分泌促進、グルカゴン抑制、胃内容排出遅延、食欲抑制といった多面的な作用を持ちます。
一方で、GLP-1は生体内半減期が約2分間と極めて短く、DPP-4酵素によって急速に不活性化されるという課題がありました。この課題に対し、研究者たちは構造修飾やペプチド改変により、安定性・作用時間・受容体親和性を高めたGLP-1RAを開発してきました。本稿では、これらのGLP-1RAの分子構造・薬理学的特性・臨床試験データをもとに、その多様な可能性について解説します。
分子生物学的基盤:GPCRとシグナル伝達の深層
GLP-1受容体(GLP1R)はGタンパク共役受容体(GPCR)に分類されます。GLP-1がGLP1Rに結合すると、細胞内でcAMPが増加し、Protein Kinase A(PKA)が活性化されます。この経路を通じて、インスリン分泌が誘導されるとともに、肝臓でのグルコース産生が抑制されます。
セマグルチド(semaglutide)やリラグルチド(liraglutide)などのGLP-1RAは、この受容体に対して内因性GLP-1よりも数倍高い結合親和性を示します。これが、1週間に1回の投与で十分な効果を持続させる薬効の鍵です。
また、これらのGLP-1RAは、単に膵β細胞に作用するだけでなく、中枢神経系、胃、心血管系、腸管上皮など多様な部位に影響を及ぼします。こうした「プレイオトロピック効果(Pleiotropic effects)」は、GLP-1RAが肥満、NASH、神経変性疾患にまで応用可能な理由です。
GLP-1の多面的作用と臓器間クロストーク
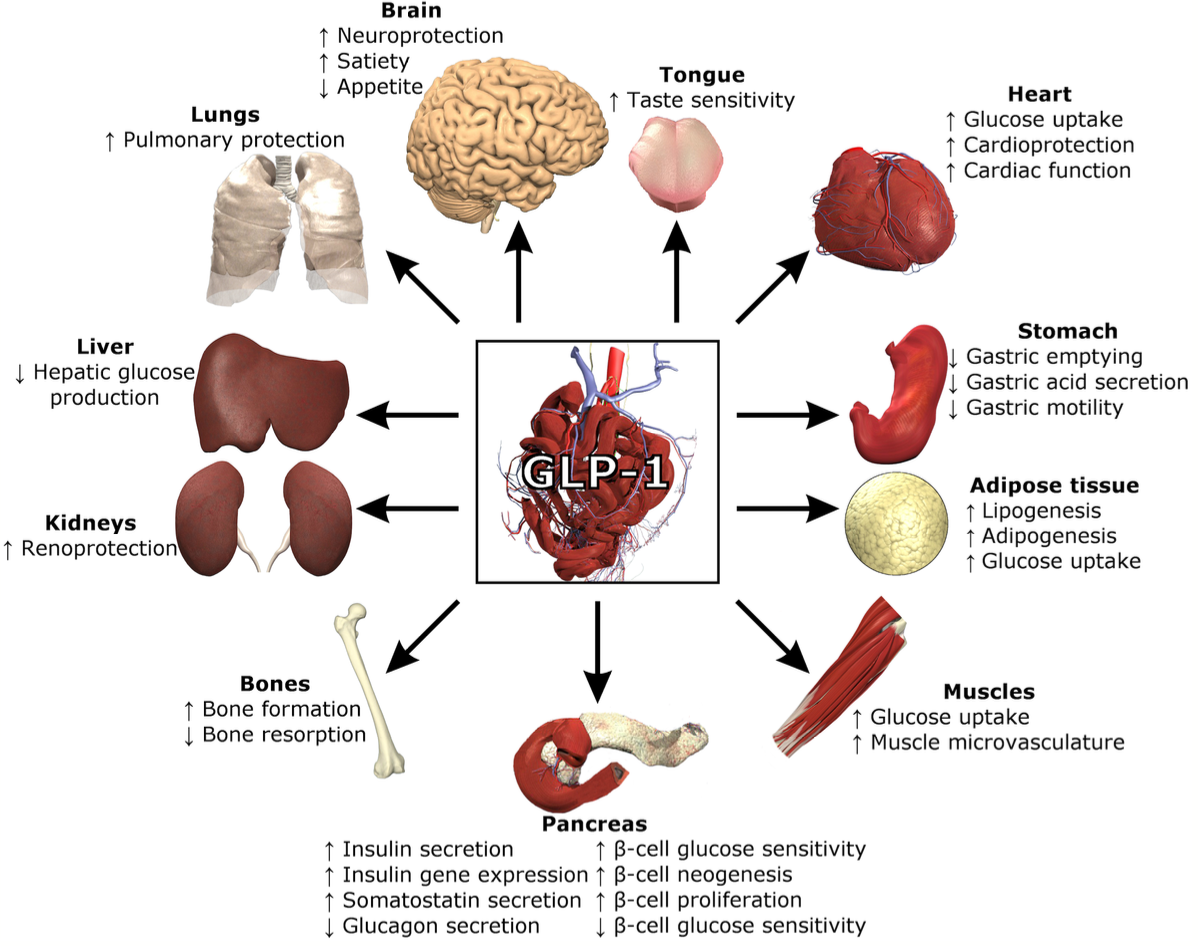
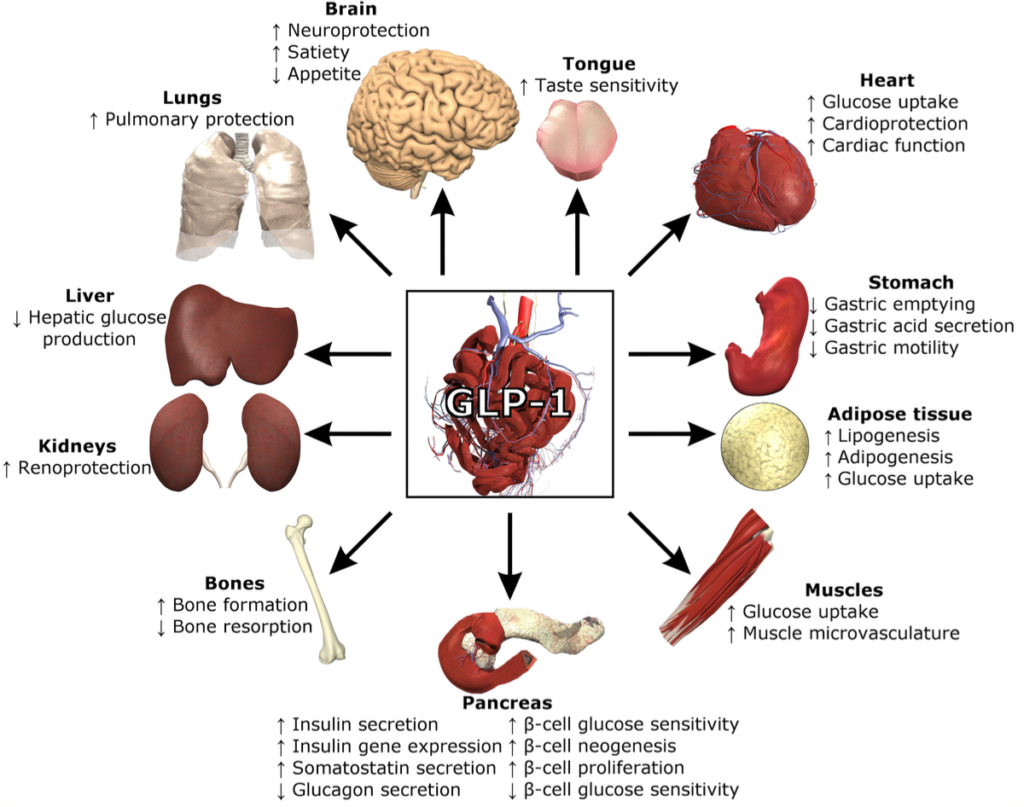
先に言及した通り、GLP-1は単なるインスリン分泌促進ホルモンではなく、複数の臓器と機能的に連携するホルモンネットワークのハブとして働いています。その作用は以下のように多岐にわたります。
膵臓(β細胞・α細胞)
GLP-1は膵島のβ細胞に作用し、血糖依存的にインスリン分泌を促進します。一方、α細胞に対してはグルカゴン分泌を抑制し、肝臓での糖新生やグリコーゲン分解を間接的に抑制します。これにより、血糖の上昇を二重に制御することが可能となります。
中枢神経系(視床下部・脳幹)
GLP-1は脳にも作用し、視床下部の摂食中枢に働きかけて食欲を抑制し、満腹感を促進します。また、報酬系への影響も報告されており、嗜癖的な食行動やドパミン経路との関連も注目されています。GLP-1受容体は海馬や大脳皮質にも発現しており、認知機能や気分にも関与する可能性が示唆されています。
胃・腸管
GLP-1は胃排出を遅延させ、食後高血糖を抑える効果を持ちます。また、十二指腸や小腸において栄養素の吸収速度を調整する作用もあります。これらの効果は、胃腸のモーター機能に対する内分泌調節として重要です。
心血管系
GLP-1受容体は心筋や血管内皮にも発現しており、心拍出量の改善、心筋保護、血圧低下などの作用が報告されています。リラグルチドやセマグルチドでは、主要心血管イベント(MACE)を有意に減少させた臨床試験(LEADER、SUSTAIN-6)が存在し、循環器疾患への応用可能性が臨床的にも裏付けられています。
肝臓(間接的作用)
肝臓自体にはGLP-1受容体が少ないとされていますが、インスリン・グルカゴン分泌への調整を介して、肝臓での糖新生の抑制や脂質代謝の改善に寄与しています。また、NASH患者において肝脂肪やALTの改善が認められています。
脂肪組織と骨格筋
GLP-1RAはインスリン感受性を向上させることで、骨格筋や脂肪細胞におけるグルコース取り込みを増加させます。さらに、炎症性サイトカインの低下や脂肪組織マクロファージの抑制を通じた抗炎症作用も報告されています。
なぜこの多面的作用が重要なのか?
GLP-1の作用は、単一の病態(例:高血糖)を対象とするのではなく、代謝症候群という複合疾患の「ハブ」として、多臓器にまたがる病態生理を調整します。糖尿病患者における肥満、高血圧、脂肪肝、心血管疾患、神経機能低下は相互に関連し合っています。そのすべてに影響を及ぼせる可能性のあるGLP-1RAは、「臓器間クロストークの調整薬」と表現しても過言ではありません。
薬物動態と分子構造
各GLP-1RAは、構造修飾により分子量・Tmax・半減期が異なり、投与間隔や臨床応用に差異があります。
- セマグルチド:脂肪酸側鎖の導入により、半減期は約7日、週1回投与。Tmaxは1.5時間。
- リラグルチド:アルブミン結合型で、半減期は11~15時間。Tmaxは約10時間、1日1回投与。
- デュラグルチド:IgG融合タンパク構造で分子量が大きく、Tmaxは48時間、半減期は5日。
- エキセナチド:Gilaモンスターの唾液由来のexendin-4を基にした薬剤で、DPP-4耐性。
これらの設計の違いが、患者のアドヒアランスや副作用プロファイル、費用対効果に影響を与えます。
セマグルチドの卓越性
セマグルチドに関する臨床試験は2017年以降だけで53件に達し、その効果と安全性が多角的に検証されてきました。
- STEP試験では、非糖尿病の肥満者に対する体重減少効果が12.4%と報告されました。
- 一方で、リラグルチドでは5.4%の体重減少に留まりました。
- セマグルチドのコスト効率は1%減量あたり1845ドル、リラグルチドは3256ドルであり、経済的にも優れています。
HbA1cの低下効果についても、セマグルチドは0.9~1.8%の改善を示しており、心血管イベントリスクの低減(SUSTAIN-6試験)も報告されています。
デュアルアゴニスト:チルゼパチド(tirzepatide)の登場
近年注目されるのが、GIP/GLP-1のデュアルアゴニストであるティルゼパチドです。40週のRCTでは、セマグルチドに比べてHbA1cをさらに0.36%多く低下させ、体重減少も上回りました。
β細胞機能、インスリン感受性、肝臓でのグルカゴン抑制といった糖尿病の病態生理の複数経路にアプローチする新しい機序は、現在、主流になりつつあります。
GLP-1RAの多面的効果
GLP-1RAは、以下のような幅広い適応が現在も試験されています。
- 非アルコール性脂肪性肝炎(NASH):肝脂肪量・炎症・線維化の抑制が報告されています。
- 多嚢胞性卵巣症候群(PCOS):メトホルミンとの併用によりBMIとインスリン抵抗性の改善。
- 神経疾患:エキセナチドはパーキンソン病におけるドパミン細胞保護作用が示唆されています。
- 高血圧・腎機能:体重減少に伴う血圧低下、腎保護作用も報告されつつあります。
- 睡眠時無呼吸症候群
おわりに
GLP-1RAは、糖尿病治療の枠を超えて、肥満、NASH、神経変性疾患、内分泌異常など、次世代の代謝医療の中核を担う存在になりつつあります
専門的な理解を深めることで、単なる「注射薬」ではなく、「全身の代謝を設計する精密医療ツール」として活用する時代がすでに始まっています。
参考文献
Mariam Z, Niazi SK. Glucagon-like peptide agonists: A prospective review. Endocrinol Diab Metab. 2024;7:e462. doi:10.1002/edm2.462
追記:GLP-1RAの多面的メカニズム:詳細
1. 血糖調節作用
β細胞への作用
- GLP-1RAは、GLP-1受容体(GLP-1R)を介してβ細胞内でcAMPを増加させ、以下の経路を活性化する:
- PKA経路:インスリン遺伝子発現促進、インスリン分泌促進。
- EPAC-Rap1経路:顆粒の分泌促進。
- PI3K/Akt経路:細胞生存と増殖、抗アポトーシス効果。
- 結果:グルコース依存的インスリン分泌の増加、β細胞の保護(増殖促進・アポトーシス抑制)。
α細胞への作用
- 直接作用:GLP-1Rの発現は少ないが、cAMP/PKA経路によってグルカゴン分泌を抑制。
- 間接作用:
- インスリンによるフィードバック抑制。
- δ細胞からのソマトスタチン分泌促進による抑制。
δ細胞との相互作用
- GLP-1はδ細胞のGLP-1Rを活性化 → ソマトスタチン分泌↑
- ソマトスタチンはα細胞とβ細胞の両方に抑制的に作用 → グルカゴンとインスリンの過剰分泌を防止。
2. 胃排出抑制・食欲抑制作用
胃腸系への作用
- GLP-1RAは胃の蠕動運動を抑制し、胃内容物の排出を遅延。
- 迷走神経の抑制的調節。
- 小腸に到達する栄養素の速度を調節 → 血糖上昇を緩やかに。
中枢神経系への作用
- 視床下部のGLP-1Rを介し摂食抑制:
- POMC/CARTニューロン活性化 → 満腹感増強。
- NPY/AgRPニューロン抑制 → 空腹感抑制。
- 満腹感の増強によるカロリー摂取抑制 → 体重減少。
3. 抗炎症・免疫調節作用
マクロファージに対する作用
- GLP-1Rはマクロファージにも発現し、cAMP/PKA/CREB経路を介して抗炎症遺伝子の発現を促進、炎症性サイトカイン(TNF-α, IL-6, IL-1β)を抑制。
- NF-κB経路の抑制により関節炎や動脈硬化性炎症を緩和。
軟骨細胞や滑膜細胞に対する効果(OAなど)
- GLP-1RAはJNK/NF-κBシグナルの抑制によって細胞のアポトーシス・肥大化・繊維化を防ぎ、OA(変形性関節症)の進行を抑制。
4. 心血管保護作用
心筋・血管内皮細胞への作用
- GLP-1Rは心筋細胞・血管内皮細胞にも発現し、PI3K/Akt経路を介して:
- 抗アポトーシス作用。
- 血管拡張作用(NO合成促進)。
- 酸化ストレス軽減。
- 臨床試験では、心不全リスクや動脈硬化進展の抑制効果も報告。
5. 神経保護作用
神経変性疾患(例:AD, PD)における作用
- GLP-1RAは中枢神経に直接作用し、神経細胞の生存を促進。
- ミクログリア活性の抑制・酸化ストレス低下によって、炎症性神経変性を緩和。
- 脳内インスリン感受性の改善 → アルツハイマー病の「第3型糖尿病」仮説とも整合。
6. 肝臓・脂肪組織への作用(NAFLD/NASH関連)
- 肝臓において脂肪蓄積を減少させ、インスリン抵抗性を改善。
- 肝星細胞やKupffer細胞の活性抑制を通じて肝線維化を抑制。
- 腸内GLP-1R経由で胆汁酸代謝や腸肝軸の調整にも関与。
7. 骨格筋・脂肪組織での糖取り込み促進
- GLUT4の膜輸送促進による筋肉でのグルコース取り込み増加。
- 脂肪組織では脂肪酸酸化を促進し、脂肪蓄積を抑制。
8. がん領域での可能性(研究段階)
- 一部のがんでGLP-1Rが発現しており、増殖抑制やアポトーシス誘導が観察されている。
- ただし、長期使用での安全性、発がん性リスクとの関係については今後の検証が必要。
補足:メカニズム別に関与する主なシグナル経路
| メカニズム | 関与する経路・因子 |
|---|---|
| インスリン分泌促進 | GLP-1R → cAMP → PKA/EPAC → CREB、PI3K/Akt |
| グルカゴン抑制 | cAMP → PKA → KATPチャネル調整、ソマトスタチン経由 |
| 食欲抑制 | 視床下部GLP-1R → POMC/CART活性化・NPY抑制 |
| 抗炎症 | cAMP/PKA/CREB、NF-κB阻害 |
| 心筋保護 | PI3K/Akt → Bcl-2発現↑、NO合成酵素↑ |
| 神経保護 | Akt/CREB、ミクログリア抑制 |
このように、GLP-1RAは単なる血糖降下薬ではなく、全身性の多面的治療効果を持つ薬理学的プラットフォームとして再評価されています。
追記の参考文献
Zheng Z, Zong Y, Ma Y, Tian Y, Pang Y, Zhang C, Gao J. Glucagon-like peptide-1 receptor: mechanisms and advances in therapy. Signal Transduct Target Ther. 2024 Sep 18;9(1):234. doi: 10.1038/s41392-024-01931-z. PMID: 39289339; PMCID: PMC11408715.