はじめに
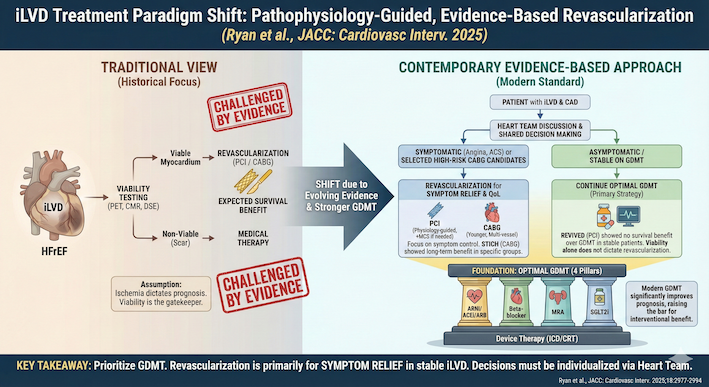
虚血性心疾患を背景とした左室機能不全(Ischemic Left Ventricular Dysfunction:iLVD)は、駆出率の低下した心不全(HFrEF)の最も主要な原因です。非虚血性心筋症と比較して、虚血性病因は短期的にも長期的にも予後不良であることが知られています。統計によれば、心不全患者の40パーセントから60パーセントに冠動脈疾患が併存しているにもかかわらず、実際に詳細な冠動脈評価が行われているのはわずか10パーセントから20パーセントに過ぎません。この乖離こそが、救えるはずの心筋を看過している可能性を示唆しています。しかし、その治療の要である血行再建術、すなわち冠動脈バイパス術(CABG)や経皮的冠動脈インターベンション(PCI)が、果たしてすべての患者に福音をもたらすのか。近年の大規模臨床試験は、この問いに複雑な答えを突きつけています。
分子病態から紐解く心筋の沈黙と適応
心筋の機能不全は、単なる血流不足という物理的な問題ではなく、分子レベルでの高度な適応戦略の果てに生じます。論文では、iLVDの病態をスタンニング、冬眠、そして梗塞のスペクトラムとして定義しています。
心筋気絶(Stunning)
スタンニング(心筋気絶)は、一過性の虚血とその後の再灌流によって生じる「灌流と収縮のデカップリング(解離)」です。分子レベルでは、一時的に収縮装置の感度が低下していますが、血流自体は正常化しており、時間の経過とともに回復可能です。
冬眠心筋(Hibernation)
対照的に、冬眠心筋(Hibernation)は、慢性的かつ反復的な虚血に対する生存戦略です。心筋細胞は、細胞死(アポトーシス)を回避するために、自らの収縮機能を意図的にダウンレギュレートし、エネルギー消費を最小限に抑えます。これは細胞生存を優先した適応プロセスですが、この「眠れる心筋」を目覚めさせるには虚血基質の除去、すなわち血行再建が不可欠となります。
梗塞
さらに、梗塞は内膜側から外膜側へと波状(wavefront)に広がる不可逆的な壊死であり、心不全の負のリモデリングと致死的不整脈の温床となります。
iLVD患者の心臓内では、これら3つの異なる状態がパッチワークのように混在しており、それが血行再建に対する反応の多様性を生んでいるのです。
生存心筋(バイアビリティ)神話の崩壊とパラダイムシフト
長らく臨床現場では、生存能テスト(Viability testing)によって機能回復が期待できる領域を特定し、その領域を狙って血行再建を行うことが標準とされてきました。しかし、PARR-2試験やSTICH試験のバイアビリティサブ解析、そして最新のREVIVED-BCIS2試験の結果は、このドグマに冷や水を浴びせました。
STICH試験に参加した601人の解析では、バイアビリティの有無と血行再建による死亡リスクの低減効果には有意な相互作用が認められませんでした。さらにREVIVED試験においても、バイアビリティの範囲が広いからといってPCIの恩恵が増すわけではないことが示されました。
むしろ、予後を規定するのは回復可能な「冬眠心筋」の量ではなく、すでに不可逆的なダメージを受けた「瘢痕(スカー)」の広がりであることが浮き彫りになったのです。
この発見は、バイアビリティがあるから手術をする、ないからしないという二分法的なアルゴリズムが、現代の強力な薬物療法の前ではその意義を失いつつあることを示唆しています。
STICHとREVIVEDが突きつける血行再建の真実
血行再建の有効性を検証した二つのランドマーク試験を詳しく見ていきましょう。
STICH試験
まず、CABGの価値を決定づけたのがSTICH試験です。LVEFが35パーセント以下の患者1,212人を対象としたこの試験では、初期の4.7年時点では薬物療法単独群と死亡率に差がありませんでした。しかし、10年間の長期追跡を行ったSTICHES試験において、ついに有意差が現れました。全死亡率はバイパス群で59パーセント、薬物療法群で66パーセントとなり、バイパス術によって平均して18ヶ月の寿命延長がもたらされたのです。特に60歳未満の若年層でその恩恵が顕著でした。
REVIVED-BCIS2試験
一方、PCIに焦点を当てたREVIVED-BCIS2試験は、異なる結果を示しました。広範な冠動脈疾患(BCIS myocardial jeopardy score 6以上)と重度左室機能不全を持つ700人を対象としましたが、3.4年の追跡期間において、全死亡または心不全入院の発生率はPCI群で37.2パーセント、薬物療法単独群で38.0パーセントと、統計的な差は認められませんでした。PCIを行っても、6ヶ月から12ヶ月時点での左室駆出率の改善すら確認されなかったのです。
この乖離の背景には、薬物療法の劇的な進化があります。REVIVED試験(患者登録期間:2002-2007年)の患者は、STICH試験(患者登録期間:2013-2020年)の時代よりもはるかに洗練された治療を受けており、それが血行再建の上乗せ効果を相対的に小さくしたと考えられます。
現代の4本柱がもたらす圧倒的な生命予後
血行再建の是非を議論する前に、まず完遂すべきはガイドラインに基づく薬物療法(Guideline-Directed Medical Therapy:GDMT)です。論文では、現代の「4本柱(4 pillars)」の威力を具体的な数値で示しています。
ARNI(アンジオテンシン受容体ネプリライシン阻害薬)、ベータ遮断薬、MRA(ミネラルコルコロイド受容体拮抗薬)、そしてSGLT2阻害薬を組み合わせることで、50歳の患者では約8年、70歳の患者でも約5年の余命延長が期待できると推計されています。
また、除細動器(ICD)や心臓再同期療法(CRT)といったデバイス治療も極めて重要です。REVIVED試験の解析では、PCIを行っても不整脈死のリスクは減少しませんでした。これは虚血よりも「瘢痕」が不整脈の主因であるためであり、血行再建後であってもデバイス治療の適応を遅らせるべきではないという教訓を残しています。
明日からの実践
この論文から得られる知見を、明日からの診療や行動にどう活かすべきか。以下の3点を実践の柱とすると良いでしょう。
第一に、安定したiLVD患者における血行再建の適応は、予後改善ではなく「症状改善」を主眼に置くべきです。コントロール困難な狭心症がある場合はPCIやCABGが強力な選択肢となりますが、無症状の患者に対して予防的にPCIを勧める根拠は現在のエビデンスには乏しいと言わざるを得ません。
第二に、意思決定プロセスにおける「ハートチーム」と「共同意思決定(Shared Decision Making:SDM)」の徹底です。特にPCIを選択する場合、手技に伴う一過性の虚血(Stunning)が、脆弱な左室を容易に破綻させるリスクを認識しなければなりません。術前に右心カテで心拍出量や左室充満圧を評価し、必要に応じてImpellaなどの補助循環(MCS)を予防的に導入する計画性が求められます。
第三に、常に最新の臨床試験にアンテナを張ることです。現在、PCIとCABGを直接比較するSTICH3試験や、補助循環の最適解を探るPROTECT IV試験が進行中です。エビデンスは固定されたものではなく、常に更新される動的なものであるという認識を持つことが重要です。
本研究の新規性と残された課題(Limitation)
このレビューの新規性は、単なる手法の紹介に留まらず、iLVDを「虚血性か非虚血性か」という二元論ではなく、両者が混在したスペクトラムとして捉え直した点にあります。また、バイアビリティテストの限界を明確にし、薬物療法の進化を踏まえた新しい治療アルゴリズムを提示した点は、臨床現場に大きな指針を与えます。
しかし、課題(Limitation)も残されています。
第一に、iLVDの国際的な共通定義が依然として存在しないため、試験間の比較が困難な点です。
第二に、保存された駆出率を持つ心不全(HFpEF)における冠動脈疾患の影響については、いまだ十分なランダム化比較試験のデータが存在しません。
第三に、血行再建によって虚血負担が「実際にどれだけ軽減されたか」という生理学的評価と予後の関連が、多くの大規模試験で系統的に評価されていない点です。
最後に
現代のiLVD治療の基盤は「4本の柱」による強力な薬物療法であり、これが予後改善の最優先事項です。 血行再建は一律の実施から、狭心症やACS例に限定した「症状改善」を主目的とする戦略へと進化しています。 ハートチームによる意思決定と補助循環を活用した精緻な手技計画こそが、複雑な病態に対する最適解です。
参考文献
Ryan M, Truesdell AG, Murphy GJ, et al. Revascularization in Ischemic Left Ventricular Dysfunction: A Pathophysiology-Guided, Evidence-Based Approach. JACC Cardiovasc Interv. 2025;18:2977-2994.