はじめに:LDLと心血管疾患の因果関係をめぐる論争
動脈硬化性心血管疾患(ASCVD)は、心筋梗塞や虚血性脳卒中などの臨床症状を伴い、世界中で罹患率と死亡率の主要な原因となっています。この疾患の発症には多くの危険因子が関与していますが、中でも低密度リポ蛋白(LDL)は最も広範に研究されている因子の一つです。しかしながら、LDLとASCVDの因果関係については依然として懐疑的な意見も存在しています。
本論文は、European Atherosclerosis Society 欧州動脈硬化学会コンセンサスパネルによる声明であり、遺伝学研究、前向き疫学コホート研究、メンデル無作為化研究、および無作為化比較試験という複数の異なるアプローチから得られた証拠を統合的に評価しています。200以上の研究、200万人以上の参加者、2000万人年以上の追跡期間、15万件以上の心血管イベントを包括的に分析した結果、LDLがASCVDの原因であることを明確に示しています。
LDLの分子生物学的特性と動脈硬化への関与
LDLはアポリポ蛋白B(apoB)を含むリポ蛋白の一種で、血中コレステロールの主要な運搬体です。LDL粒子は直径20-25nmの球状構造をしており、中心部にエステル型コレステロールを、表面に遊離コレステロール、リン脂質、および1分子のapoBタンパク質を持っています。
動脈硬化の発症において鍵となるのは、LDLなどのapoB含有リポ蛋白が動脈内膜に保持(retention)され蓄積する過程です。生理的なLDLコレステロール(LDL-C)レベル(新生児の典型的な値である0.5-1.0 mmol/L(20-40 mg/dL)では、LDL粒子の保持確率と動脈硬化発症リスクは低いのですが、このレベルを超えると、LDLの動脈内膜内保持が始まり、マクロファージの泡沫化、慢性炎症などが生じ、動脈硬化プラークが進行性に発達します。
分子生物学的には、LDL受容体(LDLR)の機能が重要です。肝臓でのLDL受容体の発現が減ると、血中のLDL-Cが上昇し、血管内皮へのLDL粒子の流入・蓄積が促進されます。LDLRの発現量はPCSK9やHMG-CoA還元酵素などの酵素活性により調節されています。これらの経路をターゲットとした治療薬が近年の治療を進化させています。
臨床現場では、LDL粒子濃度そのものではなく、LDL粒子が運ぶコレステロール量(LDL-C)が測定されることが一般的です。通常の状態ではLDL-CとLDL粒子数は高い相関がありますが、代謝症候群、糖尿病、高トリグリセリド血症などの状態では、小型で高密度のコレステロール貧弱なLDL粒子が優位になるため、LDL-CがLDL粒子数を正確に反映しなくなることがあります。
遺伝性脂質代謝異常症からの証拠
家族性高コレステロール血症(FH)は、LDL受容体(LDLR)遺伝子の機能喪失型変異によって引き起こされる常染色体優性遺伝疾患です。ヘテロ接合体FH(HeFH)は世界で200-300人に1人の割合で発生し、未治療の場合4.5-12 mmol/L(約174〜464 mg/dL)のLDL-CレベルとASCVDリスクの顕著な上昇を示します。ホモ接合体FH(HoFH)はさらに稀で、出生時から13 mmol/L(約502 mg/dL)を超えるLDL-Cレベルを示し、小児期または青年期早期にほぼ普遍的にASCVDを発症します。
FH家系において、変異を継承した兄弟は継承しなかった兄弟と比べて明らかに高いLDL-Cレベルとそれに比例したASCVD生涯リスクを示します。逆に、PCSK9遺伝子の機能喪失型変異はLDL-Cレベルの低下とASCVDリスクの顕著な減少をもたらします。これらの自然実験とも言える遺伝学的所見は、LDLがASCVDを引き起こす強力な証拠を提供しています。LDL-CとASCVDリスクの“量的”な関係が浮き彫りになったとも言えます。
前向き疫学研究のメタ解析結果
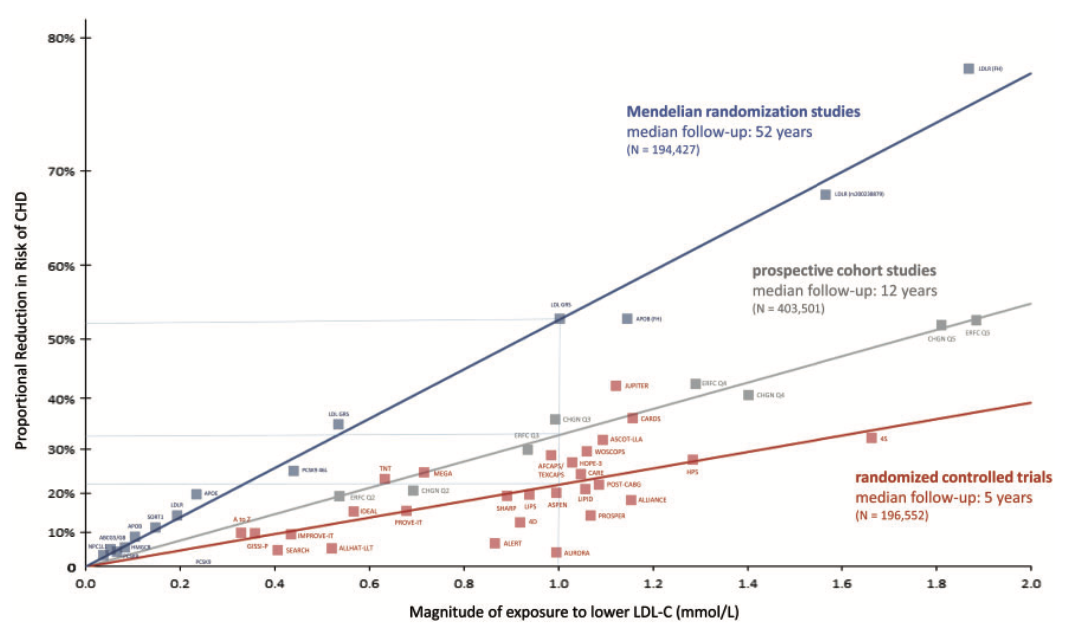
68の前向き研究から302,430人の個人参加者データを統合したEmerging Risk Factors Collaboration(ERFC)のメタ解析では、LDL-C濃度と非致死的心筋梗塞または冠動脈疾患死亡リスクとの間に連続的な対数直線的関係が認められました。LDL-Cが1 mmol/L(約38.6 mg/dL)上昇するごとに冠動脈イベントリスクが対数線形に増加します。
同様に、Prospective Studies Collaborationによる61の前向きコホート研究、892,337人のメタ解析でも、血漿総コレステロールと虚血性心疾患死亡リスクとの間に強い段階的な対数直線的関連が報告されています。
これらの大規模疫学研究は、LDL-C濃度が用量依存的にASCVDリスクを上昇させることを一貫して示しており、その関連性は非常に強固です(相対リスク比1.5-3.0程度)。
メンデル無作為化(Mendelian Randomization)研究の革新的な知見
Mendelian randomization(MR)は、生まれながらに決定される遺伝的変異を利用し、ランダム化比較試験と同等の因果性評価を行う手法です。LDL-CとASCVDの因果関係を評価する画期的なアプローチになり得ます。50以上の遺伝子の変異がLDL-C低下と関連しており、これらの変異がASCVDリスクの低下とも関連していることが明らかになりました。
特に注目すべきは、現在使用されているLDL-C低下療法の標的となる遺伝子(スタチンの標的であるHMGCR、エゼチミブの標的であるNPC1L1、PCSK9阻害薬の標的であるPCSK9)の変異が、LDL-Cを低下させるとともにASCVDリスクも比例して低下させることです。これらの遺伝的変異がLDL-Cを低下させるメカニズムはそれぞれ異なるにもかかわらず、LDL-C1mmol/L(38.7mg/dL)低下あたりのASCVDリスク減少効果はほぼ同等(約20-25%減少)でした。
この知見は、LDL-C低下による心血管ベネフィットが、その作用機序によらず、達成されたLDL-C低下の絶対量に比例することを強く示唆しています。
無作為化比較試験の決定的な証拠
26のスタチン試験、約170,000人を対象としたメタ解析では、スタチン治療によるLDL-C1mmol/L(38.7mg/dL)低下ごとに、主要心血管イベントの相対リスクが22%減少することが示されました。この効果は治療1年目ではやや小さく、その後治療期間が延びるにつれて一定の22-24%のリスク減少が持続します。
IMPROVE-IT試験では、スタチン単独療法と比較してエゼチミブを追加することでLDL-Cを0.40 mmol/L(15.5mg/dL)低下させ、主要心血管イベントを6.5%減少させました。
SHARP試験では、シンバスタチンとエゼチミブの併用療法がLDL-Cを0.85 mmol/L(32.9mg/dL)低下させ、主要心血管イベントを17%減少させました。
これらの結果は、スタチン単独療法で得られたLDL-C低下あたりのベネフィットと一致しています。
さらに画期的なのは、PCSK9阻害薬エボロクマブに関するFOURIER試験の結果です。スタチンにエボロクマブを追加することでLDL-Cを1.4 mmol/L(54.2mg/dL)低下させ(平均LDL-C 0.78 mmol/L(30 mg/dl))、心血管死亡、心筋梗塞または脳卒中の発生率を20%減少させました。GLAGOV試験では、エボロクマブによるLDL-C低下が冠動脈プラークの退縮をもたらし、その程度は達成されたLDL-Cレベルに直接比例していました。
因果関係の基準に対する評価
本論文では、Bradford Hillの因果関係基準に基づいてLDLとASCVDの関係を評価しています。その結果、LDLとASCVDの関連は以下の基準をすべて満たすことが明らかになりました:
- 生物学的妥当性:LDLは動脈硬化の開始と進行に直接関与
- 関連の強さ:単一遺伝子および多遺伝子性のLDL上昇は生涯リスクを著しく増加
- 生物学的勾配:用量依存的な対数直線的関連
- 時間的関係:LDL上昇はASCVD発症に先行
- 特異性:他の危険因子から独立した関連
- 一貫性:200以上の研究で一貫した結果
- 整合性:遺伝学研究、疫学研究、臨床試験の結果が一致
- 介入によるリスク減少:LDL低下療法が心血管イベントを減少
臨床的意義と実践への応用
この研究の最も重要な臨床的意義は、LDL-C低下による心血管ベネフィットが以下の3つの要素によって決定されることです:
- ベースラインのLDL-Cレベル
- 達成されたLDL-Cの絶対的減少幅
- 治療期間(曝露期間)
メンデル無作為化研究と無作為化試験のデータを統合すると、LDL-Cを1mmol/L(38.7mg/dL)低下させることで、治療期間に応じて以下のような相対リスク減少が期待できます:
- 1年目:約10%減少
- 2年目:約16%減少
- 3年目以降:年間約1.5%ずつ追加減少
- 5年間の治療:20-25%減少
- 40年間の治療(または曝露):50-55%減少
臨床医はこれらのデータを用いて、患者のベースラインリスク、LDL-Cレベル、期待される治療期間に基づいて、LDL-C低下療法の潜在的ベネフィットを個別に評価できます。特に、FH患者や高リスク患者では、早期からの積極的なLDL-C低下が推奨されます。
研究の限界と今後の課題
本研究にはいくつかの限界があります。第一に、ほとんどの臨床研究でLDL粒子濃度の代わりにLDL-Cが使用されているため、特に代謝異常を伴う患者では結果の解釈に注意が必要です。第二に、CETP阻害剤の効果については不明な点が残っており、進行中のREVEAL試験の結果が待たれます。第三に、遺伝的要因がLDL粒子の動脈壁保持 susceptibilityに影響を与える可能性がありますが、この分野の研究はまだ発展途上です。
医療実践への具体的な提言
本コンセンサス声明は、LDLが単なるリスクマーカーではなく、ASCVDの原因であることを明確にしています。この結論に基づき、以下のような実践的な提言が可能です:
- 早期介入の重要性:LDL-Cの影響は累積的であるため、高リスク患者では早期からの治療開始を考慮
- 治療目標:より低いLDL-Cレベルを達成することで、より大きな臨床的ベネフィットが期待
- 個別化医療:患者の遺伝的バックグラウンドや他の危険因子を考慮した治療戦略
- 長期管理:LDL-C低下療法は長期にわたって継続することが重要
特に、FH患者や既存のASCVDを持つ患者では、より積極的なLDL-C低下(1.8 mmol/L(70 mg/dL)以下を目標)が推奨されます。新しいPCSK9阻害薬の登場により、これまで困難であった極めて低いLDL-Cレベルの達成が可能になり、さらなる心血管イベントの減少が期待できます。
把握しておく一般的な知識
- 若年からの予防:高リスク者(例:FH)では、10代からの介入が推奨されます。
- LDL-Cの現在値を知る:まずは採血。目標値は70 mg/dL未満(1.8 mmol/L)です。
- 食事と運動:飽和脂肪酸の制限、植物ステロールの摂取、適度な有酸素運動が効果的です。
- 必要なら薬物療法:スタチンを中心に、必要に応じてエゼチミブやPCSK9阻害薬の導入も検討。
結論
「LDLはASCVDの原因である」。これはもはや仮説ではなく、膨大なエビデンスに裏打ちされた確固たる結論です。多様な証拠が示すのは、“どんな方法でも、LDL-Cを下げれば、リスクは下がる”という極めてシンプルかつ実践的なメッセージです。明日から、あなた自身や患者のLDL-Cと正面から向き合ってみてください。それが、心血管イベントを未然に防ぐ最良の一手です。
参考文献
Ference, B. A., Ginsberg, H. N., Graham, I., Ray, K. K., Packard, C. J., Bruckert, E., … & Catapano, A. L. (2017). Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. A consensus statement from the European Atherosclerosis Society Consensus Panel. European Heart Journal, 38(32), 2459-2472. https://doi.org/10.1093/eurheartj/ehx144