はじめに
従来の虚血性心疾患の理解は、主に太い冠動脈の閉塞や狭窄、すなわち「アテローム性動脈硬化」に焦点を当ててきました。しかし、冠動脈に目立った狭窄がないにもかかわらず、狭心症や心筋虚血の症状を呈する患者(INOCA:Ischemia with Non-Obstructive Coronary Arteries)が多数存在し、その予後は決して良好ではありません。
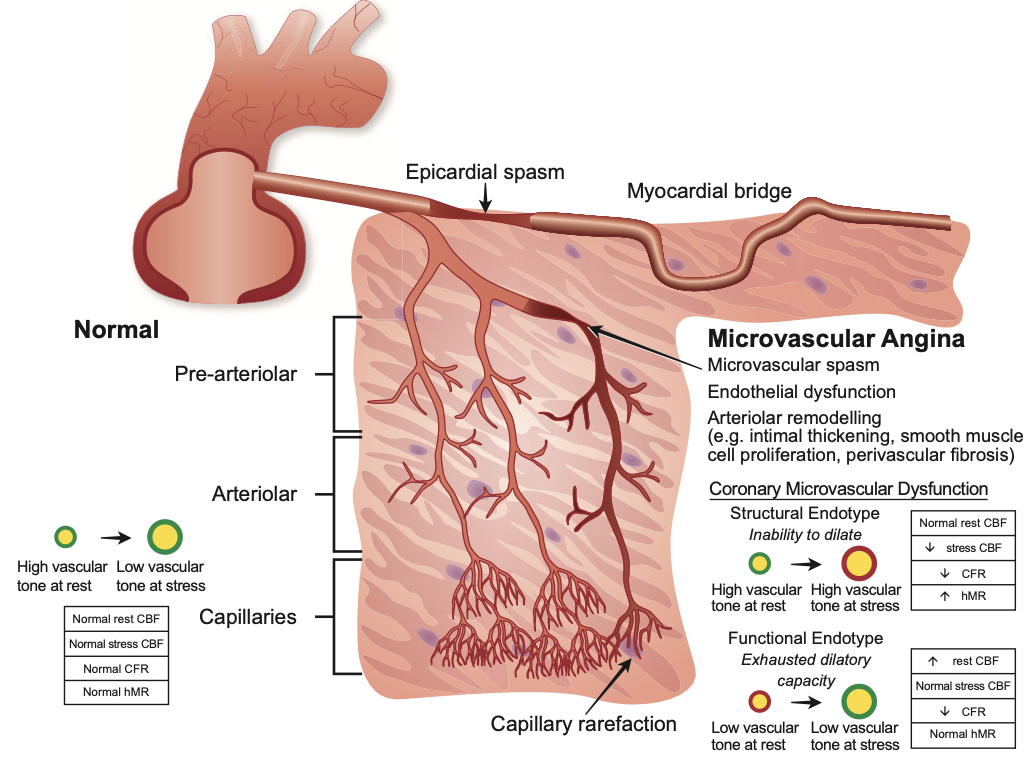
このINOCAの主要な原因とされるのが、直径500マイクロメートル以下の微細な血管の機能異常、すなわち冠微小血管機能障害(Coronary Microvascular Dysfunction: CMD)です。CMDは、心不全や心臓死といった有害なアウトカムと関連することが知られています。
一方、心室性期外収縮(Premature Ventricular Contractions: PVC)は、一般的に「ドキッ」「脈が飛ぶ」といった自覚症状を引き起こす不整脈ですが、その発生頻度(PVC Burden)が一定の閾値(例えば、24時間ホルター心電図中で総拍動数の0.5%以上、5.0%以上)を超えると、心不全の悪化や死亡率の上昇を予測する強力な因子となることが確立されています。
本研究の最も重要な新規性は、安定狭心症患者において、CMDの存在がPVCの発生および負荷量と独立して関連しているという、これまで見過ごされてきた病態生理学的連関を初めて、そして明確に示した点です。既存の研究ではPVCの予後予測的価値は広く認識されていましたが、その発生メカニズムにおけるCMDの直接的な関与は体系的に検討されていませんでした。
研究デザインとCMDの診断法
本研究は、合計300人の安定狭心症またはそれに相当する症状を持つ患者((年齢中央値70歳 [60-78歳]、男性187名 [62.3%]))を対象としたケースコントロール研究です(対象期間:2020年12月~2024年7月)。
患者は2つのコホートに分類され、いずれも標準化された微小循環機能評価を受けています。
- コホート1(n=260): ストレス心臓磁気共鳴画像法(Stress Cardiac Magnetic Resonance Imaging: CMR)によりCMDを診断しました。Stress CMRは心筋血流予備能(MPR)を定量的に評価する非侵襲的な最先端手法であり、CMDは89例(34.2%)に認められました。
- コホート2(n=40): 連続熱希釈法(Continuous Thermodilution)を用い、専門的なソフトウェア(CoroFlow)と診断基準に基づき評価しました。この手法は侵襲的なゴールドスタンダードに相当し、CMDは29例(72.5%)に認められました。
PVCの発生数は、CMD診断から6ヶ月以内に記録されたホルター心電図データを用いて定量的に分析されました。
定量的データが示す強力な連関性
研究結果は、CMDがPVC発生に及ぼす影響を、具体的な数値をもって示しています。
PVC発生数の比較
コホート1において、CMDを有する患者群は、CMDを有さない対照群と比較して、24時間あたりのPVC発生数の中央値(四分位範囲:IQR)が著しく高値でした。
- CMD非患者群: 93拍/24時間(IQR 5-599)
※ 第1四分位数 (Q1): 5拍 第3四分位数 (Q3): 599拍 - CMD患者群:635拍/24時間(IQR 112-4284)
- この差は統計的に極めて有意でした(P<.001)。
臨床的に重要なPVC負荷量の比較とオッズ比
心不全や死亡のリスクとして確立されているPVC負荷量の閾値(バーデン)超過率も、CMD群で顕著に増加していました。
コホート1の単変量解析では、CMDは以下のPVC負荷量閾値超過と関連する高いオッズ比(OR)を示しています。
| PVC負荷量閾値 | CMD群の超過率 | オッズ比 (OR) | 95% 信頼区間 (CI) | P値 |
|---|---|---|---|---|
| 0.5%以上 | 51.7% | 3.50 | 2.03-6.05 | <.001 |
| 5.0%以上 | 22.5% | 2.63 | 1.30-5.32 | .006 |
| 10.0%以上 | 13.5% | 3.18 | 1.25-8.09 | .01 |
さらに、年齢やその他の併存疾患を調整した多変量ロジスティック回帰分析においても、CMDはPVC負荷量閾値超過と関連する唯一の独立した予測因子として認められました。
- PVC負荷量 0.5%以上:調整済みOR 3.78 (95% CI, 2.21-6.74; P<.001)
- PVC負荷量 5.0%以上:調整済みOR 3.23 (95% CI, 1.51-6.93; P=.003)
- PVC負荷量 10.0%以上:調整済みOR 3.81 (95% CI, 1.41-10.27; P=.008)
コホート2(熱希釈法)の結果も同様の傾向を示しており、特に0.5%以上のPVC負荷量超過に対する調整済みORは9.70(95% CI, 1.04-90.91; P=.047)と非常に高い値を示しました。
病態生理学的考察と分子生物学的視点
本研究は、CMDとPVC発生の間に因果関係を示すものではありませんが、この強い独立した関連性は、両者をつなぐ共通の病態生理学的メカニズムの存在を強く示唆しています。
CMDは、微小血管の構造的・機能的異常により、心筋への血流(酸素供給)が不足する心筋虚血を引き起こします。この虚血が、心臓の電気的安定性に影響を与える主要なトリガーであると考えられます。
- 虚血と電気的不安定性:
- 心筋が虚血状態に陥ると、細胞内は酸素不足、pH低下(アシドーシス)、カリウム流出による細胞外カリウム濃度の上昇といった変化が起こります。
- これらの変化は、心筋細胞のイオンチャネル機能に影響を与え、再分極異常(特にEarly Afterdepolarizations: EADsやDelayed Afterdepolarizations: DADs)を生じさせます。
- EADsやDADsは、正常な興奮に続いて異常な興奮を引き起こすことで、期外収縮(PVC)の発生源(トリガー活動)となり得ます。
- 炎症と神経系の関与:
- CMDの内皮機能障害や構造的リモデリングの背景には、慢性的な低レベルの炎症や酸化ストレスが関与しています。
- 炎症性サイトカインや活性酸素種(ROS)は、心筋細胞の構造やイオンチャネルを障害し、電気的リモデリングを促進します。
- さらに、CMDの患者は自律神経の不均衡(交感神経の過剰亢進)を伴うことが多く、この交感神経刺激が微小血管の異常な収縮(攣縮)と、心筋の電気的興奮性の亢進を同時に引き起こし、PVCを誘発している可能性があります。実際、過去の研究では、心臓のコリン作動性ニューロンの機能障害が心室性不整脈の感受性を高めることが示されており、自律神経系の異常が共通の病態である可能性を裏付けています。
研究の限界(Limitations)
本研究は重要な知見を提供しましたが、その解釈には以下の限界を考慮する必要があります。
- 因果関係の非確立: 本研究はケースコントロール研究であり、CMDとPVCの関連性を示したものの、CMDがPVCの「原因」であるという因果関係を直接証明したものではありません。
- 地域限定的な観察研究: 欧州のある医療機関における連続患者のデータに基づく地域限定的な観察研究であり、一般化可能性(Generalizability)には限界があります。
- CMDの評価法: コホート1とコホート2でCMDの評価法が異なり、評価法間の特性の違いが結果に影響を与えている可能性を排除できません。
- 因果性の検討不足: 論文は病態生理学的相互作用の可能性を示唆していますが、この地域的観察研究ではCMDが心室性異所性活動の転帰試験で報告されていないことに言及し、今後の研究が必要であることを示唆しています。
明日からの実践
この学術的な知見は、臨床家、研究者、そして心臓の健康に関心を持つ皆様にとって、以下のような実践的な行動と洞察をもたらします。
医療従事者
- PVC患者の精査基準の再評価: 高いPVC負荷量(特に0.5%以上)を示す患者に対し、構造的心疾患がない場合でも、心臓の微小血管の状態(CMD)を積極的に評価する意識を持つことが重要です。心臓MRI(perfusion CMR)や侵襲的な冠血流予備能(CFR)/微小血管抵抗指数(IMR)の測定といった機能評価を検討する価値があります。
- 個別化された治療戦略: CMDとPVCが共存する患者においては、従来のPVC治療(例:β遮断薬、抗不整脈薬)に加え、CMDの背景にある病態(内皮機能障害、炎症、自律神経の不均衡)をターゲットとした治療(ACE阻害薬/ARB、スタチン、生活習慣改善)をより強化することが、PVCの改善と予後向上につながる可能性があります。
一般の方
- PVCの原因探求の重要性: 単に「ストレスや疲れで期外収縮が出た」と自己判断せず、PVCが頻繁に出る場合は、心臓の電気的な問題だけでなく、「心筋の酸素不足(虚血)」という血流の問題が隠れていないか、医師に相談し、CMDの可能性を含めた精密検査を依頼することが、将来的な心不全リスクの早期発見につながります。
- リスク因子管理の再認識: PVCや狭心症の症状がある場合、高血圧、脂質異常症、糖尿病といった古典的な心血管リスク因子の厳格な管理が、微小血管の機能を守り、ひいては不整脈の発生を抑制する最も実践的な予防策となります。
参考文献
Kahle, A. K., Wafaisade, B., Alken, F.-A., et al. (2025). Coronary Microvascular Dysfunction and Premature Ventricular Contractions in Patients With Stable Angina. JAMA Network Open, 8(12), e2546595. doi:10.1001/jamanetworkopen.2025.46595
参考